从某些性质看, NH3和H2O,NH 和H3O+,OH-和NH
和H3O+,OH-和NH ,NH
,NH 和O2-两两相似。
和O2-两两相似。
(1)试写出乙酸在液态氨中的形式_______ 。在水溶液中CH3COOH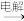 CH4+CO2,则乙酸在液态氨中的相应反应的方程式为
CH4+CO2,则乙酸在液态氨中的相应反应的方程式为_______ 。
(2)在液态氟化氢中,SbF5成为导电强的溶液,其离子方程式为_______ ,生成的两种物质的几何构型为_______ ,_______ 。
 和H3O+,OH-和NH
和H3O+,OH-和NH ,NH
,NH 和O2-两两相似。
和O2-两两相似。(1)试写出乙酸在液态氨中的形式
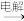 CH4+CO2,则乙酸在液态氨中的相应反应的方程式为
CH4+CO2,则乙酸在液态氨中的相应反应的方程式为(2)在液态氟化氢中,SbF5成为导电强的溶液,其离子方程式为
2007高二·安徽·竞赛 查看更多[1]
更新时间:2021-08-07 16:22:38
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】如图为氯及其化合物的“价−类”二维图。
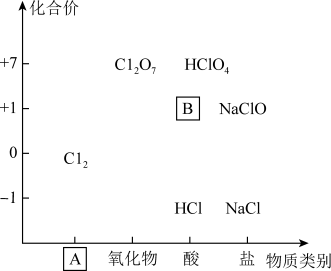
(1)二维图中A的类别为_______ ;B的名称为_______ 。
(2)已知 是一元强酸,写出
是一元强酸,写出 溶液与氢氧化钠溶液反应的离子方程式
溶液与氢氧化钠溶液反应的离子方程式_______ 。
(3)某同学研究HCl性质,进行如下预测:
①从物质类别上看,HCl属于酸,能与大理石反应,相应的离子方程式为_______ ;
②从化合价角度看,HCl具有_______ 性,能与_______ 发生反应(填标号)。
A.NaClOB.FeC.KMnO4D.NaOH
(4)某同学用强光照射氯水,同时使用数据采集器采集数据如图。
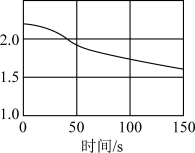
光照新制氯水,发生反应的化学方程式为_______ ;该同学采集的数据是_______ (填标号)。
A.氯水的pHB.氯离子的浓度C.溶液的电导率

(1)二维图中A的类别为
(2)已知
 是一元强酸,写出
是一元强酸,写出 溶液与氢氧化钠溶液反应的离子方程式
溶液与氢氧化钠溶液反应的离子方程式(3)某同学研究HCl性质,进行如下预测:
①从物质类别上看,HCl属于酸,能与大理石反应,相应的离子方程式为
②从化合价角度看,HCl具有
A.NaClOB.FeC.KMnO4D.NaOH
(4)某同学用强光照射氯水,同时使用数据采集器采集数据如图。

光照新制氯水,发生反应的化学方程式为
A.氯水的pHB.氯离子的浓度C.溶液的电导率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图所示是某化学兴趣小组探究溶液中离子浓度与溶液密度的关系。首先在水槽中加入200mL一定浓度的H2SO4溶液(ρ>1g/mL),同时将一个表面光滑的小球放入溶液中,小球悬浮在溶液中央。然后再进行以下操作,请回答问题:

(1)向溶液中逐滴加入与H2SO4溶液密度相同的Ba(OH)2溶液至反应完全,观察到的现象是___ ,反应的化学方程式是___ 。
(2)将Ba(OH)2溶液换成浓度相同(假设密度也相同)的Na2SO4溶液或Na2CO3溶液时(设反应后的体积为两溶液的体积和)。
①滴加Na2SO4溶液的过程中,小球的位置___ 。(填“上浮”、“下沉”或“不变”)
②滴加Na2CO3的过程中,观察到的现象是___ ,反应的化学方程式是___ 。

(1)向溶液中逐滴加入与H2SO4溶液密度相同的Ba(OH)2溶液至反应完全,观察到的现象是
(2)将Ba(OH)2溶液换成浓度相同(假设密度也相同)的Na2SO4溶液或Na2CO3溶液时(设反应后的体积为两溶液的体积和)。
①滴加Na2SO4溶液的过程中,小球的位置
②滴加Na2CO3的过程中,观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】纯净的过氧化氢( )为浅蓝色液体,能与水以任意比例混溶,
)为浅蓝色液体,能与水以任意比例混溶, 的空间结构示意图如下。
的空间结构示意图如下。
(1)下列关于 的说法中正确的是___________(填字母)。
的说法中正确的是___________(填字母)。
(2) 性质活泼,常用于废水处理、制备过氧化物等。
性质活泼,常用于废水处理、制备过氧化物等。
① 可使酸性
可使酸性 溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式为
溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式为___________
②在乙醚存在下, 可与酸性
可与酸性 反应生成一种
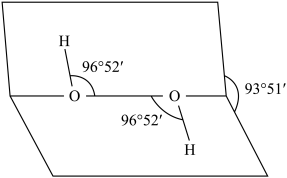
反应生成一种共价化合物 :二过氧 合铬的氧化物[化学式为: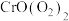 ],该反应是否为氧化还原反应
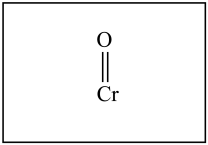
],该反应是否为氧化还原反应___________ (填“是”或“否”);试在图中补充完整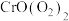 的分子结构
的分子结构___________ 。
③Cr在元素周期表的位置___________ ;基态铬原子的价电子排布图___________ ,它位于元素周期表的___________ 区。
(3) 可将
可将 氧化为硫酸。基态S原子电子占据最高能级的电子云轮廓图为
氧化为硫酸。基态S原子电子占据最高能级的电子云轮廓图为___________ 形, 的空间结构为
的空间结构为___________ 形。
 )为浅蓝色液体,能与水以任意比例混溶,
)为浅蓝色液体,能与水以任意比例混溶, 的空间结构示意图如下。
的空间结构示意图如下。
(1)下列关于
 的说法中正确的是___________(填字母)。
的说法中正确的是___________(填字母)。| A.分子中有非极性键 | B.沸点比水高 |
| C.分子是非极性分子 | D.氧原子的轨道发生了 杂化 杂化 |
 性质活泼,常用于废水处理、制备过氧化物等。
性质活泼,常用于废水处理、制备过氧化物等。①
 可使酸性
可使酸性 溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式为
溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式为②在乙醚存在下,
 可与酸性
可与酸性 反应生成一种
反应生成一种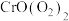 ],该反应是否为氧化还原反应
],该反应是否为氧化还原反应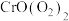 的分子结构
的分子结构
③Cr在元素周期表的位置
(3)
 可将
可将 氧化为硫酸。基态S原子电子占据最高能级的电子云轮廓图为
氧化为硫酸。基态S原子电子占据最高能级的电子云轮廓图为 的空间结构为
的空间结构为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
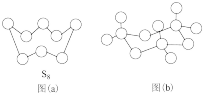
(1)图(a)为 的结构,其硫原子的杂化轨道类型为
的结构,其硫原子的杂化轨道类型为___________ 。
(2)气态三氧化硫以单分子形式存在,其分子的空间结构为___________ ;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为___________ 。
(3) 分子中所有原子均满足8电子构型,
分子中所有原子均满足8电子构型, 分子中
分子中 键和
键和 键的个数比为
键的个数比为___________ ,中心原子的杂化方式为___________ 。
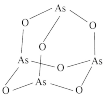
(4) 的分子结构如图所示,其中
的分子结构如图所示,其中 原子的杂化方式为
原子的杂化方式为___________ 。
(5) 中,
中, 原子的轨道杂化方式为
原子的轨道杂化方式为___________ 。

(1)图(a)为
 的结构,其硫原子的杂化轨道类型为
的结构,其硫原子的杂化轨道类型为(2)气态三氧化硫以单分子形式存在,其分子的空间结构为
(3)
 分子中所有原子均满足8电子构型,
分子中所有原子均满足8电子构型, 分子中
分子中 键和
键和 键的个数比为
键的个数比为(4)
 的分子结构如图所示,其中
的分子结构如图所示,其中 原子的杂化方式为
原子的杂化方式为
(5)
 中,
中, 原子的轨道杂化方式为
原子的轨道杂化方式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2010年中,广西某钛业有限公司工人对尚存有TiCl4残留物的过滤设备用水清洗时,发生“泄漏”事故,导致周边数十位村民身体不适。导致村民不适的泄漏物最大可能的是_______ ,相关的反应方程式是:_________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】银能与氢碘酸、氢硫酸反应,置换出氢气,请说明其原理______________________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】取100.0 mL自来水样,加入NH3-NH4Cl缓冲溶液控制pH=10.0,以铬黑T为指示剂,用0.01000mol/LEDTA滴定至溶液由红色变为蓝色,用去13.06 mL。另取100.0 mL该水样,以NaOH控制溶液pH=12~13,以钙指示剂指示终点,用去0.01000 mol/LEDTA 6.87 mL。再取100.0 mL该水样,加HCl调至pH为2~3,加入0.05000 mol/L BaCl2标液10.00 mL;待反应完全后,再加NH3-NH4Cl缓冲溶液控制pH=10.0,以铬黑T为指示剂,用0.01000 mol/L EDTA滴定至变为蓝色,用去18.75 mL。
(1)往0.25L 1.0 mol/L NH4Cl试剂加入多少克NaOH,可配制pH=10.0的氨性缓冲溶液_____ (pKb (NH3) =4.74)
(2)计算水样中Ca2+, Mg2+和SO 的含量,以mg/L表示
的含量,以mg/L表示______ 。
(3)写出滴定第一份水样到达终点时,铬黑T (以HIn2-表示)的指示反应方程式______ 。
(1)往0.25L 1.0 mol/L NH4Cl试剂加入多少克NaOH,可配制pH=10.0的氨性缓冲溶液
(2)计算水样中Ca2+, Mg2+和SO
 的含量,以mg/L表示
的含量,以mg/L表示(3)写出滴定第一份水样到达终点时,铬黑T (以HIn2-表示)的指示反应方程式
您最近一年使用:0次

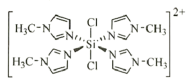
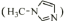 反应可以得到M2+,其结构如图所示:
反应可以得到M2+,其结构如图所示: