下列各物质中,按熔点由高到低的顺序排列正确的是
| A.CH4>SiH4>GeH4>SnH4 | B.KCl>NaCl>MgCl2>MgO |
| C.MgBr2<SiCl4<BN | D.金刚石>晶体硅>钠 |
2021高三·全国·专题练习 查看更多[1]
(已下线)考点35 晶体结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)
更新时间:2021-08-10 00:35:16
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是( )
| A.二氧化硅与二氧化碳都是共价化合物,且晶体类型相同 |
| B.氧气生成臭氧的过程中有化学键的断裂和生成 |
| C.因为N≡N键的键能比O≡0键的键能大,所以氮气的沸点比氧气的高 |
| D.硫晶体与氖晶体均是由单原子构成的分子晶体 |
您最近一年使用:0次
【推荐2】吡啶又称为氮苯,与苯都有大π键。吡啶可以看作苯分子中的一个(CH)被取代的化合物,其广泛用于医药工业原料。一种由糠醛制备吡啶的原理如下:
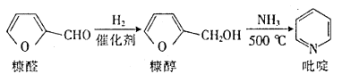
下列说法正确的是

下列说法正确的是
| A.糠醛、糠醇、吡啶分子中所有原子均可能共平面 |
| B.糠醛、糠醇、吡啶分子中所有碳原子的杂化方式相同 |
| C.吡啶与苯分子的熔点高低主要取决于所含化学键的键能 |
| D.吡啶与苯分子中参与形成大π键的各原子所提供的电子数相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】在298K、101kPa下,由稳定的单质发生反应生成1mol化合物的反应热叫该化合物的标准摩尔生成热△fHmθ。氧族元素氢化物a、b、c、d的生成热数据如图。下列判断正确的是


| A.沸点:H2O>H2S>H2Se>H2Te |
B.H2S(g)+ O2(g)=S(s)+H2O(1) △H=-265 kJ/mol O2(g)=S(s)+H2O(1) △H=-265 kJ/mol |
| C.H2Se(g)=Se(g)+H2(g) △H=+81 kJ/mol |
D.反应Te(s)+H2(g) H2Te(g)达平衡后升温,平衡常数将减小 H2Te(g)达平衡后升温,平衡常数将减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下面有关晶体的叙述中,正确的是( )
| A.在晶体中只要有阳离子就一定有阴离子 |
| B.离子晶体中只有离子键没有共价键,分子晶体中只有分子间作用力没有共价键 |
| C.分子晶体中分子间作用力越大,分子越稳定 |
| D.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关说法不正确的是
| A.NaBr属于离子化合物 | B.HCl分子中含极性共价键 |
C.热稳定性: | D.卤族元素在自然界中都以化合态存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述不正确的是( )
| A.原子晶体中共价键越强,熔点越高 |
| B.在卤族元素(F、Cl、Br、I)的氢化物中,HCl的沸点最低 |
| C.CaH2、Na2O2晶体的阴、阳离子个数比分别为2∶1、1∶1 |
| D.晶体熔点:金刚石>食盐>冰>干冰 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于物质性质的比较,正确的是( )
| A.相同温度下,水中的溶解度:NaHCO3>Na2CO3 |
| B.熔点:铯>钾>钠>钠和钾的合金 |
| C.熔沸点:HI>HBr>HCl>HF |
| D.热稳定性:HF>HCl>HBr>HI |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知 的熔点为2700℃,其晶胞结构如图所示。已知Si-28、C-12,下列说法错误的是
的熔点为2700℃,其晶胞结构如图所示。已知Si-28、C-12,下列说法错误的是
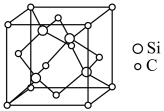
 的熔点为2700℃,其晶胞结构如图所示。已知Si-28、C-12,下列说法错误的是
的熔点为2700℃,其晶胞结构如图所示。已知Si-28、C-12,下列说法错误的是
A. 晶体中碳原子和硅原子均采用 晶体中碳原子和硅原子均采用 杂化 杂化 |
| B.硅单质的熔点高于2700℃ |
| C.距离硅原子最近的硅原子数为12 |
D.若晶胞参数为 ,则该晶体的密度为 ,则该晶体的密度为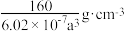 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】工业上制备粗硅的反应为 ,若C过量,还会生成SiC.下列叙述错误的是
,若C过量,还会生成SiC.下列叙述错误的是
 ,若C过量,还会生成SiC.下列叙述错误的是
,若C过量,还会生成SiC.下列叙述错误的是A.1个CO分子内只含有1个 键和2个 键和2个 键 键 |
| B.键能:C—H>Si—H,因此甲硅烷没有甲烷稳定 |
| C.键长:C—Si<Si—Si,因此熔点:SiC>Si |
| D.键长:C一C<Si—Si,因此C的还原性大于Si的还原性 |
您最近一年使用:0次



 键的大
键的大 能萃取碘水中的
能萃取碘水中的 ,体现了相似相溶原理
,体现了相似相溶原理

