某研究性学习小组设计实验探究铝等金属的性质:将铝片(不除氧化膜)投入浓氯化铜溶液中,铝表面很快出现一层海绵状暗红色物质,接下来铝片上产生大量气泡,触摸容器知溶液温度迅速上升,收集气体,检验其具有可燃性。若用同样的铝片投入同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。
(1)铝与氯化铜溶液能迅速反应,而与同浓度的硫酸铜溶液在短时间内不反应的原因可能是____ 。
a.氯化铜溶液酸性比同浓度的硫酸铜溶液酸性强
b.硫酸铜水解生成硫酸使铝钝化
c.氯离子能破坏氧化铝表面薄膜,而硫酸根离子不能
d.生成氯化铝溶于水,而生成硫酸铝不溶于水
请设计一个简单实验验证你的选择:_______ 。
(2)铝片表面出现的暗红色物质是_______ ,产生该物质的离子方程式是_______ ,用离子方程式解释产生气泡:_______ 。
(3)放出的气体是_______ ,请从有关物质的浓度、能量、是否有电化学作用等分析开始阶段产生气体的速率不断加快的原因是_______ 。
(4)某同学通过一定的实验操作,也能使铝片与硫酸铜溶液反应加快,他采取的措施可能是
(1)铝与氯化铜溶液能迅速反应,而与同浓度的硫酸铜溶液在短时间内不反应的原因可能是
a.氯化铜溶液酸性比同浓度的硫酸铜溶液酸性强
b.硫酸铜水解生成硫酸使铝钝化
c.氯离子能破坏氧化铝表面薄膜,而硫酸根离子不能
d.生成氯化铝溶于水,而生成硫酸铝不溶于水
请设计一个简单实验验证你的选择:
(2)铝片表面出现的暗红色物质是
(3)放出的气体是
(4)某同学通过一定的实验操作,也能使铝片与硫酸铜溶液反应加快,他采取的措施可能是
| A.用砂纸擦去铝片表面的氧化膜后投入硫酸铜溶液中 |
| B.把铝片投入热氢氧化钠溶液中一段时间后,取出洗涤,再投入硫酸铜溶液中 |
| C.向硫酸铜溶液中滴加氢氧化钠溶液,再投入铝片 |
| D.在铝片上捆上几枚铜钉后投入同浓度的硫酸铜溶液中 |
2021高三·浙江·专题练习 查看更多[1]
(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)
更新时间:2021-08-12 17:53:23
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】由单质A和化合物B两种粉末组成的混合物,在一定条件下可按下页框图所示关系进行转化:
请回答:
(1) A、B的化学式分别是_____________________ 、_____________________ 。
(2) 写出反应①的化学反应方程式____________________________________ 。
(3)写出反应②、③的离子方程式②___________________________________ ;
③_______________________________________________________________ 。
(4)若要保存F溶液,应采取什么措施?_______________________________ ;
为什么?__________________________________________________________ 。

请回答:
(1) A、B的化学式分别是
(2) 写出反应①的化学反应方程式
(3)写出反应②、③的离子方程式②
③
(4)若要保存F溶液,应采取什么措施?
为什么?

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某兴趣小组采用10.0g废易拉罐(含90%的Al,还含有少量的Fe、Mg等杂质)制备明矾[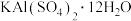 ]的实验流程如图:
]的实验流程如图:
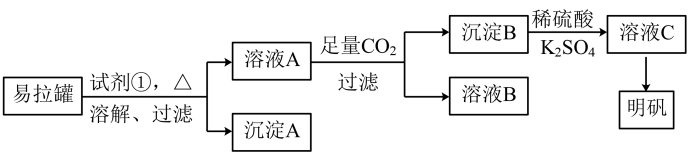
(1)试剂①应选用___________ (填字母)。
a.盐酸 b. 溶液 c.氨水 d.NaOH溶液
溶液 c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为___________ 。
(3)从溶液C中得到明矾的实验操作为___________ 、___________ 过滤。
(4)能否将步骤中的CO2溶液替换为盐酸?请回答并简述理由___________ 。
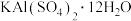 ]的实验流程如图:
]的实验流程如图:
(1)试剂①应选用
a.盐酸 b.
 溶液 c.氨水 d.NaOH溶液
溶液 c.氨水 d.NaOH溶液(2)易拉罐溶解过程中主要反应的化学方程式为
(3)从溶液C中得到明矾的实验操作为
(4)能否将步骤中的CO2溶液替换为盐酸?请回答并简述理由
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组用铝箔制备Al2O3、AlCl3·6H2O及明矾晶体,具体流程如下:

请回答:
(1)步骤I中发生的化学方程式__ ;步骤II发生的离子方程式___ 。
(2)步骤Ⅲ发生的化学方程式___ 。
(3)步骤Ⅴ,过滤时,用到的玻璃仪器有___ 。
(4)由于无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室需用下列装置制备。

①装置A中发生反应的离子方程式为_____ 。
②装置B中盛放饱和NaCl溶液,该装置的主要作用是____ 。
③F中试剂的作用是___ ,用球形干燥管装填适当试剂后也可起到F和G的作用,所装填的试剂为____ 。

请回答:
(1)步骤I中发生的化学方程式
(2)步骤Ⅲ发生的化学方程式
(3)步骤Ⅴ,过滤时,用到的玻璃仪器有
(4)由于无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室需用下列装置制备。

①装置A中发生反应的离子方程式为
②装置B中盛放饱和NaCl溶液,该装置的主要作用是
③F中试剂的作用是
您最近一年使用:0次
【推荐1】回答下列问题。
总结:乙酸的酸性
①___________ ;
②___________ ;
③___________ ;
④___________ 。
| 实验内容 | 实验现象 | 反应的化学方程式 |
| 向试管中加入约2mL乙酸溶液,然后滴入数滴紫色石蕊试液,观察颜色变化 | 溶液变红 | |
| 向试管中加入适量锌粒,然后加入约2mL冰醋酸溶液 | 溶液中有气泡生成 | |
| 向试管中加入适量碳酸钙,然后加入约2mL冰醋酸溶液 | 碳酸钙溶解,有大量气泡生成 | |
| 向试管中加入约2mLNaOH溶液,滴入数滴酚酞溶液,然后逐滴滴加乙酸溶液,观察颜色变化 | 溶液由红色逐渐变为无色 |
①
②
③
④
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:

(1)写出B中发生反应的化学方程式___________ 。
(2)E中为红色干布条,F中为红色湿布条,可观察到的现象是___________ ,对比E和F中现象的差异可得出的结论及解释是___________ 。
(3)试管C和D中试剂各为___________ 。
(4)装置G处发生反应的离子方程式为___________ 。
(5)用离子方程式表示试剂X的作用___________ 。
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
①“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式___________ 。
②需“密闭保存”的原因___________ 。

(1)写出B中发生反应的化学方程式
(2)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(3)试管C和D中试剂各为
(4)装置G处发生反应的离子方程式为
(5)用离子方程式表示试剂X的作用
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
| 注意事项: 1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。 2.密封保存,请勿与洁厕灵同时作用。 3.保质期为一年 |
②需“密闭保存”的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2: ,该反应中被氧化的元素是
,该反应中被氧化的元素是___________ (填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为___________ L。
(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率。(已知SO3熔点为16. 8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响。)

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是___________ 。
②实验过程中,需要通入氧气。试写出一个用如图所示装置制取氧气的化学方程式___________ 。
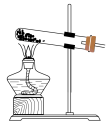
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是___________ 。
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是____________ 用含字母的代数式表示,不用化简)。
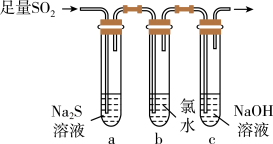
(3)某学习小组设计用如图装置验证二氧化硫的化学性质。
①能说明二氧化硫具有氧化性的实验现象为___________ 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是___________ (填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为___________ 。
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=___________ (用含硫微粒浓度的代数式表示)。
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:
 ,该反应中被氧化的元素是
,该反应中被氧化的元素是(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率。(已知SO3熔点为16. 8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响。)

①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是
②实验过程中,需要通入氧气。试写出一个用如图所示装置制取氧气的化学方程式

③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是
(3)某学习小组设计用如图装置验证二氧化硫的化学性质。
①能说明二氧化硫具有氧化性的实验现象为
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:

方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=
您最近一年使用:0次



