实验室用Na2SO3固体与70%的硫酸反应制取SO2气体时,利用刚吸收过少量HI气体的FeCl3溶液吸收SO2气体。
(1)FeCl3溶液与HI反应的离子方程式为___ 。
(2)有同学认为SO2气体通入刚吸收过少量HI气体的FeCl3溶液中,SO2首先与溶液中过量Fe3+反应,然后再与I2反应生成SO ,则SO
,则SO 、Fe3+、I2微粒的氧化性强弱顺序是:
、Fe3+、I2微粒的氧化性强弱顺序是:___ 。
(3)若用FeCl3溶液吸收SO2气体,吸收一段时间后,吸收液中一定存的离子有H+、Fe2+、Cl-、SO ,请设计实验,探究该吸收液中可能存在的主要离子(不考虑空气的CO2的影响)。
,请设计实验,探究该吸收液中可能存在的主要离子(不考虑空气的CO2的影响)。
①提出合理假设:
假设1:只存在HSO 、SO
、SO ;
;
假设2:既不存在HSO 、SO
、SO 也不存在Fe3+;
也不存在Fe3+;
假设3:___ 。
②设计实验方案,验证假设。请在答题卷上写出实验步骤以及预期现象和结论。限选实验试剂:3moL·L-1H2SO4。1moL·L-1NaOH、0.01moL·L-1KMnO4、20%KSCN、紫色石蕊试液、品红溶液。
(4)测定空气中SO2含量的方法是:把500L含SO2气体的空气通过20mL含0.00015molKMnO4的溶液中,充分反应后,再用0.0200mol/L的KI溶液滴定过量的KMnO4,消耗KI溶液25.0mL,则空气中的SO2含量为___ mg/L。(5SO2+2MnO +2H2O=2Mn2++5SO
+2H2O=2Mn2++5SO +4H+,10I-+2MnO
+4H+,10I-+2MnO +16H+=2Mn2++5I2+8H2O)
+16H+=2Mn2++5I2+8H2O)
(1)FeCl3溶液与HI反应的离子方程式为
(2)有同学认为SO2气体通入刚吸收过少量HI气体的FeCl3溶液中,SO2首先与溶液中过量Fe3+反应,然后再与I2反应生成SO
 ,则SO
,则SO 、Fe3+、I2微粒的氧化性强弱顺序是:
、Fe3+、I2微粒的氧化性强弱顺序是:(3)若用FeCl3溶液吸收SO2气体,吸收一段时间后,吸收液中一定存的离子有H+、Fe2+、Cl-、SO
 ,请设计实验,探究该吸收液中可能存在的主要离子(不考虑空气的CO2的影响)。
,请设计实验,探究该吸收液中可能存在的主要离子(不考虑空气的CO2的影响)。①提出合理假设:
假设1:只存在HSO
 、SO
、SO ;
;假设2:既不存在HSO
 、SO
、SO 也不存在Fe3+;
也不存在Fe3+;假设3:
②设计实验方案,验证假设。请在答题卷上写出实验步骤以及预期现象和结论。限选实验试剂:3moL·L-1H2SO4。1moL·L-1NaOH、0.01moL·L-1KMnO4、20%KSCN、紫色石蕊试液、品红溶液。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管A中, | |
| 步骤2: | |
| 步骤3:…… |
 +2H2O=2Mn2++5SO
+2H2O=2Mn2++5SO +4H+,10I-+2MnO
+4H+,10I-+2MnO +16H+=2Mn2++5I2+8H2O)
+16H+=2Mn2++5I2+8H2O)
更新时间:2021-08-21 15:05:06
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】焦亚硫酸钠 是常用的食品抗氧化剂之一。某研究小组进行如下实验:
是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一:焦亚硫酸钠的制取。采用如图装置 实验前已除尽装置内的空气
实验前已除尽装置内的空气 制取
制取 。装置Ⅱ中有
。装置Ⅱ中有 晶体析出,发生的反应为
晶体析出,发生的反应为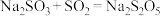 。
。
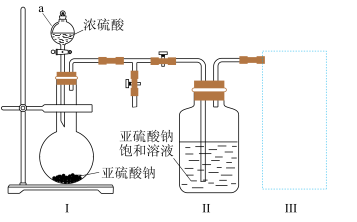
(1)A仪器的名称为:______ ,实验前要进行 ______ ;装置Ⅰ中产生气体的化学方程式为 ______
(2)浓硫酸______  能或不能
能或不能 用稀硫酸代替,原因是
用稀硫酸代替,原因是 ______
(3)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是______
(4)装置Ⅲ用于处理尾气,可选用如图的最合理装置 夹持仪器已略去
夹持仪器已略去 为
为 ______  填序号
填序号

实验二:葡萄酒中抗氧化剂残留量的测定。
(5)葡萄酒常用 作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量
作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量 以游离
以游离 计算
计算 的方案如下:
的方案如下:
葡萄酒样品100.00mL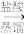 馏分
馏分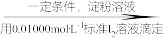 溶液出现蓝色且30s内不褪色
溶液出现蓝色且30s内不褪色 已知:滴定时反应的化学方程式为
已知:滴定时反应的化学方程式为
①按上述方案实验,消耗标准 溶液
溶液 ,该次实验测得样品中抗氧化剂的残留量
,该次实验测得样品中抗氧化剂的残留量 以游离
以游离 计算
计算 为
为 ______ 
②在上述实验过程中,若有部分HI被空气氧化,则测定结果______  填“偏高”“偏低”或“不变”
填“偏高”“偏低”或“不变” 。
。
 是常用的食品抗氧化剂之一。某研究小组进行如下实验:
是常用的食品抗氧化剂之一。某研究小组进行如下实验:实验一:焦亚硫酸钠的制取。采用如图装置
 实验前已除尽装置内的空气
实验前已除尽装置内的空气 制取
制取 。装置Ⅱ中有
。装置Ⅱ中有 晶体析出,发生的反应为
晶体析出,发生的反应为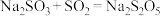 。
。
(1)A仪器的名称为:
(2)浓硫酸
 能或不能
能或不能 用稀硫酸代替,原因是
用稀硫酸代替,原因是 (3)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是
(4)装置Ⅲ用于处理尾气,可选用如图的最合理装置
 夹持仪器已略去
夹持仪器已略去 为
为  填序号
填序号

实验二:葡萄酒中抗氧化剂残留量的测定。
(5)葡萄酒常用
 作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量
作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量 以游离
以游离 计算
计算 的方案如下:
的方案如下:葡萄酒样品100.00mL
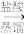 馏分
馏分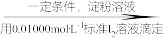 溶液出现蓝色且30s内不褪色
溶液出现蓝色且30s内不褪色 已知:滴定时反应的化学方程式为
已知:滴定时反应的化学方程式为
①按上述方案实验,消耗标准
 溶液
溶液 ,该次实验测得样品中抗氧化剂的残留量
,该次实验测得样品中抗氧化剂的残留量 以游离
以游离 计算
计算 为
为 
②在上述实验过程中,若有部分HI被空气氧化,则测定结果
 填“偏高”“偏低”或“不变”
填“偏高”“偏低”或“不变” 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室利用如图装置探究SO2还原CuO,并进一步检测产物含量。回答下列相关问题:

Ⅰ. SO2还原CuO探究
(1)装置A中发生反应的化学方程式_______________________________________ 。
(2)在制取SO2时,使用H2SO4溶液的浓度为__________ 时(填序号,从下列浓度中选取),制备SO2的速率明显快。请解释不选下列其它浓度硫酸的原因____________________ 。
a. 98% H2SO4 b.65% H2SO4 c. 5% H2SO4
(3)充分反应后,黑色固体变为红色。取C中适量的产物,加水后溶液显蓝色并有红色沉淀物,取红色沉淀物滴加盐酸,溶液又呈现蓝色并仍有少量红色不溶物,由此可以得出:
①已知SO2与CuO反应生成两种产物,写出该化学方程式___________________________ 。
②取红色沉淀物滴加盐酸,反应的离子方程式______________________________________ 。
Ⅱ.生成物中CuSO4含量检测
(4)用“碘量法”测定产物中CuSO4含量。取m g固体溶解于水配制成100mL溶液,取20.00mL溶液滴加几滴稀硫酸,再加入过量KI溶液,以淀粉为指示剂用Na2S2O3标准溶液滴定,相关化学反应为2Cu2++4I-=2CuI↓+I2,I2+I-⇌I ,I2+2S2O
,I2+2S2O =S4O
=S4O +2I-。
+2I-。
①若消耗0.1000mol/L Na2S2O3标准溶液VmL,则产物中CuSO4质量分数为____________ 。
②CuI沉淀物对I 具有强的吸附能力,由此会造成CuSO4质量分数测定值
具有强的吸附能力,由此会造成CuSO4质量分数测定值_______ (填“偏大”或“偏小”)。

Ⅰ. SO2还原CuO探究
(1)装置A中发生反应的化学方程式
(2)在制取SO2时,使用H2SO4溶液的浓度为
a. 98% H2SO4 b.65% H2SO4 c. 5% H2SO4
(3)充分反应后,黑色固体变为红色。取C中适量的产物,加水后溶液显蓝色并有红色沉淀物,取红色沉淀物滴加盐酸,溶液又呈现蓝色并仍有少量红色不溶物,由此可以得出:
①已知SO2与CuO反应生成两种产物,写出该化学方程式
②取红色沉淀物滴加盐酸,反应的离子方程式
Ⅱ.生成物中CuSO4含量检测
(4)用“碘量法”测定产物中CuSO4含量。取m g固体溶解于水配制成100mL溶液,取20.00mL溶液滴加几滴稀硫酸,再加入过量KI溶液,以淀粉为指示剂用Na2S2O3标准溶液滴定,相关化学反应为2Cu2++4I-=2CuI↓+I2,I2+I-⇌I
 ,I2+2S2O
,I2+2S2O =S4O
=S4O +2I-。
+2I-。①若消耗0.1000mol/L Na2S2O3标准溶液VmL,则产物中CuSO4质量分数为
②CuI沉淀物对I
 具有强的吸附能力,由此会造成CuSO4质量分数测定值
具有强的吸附能力,由此会造成CuSO4质量分数测定值
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某学校化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物的性质,设计如下实验。请回答下列问题:
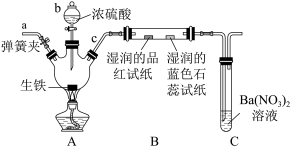
(1)甲同学按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为___________ 实验开始前打开弹簧夹,向a处通入 ,其目的是
,其目的是___________ ,实验过程中将浓硫酸加入装置A中的操作是___________ 。
(2)要证明 具有漂白性,在装置B中观察到
具有漂白性,在装置B中观察到_____ 现象。装置C中有白色沉淀生成,写出该反应的离子方程式:___________ 。
(3)乙同学认为装置A中还会产生 气体,请写出产生
气体,请写出产生 的化学方程式:
的化学方程式:_____ ,为了验证装置A中产生的气体中含有 ,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为c→( )→( )→( )(填序号)
,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为c→( )→( )→( )(填序号) _____ 。
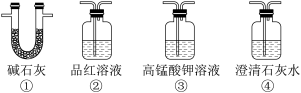

(1)甲同学按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为
 ,其目的是
,其目的是(2)要证明
 具有漂白性,在装置B中观察到
具有漂白性,在装置B中观察到(3)乙同学认为装置A中还会产生
 气体,请写出产生
气体,请写出产生 的化学方程式:
的化学方程式: ,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为c→( )→( )→( )(填序号)
,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为c→( )→( )→( )(填序号) 
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】以下是有关铝的实验探究,请回答相关问题:
(1)向集满 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:___________ 。
(2)向铝粉中添加少量 固体并充分混合,将其加热到1000℃时可与
固体并充分混合,将其加热到1000℃时可与 反应制备
反应制备 ,已知
,已知 溶液显酸性,下列说法正确的是___________。
溶液显酸性,下列说法正确的是___________。
(3)用打磨过的铝片进行如下实验,下列分析不合理的是___________。

(4)为探究铝片(未打磨)与 溶液的反应,实验如下:
溶液的反应,实验如下:
下列说法不正确的是___________。
(5)某铝土矿的主要成分为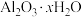 ,还含有
,还含有 和
和 杂质。称取
杂质。称取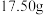 铝土矿样品,加入
铝土矿样品,加入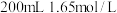 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。
①该试样中 的物质的量为
的物质的量为___________ mol。
②样品中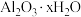 的x=
的x=___________ 。
(1)向集满
 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:(2)向铝粉中添加少量
 固体并充分混合,将其加热到1000℃时可与
固体并充分混合,将其加热到1000℃时可与 反应制备
反应制备 ,已知
,已知 溶液显酸性,下列说法正确的是___________。
溶液显酸性,下列说法正确的是___________。A. 是一种金属材料 是一种金属材料 |
B. 与足量氢氧化钠溶液共热时生成氢氧化铝和氨气 与足量氢氧化钠溶液共热时生成氢氧化铝和氨气 |
C.少量 能够破坏Al表面的 能够破坏Al表面的 薄膜 薄膜 |
D. 与足量盐酸反应的离子方程式为 与足量盐酸反应的离子方程式为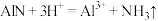 |

| A.①中铝片表面被浓硝酸氧化,生成了一层致密的氧化物薄膜,阻止了酸与内层金属的进一步反应 |
| B.②中产生的气泡是氮氧化合物,不是氢气 |
C.③中沉淀溶解的离子方程式是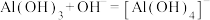 |
| D.②中加水稀释过程中,仅发生了氧化还原反应 |
 溶液的反应,实验如下:
溶液的反应,实验如下: |  | |
| 无明显现象 | 铝片表面产生细小气泡 | 出现白色沉淀,产生大量气泡(经检验为 和 和 ) ) |
A. 溶液呈碱性 溶液呈碱性 |
B.对比Ⅰ、Ⅲ,推测 溶液能破坏铝表面的氧化膜 溶液能破坏铝表面的氧化膜 |
C.Ⅳ溶液中可能存在大量 |
D.推测出现白色浑浊的可能原因: |
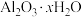 ,还含有
,还含有 和
和 杂质。称取
杂质。称取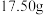 铝土矿样品,加入
铝土矿样品,加入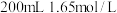 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。①该试样中
 的物质的量为
的物质的量为②样品中
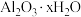 的x=
的x=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
(1)ClO2的制备:
已知:SO2+NaClO3+H2SO4=2ClO2↑+2NaHSO4
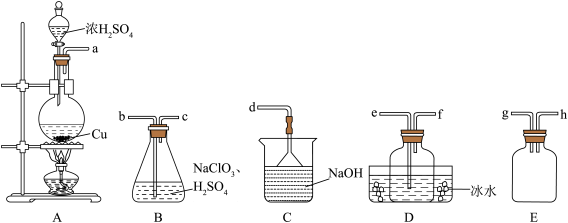
①装置A中反应的化学方程式为________________ 。
②欲收集干燥的ClO2,选择上图中的装置,其连接顺序为A→_______ 、_______ 、_______ →C(按气流方向)。
③装置D的作用是_______________ 。
(2)ClO2与Na2S的反应
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究Ⅰ中反应的产物。

④ClO2与Na2S反应的离子方程式为___________ 。用于处理含硫废水时,ClO2相对于Cl2的优点是______________ (任写一条)。
(1)ClO2的制备:
已知:SO2+NaClO3+H2SO4=2ClO2↑+2NaHSO4

①装置A中反应的化学方程式为
②欲收集干燥的ClO2,选择上图中的装置,其连接顺序为A→
③装置D的作用是
(2)ClO2与Na2S的反应
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究Ⅰ中反应的产物。

| 操作步骤 | 实验现象 | 结论 |
| 取少量I中溶液于试管甲中,滴加品红溶液和盐酸 | 品红始终不褪色 | ①无 |
| 另取少量I中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ② | 有SO42−生成 |
| ③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管丙内 | 有白色沉淀生成 | 有Cl−生成 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.学生利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取 晶体。(图中夹持及尾气处理装置均已略去)
晶体。(图中夹持及尾气处理装置均已略去)
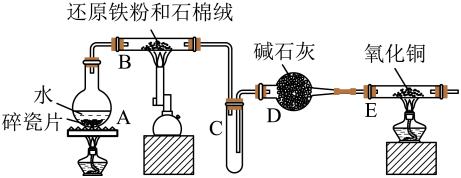
回答下列问题:
(1)所用铁粉中若有杂质,欲除去不纯铁粉中混有的铝粉可以选用的试剂为___________ (填序号),涉及反应的离子方程式为___________ 。
a.稀盐酸 b.氢氧化钠溶液 c.浓硫酸 d. 溶液
溶液
(2)反应发生后装置B中发生反应的化学方程式是___________ ,D装置的作用:___________ 。
(3)E装置中的现象是___________ 。
Ⅱ.该小组学生把B中反应后的产物加入足量的盐酸,过滤,用上述滤液制取 晶体,设计流程如下:
晶体,设计流程如下:
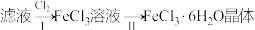
(4)用离子方程式表示步骤I中通入 的作用
的作用___________ 。
(5)步骤Ⅱ的操作为___________ 、___________ 、___________ 、自然晾干。
 晶体。(图中夹持及尾气处理装置均已略去)
晶体。(图中夹持及尾气处理装置均已略去)
回答下列问题:
(1)所用铁粉中若有杂质,欲除去不纯铁粉中混有的铝粉可以选用的试剂为
a.稀盐酸 b.氢氧化钠溶液 c.浓硫酸 d.
 溶液
溶液(2)反应发生后装置B中发生反应的化学方程式是
(3)E装置中的现象是
Ⅱ.该小组学生把B中反应后的产物加入足量的盐酸,过滤,用上述滤液制取
 晶体,设计流程如下:
晶体,设计流程如下: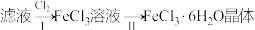
(4)用离子方程式表示步骤I中通入
 的作用
的作用(5)步骤Ⅱ的操作为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某厂以工业粗盐(含Ca2+、 Mg2+、SO 等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,其工艺流程如下图所示:
等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,其工艺流程如下图所示:
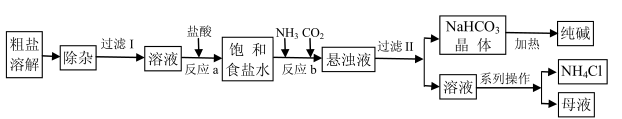
请回答下列问题:
(1)“除杂”步骤中需加入两种试剂,按加入顺序写出其名称____________ 。
(2)写出“反应a”的离子方程式___________ ;写出“反应b”的化学方程式___________ 。
(3)“过滤II”所得“溶液”中除NH 和Cl-外,还存在的阳离子有
和Cl-外,还存在的阳离子有___________ ,阴离子有___________ ;对该溶液进行的“系列操作”包括___________ 。
(4)上述工艺流程中可循环利用的物质有___________ 。
(5)工业纯碱的等级标准如下表所示:
称取某纯碱样品10.00g, 加入适量水溶解,再加入过量CaCl2溶液,充分反应后过滤、洗涤沉淀、干燥,称得沉淀质量为9.33g。请通过计算判断该纯碱样品的等级___________ 。
 等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,其工艺流程如下图所示:
等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,其工艺流程如下图所示:
请回答下列问题:
(1)“除杂”步骤中需加入两种试剂,按加入顺序写出其名称
(2)写出“反应a”的离子方程式
(3)“过滤II”所得“溶液”中除NH
 和Cl-外,还存在的阳离子有
和Cl-外,还存在的阳离子有(4)上述工艺流程中可循环利用的物质有
(5)工业纯碱的等级标准如下表所示:
| 等级 | 优等品 | 一等品 | 合格品 |
| Na2CO3含量1% | ≥99.2 | ≥98.8 | ≥98.0 |
称取某纯碱样品10.00g, 加入适量水溶解,再加入过量CaCl2溶液,充分反应后过滤、洗涤沉淀、干燥,称得沉淀质量为9.33g。请通过计算判断该纯碱样品的等级
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】据报道,2002年某市一辆满载砒霜的大货车翻下山坡,少量砒霜散落河水中。有关部门紧急采取措施。已知砒霜的化学式为:As2O3,剧毒,在低温下微溶于水,溶于水后生成亚砷酸,亚砷酸为三元弱酸。请回答下列问题:
(1)有关部门采取措施中加入一种物质。这种物质是___ (写名称),写出与亚砷酸在水中反应的化学方程式___ 。
(2)古时确定人是否是砒霜中毒死亡,常用马氏试砷法。其原理是在含砒霜的物质中加入Zn和稀H2SO4,得到一种气体A。加热A,在试管中得到砷镜。写出上述两个化学方程式___ 、___ 。
(3)砒霜与面粉、淀粉、味精及小苏打极其相似,容易误食中毒,急救方法之一是,立即将中毒者移离现场,灌服氢氧化铁胶体或悬浊液(12%硫酸亚铁溶液与20%氧化镁等量混合)并进行催吐,写出制备氢氧化铁胶体或悬浊液的反应原理___ (用方程式表示)。经过上述催吐后再进一步药物处理,即可得救。
(1)有关部门采取措施中加入一种物质。这种物质是
(2)古时确定人是否是砒霜中毒死亡,常用马氏试砷法。其原理是在含砒霜的物质中加入Zn和稀H2SO4,得到一种气体A。加热A,在试管中得到砷镜。写出上述两个化学方程式
(3)砒霜与面粉、淀粉、味精及小苏打极其相似,容易误食中毒,急救方法之一是,立即将中毒者移离现场,灌服氢氧化铁胶体或悬浊液(12%硫酸亚铁溶液与20%氧化镁等量混合)并进行催吐,写出制备氢氧化铁胶体或悬浊液的反应原理
您最近一年使用:0次

 和
和 发生核聚变,生成新的核素并释放出
发生核聚变,生成新的核素并释放出


