硒和硫是同一主族元素,二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或H2SO4反应生成SeO2以回收Se。完成下列填空:
(1)Se和一定量的浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3反应的化学方程式:________________________________________ 。
(2)已知:Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O===Se+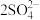 +4H+,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是
+4H+,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是________________________________________ 。
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①_____SeO2+_______KI+______HNO3=__________Se+__________I2+__________KNO3+_______H2O
②I2+2Na2S2O3===Na2S4O6+2NaI
配平化学方程①,并标出电子转移的方向和数目。__________
(4)实验中,准确称量SeO2样品0.1500g,消耗了0.2000mol·L-1的Na2S2O3溶液25.00mL,所测样品中SeO2的质量分数为__________ 。
(1)Se和一定量的浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3反应的化学方程式:
(2)已知:Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O===Se+
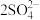 +4H+,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是
+4H+,SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①_____SeO2+_______KI+______HNO3=__________Se+__________I2+__________KNO3+_______H2O
②I2+2Na2S2O3===Na2S4O6+2NaI
配平化学方程①,并标出电子转移的方向和数目。
(4)实验中,准确称量SeO2样品0.1500g,消耗了0.2000mol·L-1的Na2S2O3溶液25.00mL,所测样品中SeO2的质量分数为
11-12高三·浙江温州·阶段练习 查看更多[16]
2012年上海市高考化学试题吉林省白城市通榆县第一中学2020届高三上学期第一次月考化学试题北京市第二十中学2018届高三10月月考化学试题安徽省合肥市第六中学2017-2018学年高一上学期期中考试化学试题山东省济宁市微山县第二中学2018届高三上学期第一次月考化学试题2018届高三一轮复习化学:考点14-氧化还原反应的计算2017届湖北省荆州中学高三上学期8月摸底化学试卷2016届辽宁省实验中学分校高三上期中测试理综化学试卷2016届山西平遥中学等重点中学高三第三次练兵化学试卷2016届山西省晋中市四校高三上学期期中联考化学试卷2016届江西省高安市第二中学高三上学期第二次段考化学试卷2016届重庆市万州二中高三上学期9月月考化学试卷2016届山东省枣庄市第二中学高三9月阶段性学情检测化学试题(已下线)2013-2014黑龙江省鹤岗一中高二下学期期末考试化学试卷(已下线)2012-2013学年湖北省部分重点中学高一秋季期中联考化学试卷(已下线)2013届浙江省乐清市第二中学高三第一次月考化学试卷
更新时间:2012-11-23 14:09:10
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】回答下列问题:
I.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究H2O2的性质,能证明H2O2有还原性的实验是___________ (填序号),可作为证据的实验现象是___________ (填字母序号)。
(2)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO___________ H2O2(填“>”或“<”);当有0.1molO2生成时,转移电子的物质的量为___________ mol。
II.全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取,相关反应如下,配平此化学方程式。___________
(3)_____NaIO3+______NaHSO3——_____NaHSO4+_______Na2SO4+_____I2+_____H2O
III.锑(Sb)被广泛用于生产各种阻燃剂、合金、陶瓷、半导体元件、医药用品等。以辉锑矿为原料制备金属锑的一种工艺流程如下。已知:辉锑矿的主要成分为Sb2S3,还含As2S5、PbS、CuO和SiO2等;浸出液主要含盐酸和SbCl3,还含SbCl5、CuCl2、AlCl3和PbCl2等。
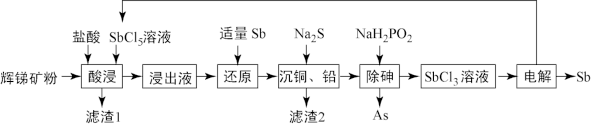
(4)“酸浸”过程中SbCl5和Sb2S3反应有S生成,该反应的还原产物是___________ (填化学式)。
(5)写出“还原”反应的化学方程式___________ 。
I.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究H2O2的性质,能证明H2O2有还原性的实验是
| 序号 | 实验 | 实验现象 |
| 1 | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去; b.有大量气泡产生 |
| 2 | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
(2)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO
II.全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取,相关反应如下,配平此化学方程式。
(3)_____NaIO3+______NaHSO3——_____NaHSO4+_______Na2SO4+_____I2+_____H2O
III.锑(Sb)被广泛用于生产各种阻燃剂、合金、陶瓷、半导体元件、医药用品等。以辉锑矿为原料制备金属锑的一种工艺流程如下。已知:辉锑矿的主要成分为Sb2S3,还含As2S5、PbS、CuO和SiO2等;浸出液主要含盐酸和SbCl3,还含SbCl5、CuCl2、AlCl3和PbCl2等。

(4)“酸浸”过程中SbCl5和Sb2S3反应有S生成,该反应的还原产物是
(5)写出“还原”反应的化学方程式
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】铁在热的稀 中反应,其主要还原产物为
中反应,其主要还原产物为 ,而在冷的稀
,而在冷的稀 中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为
中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为 。请分析如图,回答有关问题。
。请分析如图,回答有关问题。
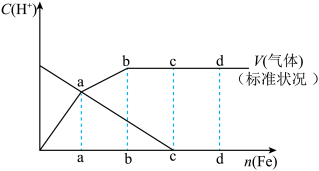
(1)假设在任一气体产生的曲线段内只有一种还原产物,试配平由b点到c点时的化学反应方程式:_____ Fe+____ HNO3—____ Fe(NO3)3+_________ +____ H2O
(2)判断从o点到a点时的还原产物,应是___________
(3)a点到b点时产生还原产物为_________ ,其原因是______________
(4)已知达到d点时反应完全结束,此时溶液中的主要阳离子为____________ 。
 中反应,其主要还原产物为
中反应,其主要还原产物为 ,而在冷的稀
,而在冷的稀 中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为
中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为 。请分析如图,回答有关问题。
。请分析如图,回答有关问题。 
(1)假设在任一气体产生的曲线段内只有一种还原产物,试配平由b点到c点时的化学反应方程式:
(2)判断从o点到a点时的还原产物,应是
(3)a点到b点时产生还原产物为
(4)已知达到d点时反应完全结束,此时溶液中的主要阳离子为
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下:
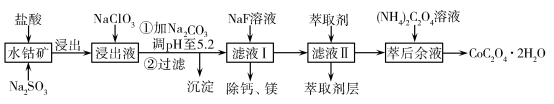
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②酸性条件下,ClO 不会氧化Co2+,ClO
不会氧化Co2+,ClO 转化为Cl-;③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
转化为Cl-;③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中加入Na2SO3的主要目的是________ 。
(2)向浸出液中加入NaClO3的离子反应方程式:________ 。
(3)已知:常温下NH3·H2O NH4++OH- Kb=1.8×10-5
NH4++OH- Kb=1.8×10-5
H2C2O4 H++HC2O4- Ka1=5.4×10-2 HC2O4-
H++HC2O4- Ka1=5.4×10-2 HC2O4- H++C2O42- Ka2=5.4×10-5
H++C2O42- Ka2=5.4×10-5
则该流程中所用(NH4)2C2O4溶液的pH________ 7(填“>”或“<”或“=”)。
(4)加入(NH4)2C2O4 溶液后析出晶体,再过滤、洗涤,洗涤时可选用的试剂有:________ 。
A.蒸馏水 B.自来水
C.饱和的(NH4)2C2O4溶液 D.稀盐酸
(5)萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是________ ;其使用的适宜pH范围是________ 。
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5


已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②酸性条件下,ClO
 不会氧化Co2+,ClO
不会氧化Co2+,ClO 转化为Cl-;③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
转化为Cl-;③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:| 沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)浸出过程中加入Na2SO3的主要目的是
(2)向浸出液中加入NaClO3的离子反应方程式:
(3)已知:常温下NH3·H2O
 NH4++OH- Kb=1.8×10-5
NH4++OH- Kb=1.8×10-5H2C2O4
 H++HC2O4- Ka1=5.4×10-2 HC2O4-
H++HC2O4- Ka1=5.4×10-2 HC2O4- H++C2O42- Ka2=5.4×10-5
H++C2O42- Ka2=5.4×10-5则该流程中所用(NH4)2C2O4溶液的pH
(4)加入(NH4)2C2O4 溶液后析出晶体,再过滤、洗涤,洗涤时可选用的试剂有:
A.蒸馏水 B.自来水
C.饱和的(NH4)2C2O4溶液 D.稀盐酸
(5)萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5

您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐1】在含砷废水中,砷元素多以+3和+5价的形式存在。工业上常利用 磁性纳米盘等吸附剂处理含砷废水,实现水体达标排放。
磁性纳米盘等吸附剂处理含砷废水,实现水体达标排放。
(1) 水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图1所示。
水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图1所示。
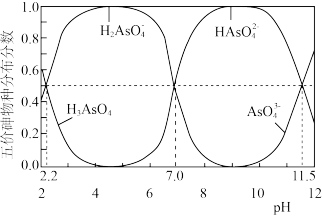
图1
① 分子中
分子中 的空间构型为
的空间构型为_______ ,将NaOH溶液滴入 溶液中,初始反应的离子方程式为
溶液中,初始反应的离子方程式为_______ 。
② 第一步电离方程式
第一步电离方程式 ,其电离常数为
,其电离常数为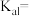
_______ 。
(2)① 磁性纳米盘制备:在一定条件,将
磁性纳米盘制备:在一定条件,将 的
的 和PVP溶于水中并加热,滴加过量NaOH溶液生成
和PVP溶于水中并加热,滴加过量NaOH溶液生成 ,再加入amL
,再加入amL 的
的 溶液。充分反应后(
溶液。充分反应后(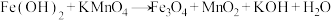 ,未配平),可制得
,未配平),可制得 磁性纳米盘。制备过程中需严格控制
磁性纳米盘。制备过程中需严格控制 溶液的用量,则a=
溶液的用量,则a=_______ 。
② 磁性纳米盘对酸性水中三价砷的去除能力远比五价砷的弱,可利用其中的
磁性纳米盘对酸性水中三价砷的去除能力远比五价砷的弱,可利用其中的 将酸性废水中的
将酸性废水中的 氧化成
氧化成 除去,反应过程中生成
除去,反应过程中生成 ,则反应的离子方程式为
,则反应的离子方程式为_______ 。
③ 磁性纳米盘处理含砷废水时,水中
磁性纳米盘处理含砷废水时,水中 、
、 、
、 和
和 对
对 的吸附率的影响如图2。
的吸附率的影响如图2。 对
对 吸附去除几乎没有影响,
吸附去除几乎没有影响, 对
对 吸附去除影响较大。请解释
吸附去除影响较大。请解释 抑制
抑制 吸附去除的可能原因
吸附去除的可能原因_______ 。

 磁性纳米盘等吸附剂处理含砷废水,实现水体达标排放。
磁性纳米盘等吸附剂处理含砷废水,实现水体达标排放。(1)
 水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图1所示。
水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图1所示。
图1
①
 分子中
分子中 的空间构型为
的空间构型为 溶液中,初始反应的离子方程式为
溶液中,初始反应的离子方程式为②
 第一步电离方程式
第一步电离方程式 ,其电离常数为
,其电离常数为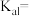
(2)①
 磁性纳米盘制备:在一定条件,将
磁性纳米盘制备:在一定条件,将 的
的 和PVP溶于水中并加热,滴加过量NaOH溶液生成
和PVP溶于水中并加热,滴加过量NaOH溶液生成 ,再加入amL
,再加入amL 的
的 溶液。充分反应后(
溶液。充分反应后(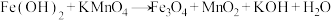 ,未配平),可制得
,未配平),可制得 磁性纳米盘。制备过程中需严格控制
磁性纳米盘。制备过程中需严格控制 溶液的用量,则a=
溶液的用量,则a=②
 磁性纳米盘对酸性水中三价砷的去除能力远比五价砷的弱,可利用其中的
磁性纳米盘对酸性水中三价砷的去除能力远比五价砷的弱,可利用其中的 将酸性废水中的
将酸性废水中的 氧化成
氧化成 除去,反应过程中生成
除去,反应过程中生成 ,则反应的离子方程式为
,则反应的离子方程式为③
 磁性纳米盘处理含砷废水时,水中
磁性纳米盘处理含砷废水时,水中 、
、 、
、 和
和 对
对 的吸附率的影响如图2。
的吸附率的影响如图2。 对
对 吸附去除几乎没有影响,
吸附去除几乎没有影响, 对
对 吸附去除影响较大。请解释
吸附去除影响较大。请解释 抑制
抑制 吸附去除的可能原因
吸附去除的可能原因
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2和HI能发生如下反应:______ NaNO2+_______ HI→_________ NO↑+_____ I2+_________ NaI +_____
(1)请将生成物补充完整并配平,并用单线桥法标出电子转移的方向和数目。___________
(2)上述反应中氧化剂与还原剂的物质的量之比为_________ ,若标准状况下生成3.36L NO,则反应中转移电子的数目是______________ 。
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤食醋,进行实验选用物质合适的是______ (填字母编号)。
A.①③⑤B.①②④C.①②⑤D.②④⑤
(4)某工厂废液中,含有2%—5%的NaNO2,直接排放会造成污染,采用NH4Cl能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为_______________ 。
(5)把氯气通到NaNO2溶液中,生成NaNO3和HCl,写出反应的离子方程式:______ 。
(6)亚硝酸盐可将正常的携氧亚铁血红蛋白转化成三价铁血红蛋白,失去携氧能力,引起组织缺氧导致中毒。美蓝是亚硝酸盐中毒的有效解毒剂。下列说法中不正确的是_______ 。
A.在中毒过程中携氧亚铁血红蛋白被氧化B.中毒时亚硝酸盐发生氧化反应
C.药品美蓝应具有还原性D.解毒时三价铁血红蛋白被还原
(1)请将生成物补充完整并配平,并用单线桥法标出电子转移的方向和数目。
(2)上述反应中氧化剂与还原剂的物质的量之比为
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤食醋,进行实验选用物质合适的是
A.①③⑤B.①②④C.①②⑤D.②④⑤
(4)某工厂废液中,含有2%—5%的NaNO2,直接排放会造成污染,采用NH4Cl能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为
(5)把氯气通到NaNO2溶液中,生成NaNO3和HCl,写出反应的离子方程式:
(6)亚硝酸盐可将正常的携氧亚铁血红蛋白转化成三价铁血红蛋白,失去携氧能力,引起组织缺氧导致中毒。美蓝是亚硝酸盐中毒的有效解毒剂。下列说法中不正确的是
A.在中毒过程中携氧亚铁血红蛋白被氧化B.中毒时亚硝酸盐发生氧化反应
C.药品美蓝应具有还原性D.解毒时三价铁血红蛋白被还原
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】(1)已知用金属钠制取氧化钠,可有多种方法:
①4Na+O2===2Na2O
②4Na+CO2===2Na2O+C
③2NaNO2+6Na===4Na2O+N2↑
在上述三种方法中最好的是_______ ,原因是______________________________________ 。该反应中作氧化剂的是________ 。
(2)据资料介绍:过氧化钠是钠在空气中燃烧的主要产物,由于空气中还含有其他成分,因此还存在其他产物,如氮化钠。已知氮化钠与水反应能生成氢氧化钠和氨气,则氮化钠与水反应的化学方程式为____________________________ 。
①4Na+O2===2Na2O
②4Na+CO2===2Na2O+C
③2NaNO2+6Na===4Na2O+N2↑
在上述三种方法中最好的是
(2)据资料介绍:过氧化钠是钠在空气中燃烧的主要产物,由于空气中还含有其他成分,因此还存在其他产物,如氮化钠。已知氮化钠与水反应能生成氢氧化钠和氨气,则氮化钠与水反应的化学方程式为
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】(1)黑火药是我国古代的四大发明之一。黑火药着火时,主要发生化学反应, 2KNO3+S+3C=K2S+N2↑+3CO2↑.在上述反应中,被还原的元素为_________ (填元素符号)。
(2)在Fe+ 4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,则56g Fe参加反应时,被还原的HNO3为___ g。
(3)某容器中发生一个化学反应,反应过程中存在Fe2+、NO 、Fe3+、NH
、Fe3+、NH 、H+和H2O六种粒子,在反应过程中测得Fe3+、NO
、H+和H2O六种粒子,在反应过程中测得Fe3+、NO 的数目随时间变化的曲线如图所示
的数目随时间变化的曲线如图所示
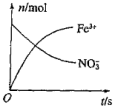
写出此离子反应方程式____________ 。
(4)某反应体系中有6种物质: NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O,其中Au2O是生成物之一。写出此化学反应方程式__________________ 。
(5)汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多2. 8mol,则转移电子的物质的量为_________ 。
(6)Cu2S与定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的个数之比为2:1时,实际参加反应的Cu2S与HNO3的个数之比为________ 。
(7)一定量的某磁黄铁矿(主要成分FeXS,S为-2价)与100mL 盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成2.4g硫单质、0.425 mol FeCl2和一定量H2S气体,且溶液中无Fe3+,该磁黄铁矿中FexS的x=_____ 。
(2)在Fe+ 4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,则56g Fe参加反应时,被还原的HNO3为
(3)某容器中发生一个化学反应,反应过程中存在Fe2+、NO
 、Fe3+、NH
、Fe3+、NH 、H+和H2O六种粒子,在反应过程中测得Fe3+、NO
、H+和H2O六种粒子,在反应过程中测得Fe3+、NO 的数目随时间变化的曲线如图所示
的数目随时间变化的曲线如图所示
写出此离子反应方程式
(4)某反应体系中有6种物质: NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O,其中Au2O是生成物之一。写出此化学反应方程式
(5)汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多2. 8mol,则转移电子的物质的量为
(6)Cu2S与定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的个数之比为2:1时,实际参加反应的Cu2S与HNO3的个数之比为
(7)一定量的某磁黄铁矿(主要成分FeXS,S为-2价)与100mL 盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成2.4g硫单质、0.425 mol FeCl2和一定量H2S气体,且溶液中无Fe3+,该磁黄铁矿中FexS的x=
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】向含有Fe2+、I-、Br- (已知还原性 >Fe2+>Br-)的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
>Fe2+>Br-)的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
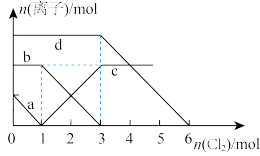
(1)图中线a、b、c、d依次代表___________ 、___________ 、___________ 、___________ 离子的物质的量变化情况(填写离子符号)。
(2)当通入2mol 时,溶液中发生反应的离子方程式是:
时,溶液中发生反应的离子方程式是:___________ 。
(3)原溶液中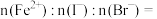
___________ 。
(4)在通入氯气的总反应中,下列离子方程式中不可能的发生的是___________
 >Fe2+>Br-)的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
>Fe2+>Br-)的溶液中缓慢通入氯气,溶液中各种离子的物质的量变化如图所示。
(1)图中线a、b、c、d依次代表
(2)当通入2mol
 时,溶液中发生反应的离子方程式是:
时,溶液中发生反应的离子方程式是:(3)原溶液中
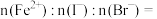
(4)在通入氯气的总反应中,下列离子方程式中不可能的发生的是___________
A. |
B. |
C.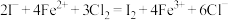 |
D. |
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】已知Ca(OH)2与Cl2反应的氧化物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应),生成物中含有Cl-、ClO-、 三种含氧元素的离子,其中ClO-、
三种含氧元素的离子,其中ClO-、 两种离子的物质的量(n)与反应时间(t)的曲线
两种离子的物质的量(n)与反应时间(t)的曲线
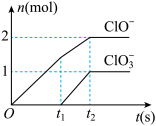
(1)t1前,氧化产物是_____________ (填化学式)。
(2)t2时,石灰乳与Cl2发生反应的总的离子方程式为:_______________ 。
(3)该反应中所消耗氯气的物质的量是______ mol。
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是__________(填字母)。
(5)配平下列离子方程式:Fe(OH)3+ClO-+OH-= +Cl-+H2O
+Cl-+H2O___________ 。
 三种含氧元素的离子,其中ClO-、
三种含氧元素的离子,其中ClO-、 两种离子的物质的量(n)与反应时间(t)的曲线
两种离子的物质的量(n)与反应时间(t)的曲线
(1)t1前,氧化产物是
(2)t2时,石灰乳与Cl2发生反应的总的离子方程式为:
(3)该反应中所消耗氯气的物质的量是
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是__________(填字母)。
| A.NaCl、Cl2 | B.NaCl、NaClO | C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
 +Cl-+H2O
+Cl-+H2O
您最近半年使用:0次



