某班同学通过实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是___________ 。
(2)甲组同学取 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为___________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红。煤油的作用是
溶液,溶液变红。煤油的作用是___________ 。
(4)丙组同学取 溶液,加入
溶液,加入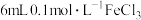 溶液混合。分别取
溶液混合。分别取 此溶液于3支试管中进行如下实验:
此溶液于3支试管中进行如下实验:
①第一支试管中加入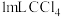 充分振荡、静置,
充分振荡、静置, 层显紫色;
层显紫色;
②第二支试管中加入1滴 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;
③第三支试管中加入1滴 溶液,溶液变红。
溶液,溶液变红。
实验②检验的离子是___________ (填离子符号);实验①和③说明:在 过量的情况下,溶液中仍含有
过量的情况下,溶液中仍含有___________ (填离子符号),由此可以证明该氧化还原反应为___________ 。
(5)丁组同学向盛有 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为___________ ;如果向 溶液中滴加
溶液中滴加 溶液,现象是
溶液,现象是___________ ;沉淀变色的原因是___________ (用化学方程式解释)。
 、
、 的性质。回答下列问题:
的性质。回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成
 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是(2)甲组同学取
 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为(3)乙组同学认为甲组的实验不够严谨,该组同学在
 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红。煤油的作用是
溶液,溶液变红。煤油的作用是(4)丙组同学取
 溶液,加入
溶液,加入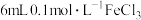 溶液混合。分别取
溶液混合。分别取 此溶液于3支试管中进行如下实验:
此溶液于3支试管中进行如下实验:①第一支试管中加入
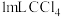 充分振荡、静置,
充分振荡、静置, 层显紫色;
层显紫色;②第二支试管中加入1滴
 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;③第三支试管中加入1滴
 溶液,溶液变红。
溶液,溶液变红。实验②检验的离子是
 过量的情况下,溶液中仍含有
过量的情况下,溶液中仍含有(5)丁组同学向盛有
 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为 溶液中滴加
溶液中滴加 溶液,现象是
溶液,现象是
更新时间:2021-09-09 19:37:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有下列八种物质:①铝②蔗糖③SiO2④H2SO4⑤NaOH⑥FeSO4溶液⑦Ba(OH)2⑧氢氧化铁胶体
(1)上述物质属于电解质的有_________ 。(填序号)
(2)向⑥中加入少量⑤的溶液,观察的现象为___________ 。
(3)上述物质中有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为_____ 。
(4)若在⑧中缓慢加入⑤,产生的现象是___________ 。
(5)③和⑤是玻璃的主要成分之一,③与⑥溶液反应的化学方程式为________ ,工艺师常用______ (填物质名称)来雕刻玻璃。
(1)上述物质属于电解质的有
(2)向⑥中加入少量⑤的溶液,观察的现象为
(3)上述物质中有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为
(4)若在⑧中缓慢加入⑤,产生的现象是
(5)③和⑤是玻璃的主要成分之一,③与⑥溶液反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)通常用小苏打的溶液除去CO2中的HCl,反应的离子方程式为:_______________ ,
不能用NaOH溶液的原因是__________ (用离子方程式表示),也不能用NaCO3的原因是__________ (用离子方程式表示)
(2)Fe(OH)2很不稳定,露置在空气中容易被氧化,发生反应的化学方程式为______________
Fe(OH)2可以用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应来制备:
①用硫酸亚铁晶体配制上述FeSO4溶液时还需加入_______ 来防止Fe2+被氧化.
②生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液.这样操作的理由是___________________ .
不能用NaOH溶液的原因是
(2)Fe(OH)2很不稳定,露置在空气中容易被氧化,发生反应的化学方程式为
Fe(OH)2可以用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应来制备:
①用硫酸亚铁晶体配制上述FeSO4溶液时还需加入
②生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液.这样操作的理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮元素的单质和化合物在生活生产中有广泛用途。
(1)氮分子中化学键名称是_______ ;氮分子的电子式为:_______ ;已知 分子与
分子与 分子结构相似,
分子结构相似, 熔点高于
熔点高于 ,其原因是(从化学键和晶体的角度用文字表述原因)
,其原因是(从化学键和晶体的角度用文字表述原因)_______ 。
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
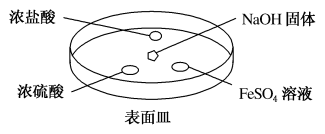
浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_______ ;浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,其中所含的正盐作为一种化肥俗称:_______ ,长期施用容易造成土壤酸化板结; 液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是
液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是_______ 和_______ 。
(3)将氨通入水中溶液呈碱性的原因(用方程式表示)_______ 。
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),写出反应的化学方程式并用单线桥标出电子转移方向和数目_______ ,该反应中被氧化的元素是_______ ,还原产物是_______ 。若反应中有3mol电子发生转移,参与反应的氨的质量为_______ g。
(1)氮分子中化学键名称是
 分子与
分子与 分子结构相似,
分子结构相似, 熔点高于
熔点高于 ,其原因是(从化学键和晶体的角度用文字表述原因)
,其原因是(从化学键和晶体的角度用文字表述原因)(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
 液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是
液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是(3)将氨通入水中溶液呈碱性的原因(用方程式表示)
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),写出反应的化学方程式并用单线桥标出电子转移方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请回答下列问题。
(1)水体中的 、
、 和
和 是高毒性的重金属离子,可用Cr(VI)表示。常用的处理方法是将Cr(VI)还原为低毒性的Cr3+或Cr(OH)3。在一定pH的水溶液中,HS-、S2-可与
是高毒性的重金属离子,可用Cr(VI)表示。常用的处理方法是将Cr(VI)还原为低毒性的Cr3+或Cr(OH)3。在一定pH的水溶液中,HS-、S2-可与 反应生成Cr(OH)3和单质硫。水溶液中S2-能与单质硫反应生成Sn2-,Sn2-能还原Cr(VI)。
反应生成Cr(OH)3和单质硫。水溶液中S2-能与单质硫反应生成Sn2-,Sn2-能还原Cr(VI)。
①在pH=9的水溶液中 与HS-反应的离子方程式为
与HS-反应的离子方程式为____ 。
②25℃时用过量S2-还原Cr(VI),发现反应后期Cr(VI)被还原的速率反而加快。产生该现象的原因可能是____ ;验证的实验方法是____ 。
(2)低浓度含砷As废水去除原理为:Fe3++ =FeAsO3↓,Fe3++
=FeAsO3↓,Fe3++ =FeAsO4↓。Na2S2O8易溶于水、有氧化性,利用Fe—Na2S2O8体系去除废水中的五价砷,反应机理如图所示。
=FeAsO4↓。Na2S2O8易溶于水、有氧化性,利用Fe—Na2S2O8体系去除废水中的五价砷,反应机理如图所示。
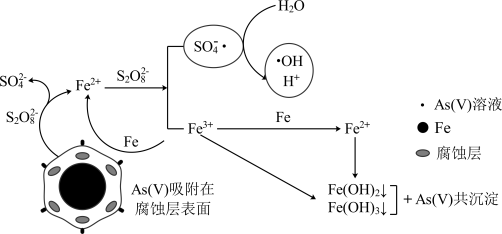
写出•OH的电子式____ 。 在此过程中的作用与发生的变化可描述为
在此过程中的作用与发生的变化可描述为____ 。
(1)水体中的
 、
、 和
和 是高毒性的重金属离子,可用Cr(VI)表示。常用的处理方法是将Cr(VI)还原为低毒性的Cr3+或Cr(OH)3。在一定pH的水溶液中,HS-、S2-可与
是高毒性的重金属离子,可用Cr(VI)表示。常用的处理方法是将Cr(VI)还原为低毒性的Cr3+或Cr(OH)3。在一定pH的水溶液中,HS-、S2-可与 反应生成Cr(OH)3和单质硫。水溶液中S2-能与单质硫反应生成Sn2-,Sn2-能还原Cr(VI)。
反应生成Cr(OH)3和单质硫。水溶液中S2-能与单质硫反应生成Sn2-,Sn2-能还原Cr(VI)。①在pH=9的水溶液中
 与HS-反应的离子方程式为
与HS-反应的离子方程式为②25℃时用过量S2-还原Cr(VI),发现反应后期Cr(VI)被还原的速率反而加快。产生该现象的原因可能是
(2)低浓度含砷As废水去除原理为:Fe3++
 =FeAsO3↓,Fe3++
=FeAsO3↓,Fe3++ =FeAsO4↓。Na2S2O8易溶于水、有氧化性,利用Fe—Na2S2O8体系去除废水中的五价砷,反应机理如图所示。
=FeAsO4↓。Na2S2O8易溶于水、有氧化性,利用Fe—Na2S2O8体系去除废水中的五价砷,反应机理如图所示。
写出•OH的电子式
 在此过程中的作用与发生的变化可描述为
在此过程中的作用与发生的变化可描述为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】苹果汁中含有Fe2+,它是人们喜欢的一种补铁饮料,现榨的苹果汁在空气中会由浅绿色Fe2+逐渐变为棕黄色Fe3+。若榨汁时加入维生素C,可以防止这种现象发生。

(1)问题一:现榨苹果汁在空气中为什么会由浅绿色变为棕黄色?_______
(2)问题二:若榨汁时加入维生素C,可防止苹果汁变色,说明维生素C具有什么性质?_______

(1)问题一:现榨苹果汁在空气中为什么会由浅绿色变为棕黄色?
(2)问题二:若榨汁时加入维生素C,可防止苹果汁变色,说明维生素C具有什么性质?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示:
Ⅰ.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是______ nm。
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:___________ 。检验反应后溶液中还存在Fe3+的试剂是__________ 。
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是______ 。
Ⅱ.现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(4)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是______ ,加铁粉后溶液增重的是 _____________ (填写离子符号)
(5)向Fe2+的溶液中滴加NaOH溶液,现象是___________________ 。
(6)欲除去FeCl2中FeCl3选用的试剂是________ ,并写出相应离子方程式:__________ 。
Ⅰ.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是
Ⅱ.现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(4)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是
(5)向Fe2+的溶液中滴加NaOH溶液,现象是
(6)欲除去FeCl2中FeCl3选用的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箱,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的化学方程式:___ 。
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,向废液中先加入过量铁粉,过滤后再向溶液中通入___ (化学式),请写出相关反应的离子方程式___ 、___ 、______ 。
(1)写出FeCl3溶液与金属铜发生反应的化学方程式:
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,向废液中先加入过量铁粉,过滤后再向溶液中通入
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】健康人体内含铁元素大约2~3g,人体内铁元素以亚铁离子和三价铁离子的形式存在,Fe2+易被吸收,所以给贫血者补充铁元素时,应补充含Fe2+的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:

(1)试剂1的名称是__ ,试剂2的名称是__ 。
(2)加入新制氯水,溶液中发生反应的离子方程式是__ 。
(3)加入试剂2时溶液为淡红色说明“速力菲”中的Fe2+已部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有__ 性。
(4)不仅溶液中Fe2+易被氧化成Fe3+,溶液中白色沉淀Fe(OH)2更易被O2氧化,请写出反应的化学方程式___ ,现象为__ 。

(1)试剂1的名称是
(2)加入新制氯水,溶液中发生反应的离子方程式是
(3)加入试剂2时溶液为淡红色说明“速力菲”中的Fe2+已部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
(4)不仅溶液中Fe2+易被氧化成Fe3+,溶液中白色沉淀Fe(OH)2更易被O2氧化,请写出反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】①在酸性条件下,向含铬废水中加入FeSO4,可将 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为__________________________
②在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为___________________________ 。
③在碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,离子方程式是_______________ 。
④对比②和③实验所得的结果,将I2、ClO-、 按氧化性由强到弱的顺序排列为
按氧化性由强到弱的顺序排列为___________ 。
 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为②在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为
③在碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,离子方程式是
④对比②和③实验所得的结果,将I2、ClO-、
 按氧化性由强到弱的顺序排列为
按氧化性由强到弱的顺序排列为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中属于盐类的是___________ (填序号,下同);相互间能发生反应的是___________ 。
(2)食盐不慎洒落在天然气的火焰上,观察的现象是___________ 。
(3)FeSO4•7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式简述其原因___________ 。
(4)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式___________ ,若生成6.72L气体(标准状况),则消耗铝的质量为___________ g。
(2)食盐不慎洒落在天然气的火焰上,观察的现象是
(3)FeSO4•7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式简述其原因
(4)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求完成下列各题:
(1)实验室保存FeCl2溶液时,为防止被氧化,需加入___________ 。
(2)消毒液(含NaClO)与洁厕剂(含HCl)不能混用,否则会生成有毒的Cl2,请写出反应的离子方程式___________ 。
(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,请写出反应的化学方程式___________ 。
(4)用双线桥法表示该反应电子转移的方向和数目: 2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑___________ 。
(5)依据化合价升降守恒配平化学方程式:__________
K2Cr2O7+HCl=KCl+CrCl3+Cl2↑+H2O
(1)实验室保存FeCl2溶液时,为防止被氧化,需加入
(2)消毒液(含NaClO)与洁厕剂(含HCl)不能混用,否则会生成有毒的Cl2,请写出反应的离子方程式
(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,请写出反应的化学方程式
(4)用双线桥法表示该反应电子转移的方向和数目:
 2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑(5)依据化合价升降守恒配平化学方程式:
K2Cr2O7+HCl=KCl+CrCl3+Cl2↑+H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】为了达到下列的实验要求,请从供选择的化学试剂或实验方法中选出合适的,将其编号填入对应的空格中,并按要求写出相应的方程式。
供选择的化学试剂或实验方法如下:
A.加入NaOH溶液,过滤、洗涤、干燥 B.通入适量的CO2
C.通入Cl2气体 D.加入适量铁粉
E.加入CaCl2溶液,观察 F.加入澄清石灰水,观察
G.丁达尔效应
(1)鉴别Fe(OH)3胶体和FeCl3溶液:________
(2)除去镁粉中的少量铝粉杂质:_______
(3)除去FeCl3溶液中FeCl2:_____ , 离子方程式____________________
(4)实验室保存FeSO4溶液时要加入____ ;
(5)除去NaHCO3溶液中的少量Na2CO3杂质:________ , 化学方程式:___________________
供选择的化学试剂或实验方法如下:
A.加入NaOH溶液,过滤、洗涤、干燥 B.通入适量的CO2
C.通入Cl2气体 D.加入适量铁粉
E.加入CaCl2溶液,观察 F.加入澄清石灰水,观察
G.丁达尔效应
(1)鉴别Fe(OH)3胶体和FeCl3溶液:
(2)除去镁粉中的少量铝粉杂质:
(3)除去FeCl3溶液中FeCl2:
(4)实验室保存FeSO4溶液时要加入
(5)除去NaHCO3溶液中的少量Na2CO3杂质:
您最近一年使用:0次



