下表是元素周期表的一部分:
(1)最高价氧化物对应的水化物中,碱性最强的是_______ ,酸性最强的是_______ 。
(2)f、g和h的气态氢化物的稳定性由强到弱的顺序是_______ 。
(3)研究发现,在元素周期表中左上方与右下方相邻元素也存在某些性质的相似性,这一规律通常称对角线规则或对角线相似,则与c呈对角线相似的元素是铍,元素符号是“Be”,如:Be与Al一样,也能与NaOH溶液反应,反应的化学方程式是:Be+2NaOH→Na2BeO2+H2↑。请根据以上信息,结合已学知识,尝试写出Be的最高价氧化物对应水化物与NaOH溶液反应的离子方程式:_______ 。
| 周期/族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | a | |||||||
| 2 | d | e | h | |||||
| 3 | b | c | f | g |
(1)最高价氧化物对应的水化物中,碱性最强的是
(2)f、g和h的气态氢化物的稳定性由强到弱的顺序是
(3)研究发现,在元素周期表中左上方与右下方相邻元素也存在某些性质的相似性,这一规律通常称对角线规则或对角线相似,则与c呈对角线相似的元素是铍,元素符号是“Be”,如:Be与Al一样,也能与NaOH溶液反应,反应的化学方程式是:Be+2NaOH→Na2BeO2+H2↑。请根据以上信息,结合已学知识,尝试写出Be的最高价氧化物对应水化物与NaOH溶液反应的离子方程式:
20-21高二上·上海·课时练习 查看更多[2]
(已下线)9.1 元素周期律-2020-2021学年秋季班高二上学期化学教材知识点精讲练(沪科版)(已下线)5.1.2 元素周期表 元素周期表的应用-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)
更新时间:2021-09-09 11:12:39
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)①写出52号元素在元素周期表中的位置___ 。
②用电子式表示MgCl2的形成过程___ 。
(2)现在需配制0.1mol/L的Na2CO3溶液480mL,需要用托盘天平称量Na2CO3固体__ g。
(3)写出碳酸钠溶液和过量盐酸反应的离子方程式___ 。
②用电子式表示MgCl2的形成过程
(2)现在需配制0.1mol/L的Na2CO3溶液480mL,需要用托盘天平称量Na2CO3固体
(3)写出碳酸钠溶液和过量盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语作答:
(1)④、⑤、⑦的原子半径由大到小的顺序为____________ 。
(2)⑥和⑦的最高价含氧酸的酸性强弱为_________________ 。
(3)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
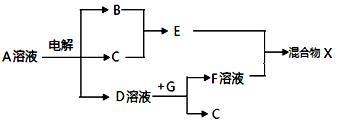
①写出电解A溶液的化学方程式______________________________________ 。
②若上图中各步反应均为完全转化,则混合物X中含有的物质有____________ 。
(4)砷(As)的化合物可用于杀虫及医疗。
①As的原子结构示意图为___________ ,②其氢化物的化学式为____________ 。
③Y由②⑤⑦三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为___________________ 。
I A | 0 | ||||||
① | II A | III A | IV A | V A | VI A | VII A | |
② | ④ | ||||||
⑤ | ③ | ⑧ | ⑥ | ⑦ |
(1)④、⑤、⑦的原子半径由大到小的顺序为
(2)⑥和⑦的最高价含氧酸的酸性强弱为
(3)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。

①写出电解A溶液的化学方程式
②若上图中各步反应均为完全转化,则混合物X中含有的物质有
(4)砷(As)的化合物可用于杀虫及医疗。
①As的原子结构示意图为
③Y由②⑤⑦三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是周期表中的一部分,根据①--⑩在周期表中的位置,用元素符号 或化学式 回答下列问题:
(1)表中元素,化学性质最不活泼的是______ ,还原性最强的单质是______ ,可用于制半导体材料的元素是______ ;
(2)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是______ ;
(3)比较⑥、⑦、⑨的氢化物的稳定性最弱的是______ ;
(4)铍 位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加
位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加______ (填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式__________ 。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ④ | ⑦ | ⑧ | ⑩ | ||||
| 3 | ② | ③ | ⑤ | ⑥ | ⑨ |
(1)表中元素,化学性质最不活泼的是
(2)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是
(3)比较⑥、⑦、⑨的氢化物的稳定性最弱的是
(4)铍
 位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加
位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】晶体硅是良好的半导体材料,多晶硅主要采用SiHCl3还原工艺生产。
(1)硅原子核外有_____ 种能量不同的电子。氯离子的核外电子排布式为________________________ 。短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是________ 。
(2)从原子结构角度解释硅元素与氯元素的非金属性强弱________________________ 。
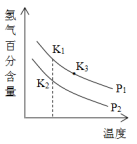
(3)900℃以上发生SiHCl3(g)+H2(g) Si(s)+3HCl(g)反应,平衡时H2的百分含量随温度、压强(P)变化如图(K为不同条件时得平衡常数)。从化学反应速率角度来说明上述反应已达到平衡状态
Si(s)+3HCl(g)反应,平衡时H2的百分含量随温度、压强(P)变化如图(K为不同条件时得平衡常数)。从化学反应速率角度来说明上述反应已达到平衡状态_______ 。
(4)若反应容器的容积为2L,10min后达到平衡,测得固体的质量增加了2.8g,则HCl的平均反应速率为______________ 。
(5)P1____ P2(选填“>”、“<”或“=”);K1、K2、K3大小关系式为___________ 。
(1)硅原子核外有
(2)从原子结构角度解释硅元素与氯元素的非金属性强弱

(3)900℃以上发生SiHCl3(g)+H2(g)
 Si(s)+3HCl(g)反应,平衡时H2的百分含量随温度、压强(P)变化如图(K为不同条件时得平衡常数)。从化学反应速率角度来说明上述反应已达到平衡状态
Si(s)+3HCl(g)反应,平衡时H2的百分含量随温度、压强(P)变化如图(K为不同条件时得平衡常数)。从化学反应速率角度来说明上述反应已达到平衡状态(4)若反应容器的容积为2L,10min后达到平衡,测得固体的质量增加了2.8g,则HCl的平均反应速率为
(5)P1
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,请回答下列问题:
(1)写出下列元素符号:⑤________ ,⑥________ 。
(2)在这些元素中(表中①~⑧),最活泼的金属元素是__________ (填元素符号,下同),最活泼的非金属元素是______ ,最不活泼的元素是________ 。
(3)在第三周期的元素中,最高价氧化物对应水化物酸性最强的是________ (填化学式),碱性最强的是________ (填化学式),原子半径最小的是________ (填元素符号)。
(4)在③与④中,化学性质较活泼的是________ (填元素符号),怎样用化学实验证明?
(简述方法即可)___________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
(1)写出下列元素符号:⑤
(2)在这些元素中(表中①~⑧),最活泼的金属元素是
(3)在第三周期的元素中,最高价氧化物对应水化物酸性最强的是
(4)在③与④中,化学性质较活泼的是
(简述方法即可)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】甲烷的氯化反应式为: CH4+Cl2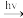 CH3Cl+HCl。对于该反应机理(反应过程)的详细描述如下:
CH3Cl+HCl。对于该反应机理(反应过程)的详细描述如下:
链引发Cl2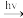 2Cl·
2Cl·
链增长CH4+Cl· ·CH3+HCl △H=+7.5 kJ/mol
·CH3+HCl △H=+7.5 kJ/mol
CH3+Cl2 CH3Cl + Cl· △H=-112.9 kJ/mol
CH3Cl + Cl· △H=-112.9 kJ/mol
链终止·Cl+Cl· Cl2
Cl2
CH3+·CH3 H3CCH3
H3CCH3
CH3+Cl· H3CCl
H3CCl
(1)在链增长的第二步反应中形成的化合物的电子式为_______ ;在反应机理的三个阶段破坏或形成的化学键类型均为_________ 。
(2)在短周期主族元素中,氯元素与其相邻元素的原子半径由大到小的顺序为_________ (用元素符号表示);与氯元素同周期且金属性最强的元素位于周期表的第_____ 周期,第____ 族。
(3)链引发的反应为_______ 反应(选填“吸热”或“放热”,下同),链终止的反应为_______ 反应。
(4)卤素单质及化合物在许多性质上都存在着递变规律,下列递变顺序正确的是_______ 。(选填字母编号)
a.相同条件下卤化银的溶解度按AgCl、AgBr、AgI 的顺序依次增大
b.卤化氢溶入水的酸性按HF、HCl、HBr、HI的顺序依次减弱
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质氧化性按F2、Cl2、Br2、I2的顺序依次减弱
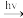 CH3Cl+HCl。对于该反应机理(反应过程)的详细描述如下:
CH3Cl+HCl。对于该反应机理(反应过程)的详细描述如下:链引发Cl2
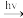 2Cl·
2Cl·链增长CH4+Cl·
 ·CH3+HCl △H=+7.5 kJ/mol
·CH3+HCl △H=+7.5 kJ/molCH3+Cl2
 CH3Cl + Cl· △H=-112.9 kJ/mol
CH3Cl + Cl· △H=-112.9 kJ/mol链终止·Cl+Cl·
 Cl2
Cl2CH3+·CH3
 H3CCH3
H3CCH3CH3+Cl·
 H3CCl
H3CCl(1)在链增长的第二步反应中形成的化合物的电子式为
(2)在短周期主族元素中,氯元素与其相邻元素的原子半径由大到小的顺序为
(3)链引发的反应为
(4)卤素单质及化合物在许多性质上都存在着递变规律,下列递变顺序正确的是
a.相同条件下卤化银的溶解度按AgCl、AgBr、AgI 的顺序依次增大
b.卤化氢溶入水的酸性按HF、HCl、HBr、HI的顺序依次减弱
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质氧化性按F2、Cl2、Br2、I2的顺序依次减弱
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。请回答下列问题:
(1)据汞的原子结构示意图 ,汞在第
,汞在第____ 周期。
(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是____ 。
(3)下列有关性质的比较能用元素周期律解释的是____ (填字母,下同)。
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是____ 。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为____ 。
②X的氢化物的电子式:____ 。
③写出Y的最高价氧化物的一种用途____ 。
(1)据汞的原子结构示意图
 ,汞在第
,汞在第(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是
(3)下列有关性质的比较能用元素周期律解释的是
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为
②X的氢化物的电子式:
③写出Y的最高价氧化物的一种用途
您最近一年使用:0次

 的原子核只有1个质子;元素Y、Z、W原子序数依次增大,且均位于
的原子核只有1个质子;元素Y、Z、W原子序数依次增大,且均位于 的原子比
的原子比 原子多8个电子。则X、Y、Z、W、E分别为
原子多8个电子。则X、Y、Z、W、E分别为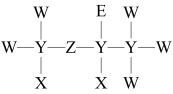
 族元素有F、Cl、Br、I、At。
族元素有F、Cl、Br、I、At。 的沸点依F、Cl、Br、I次序升高的原因是
的沸点依F、Cl、Br、I次序升高的原因是 )时,谱图中出现质荷比(相对分子质量)为64和
)时,谱图中出现质荷比(相对分子质量)为64和 的峰,请问出现
的峰,请问出现 中的化学键具有明显的共价性,蒸汽状态下以双聚分子
中的化学键具有明显的共价性,蒸汽状态下以双聚分子 存在的结构式为
存在的结构式为

