将40g铁粉放入600g稀硝酸中,若两者恰好完全反应,且稀硝酸被还原成NO,求:稀硝酸的质量分数___ 。
20-21高二上·全国·课时练习 查看更多[2]
更新时间:2021-09-10 20:28:12
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】(1)取300 mL 0.2 mol/L的 KI溶液与一定量的酸性 KMnO4 溶液恰好反应,生成等物质的量的 I2和 KIO3,则消耗 KMnO4的物质的量是________ mol。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是___________________ ,又变为棕黄色的原因是(用离子方程式解释)________________________________________________ 。
(3)在 100 mLFeBr2 溶液中通入标准状况下3.36 L Cl2,溶液中有 1/4的 Br-被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为________ mol/L。
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式__________________ 。向反应后的溶液中通入过量CO2,反应的离子方程式为__________________ 。
(5)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式_______________________________________ ,反应中生成0.2 mol HNO3,转移的电子数目为_______________________ 。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是_______ 。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
(3)在 100 mLFeBr2 溶液中通入标准状况下3.36 L Cl2,溶液中有 1/4的 Br-被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式
(5)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2,在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性。金属离子已完全沉淀,沉淀质量为39.2g。
(1)Cu和Cu2O的混合物中铜的物质的量为________ mol
(2)产生的NO在标准状况下的体积为______ L
(3)硝酸的物质的量浓度为_____________ mol/L
(4)Cu、Cu2O与硝酸反应后剩余HNO3为______ mol
(1)Cu和Cu2O的混合物中铜的物质的量为
(2)产生的NO在标准状况下的体积为
(3)硝酸的物质的量浓度为
(4)Cu、Cu2O与硝酸反应后剩余HNO3为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】有Fe和Fe2O3的混合物溶于500 mL的稀硝酸中,放出NO气体22.4 L(标准状况)并余5.44 g Fe,过滤,向滤液中通入20.16 L的Cl2(标准状况),恰好能使溶液中的Fe2+全部氧化。
求:(1)稀硝酸的物质的量浓度_______________________ ;
(2)原混合物中Fe的质量__________ ,氧化铁的物质的量_____________ 。
求:(1)稀硝酸的物质的量浓度
(2)原混合物中Fe的质量
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】取一定质量的Fe、Cu混合物的粉末平均分成四等份,分别向其中逐渐加入不同体积但同浓度的稀硝酸,实验中收集到的NO气体的体积及剩余固体的质量均记录在下表中(气体体积均在标准状况下测定)。
(1)写出实验①中化学反应的方程式_______________________________________
(2)计算稀硝酸的物质的量浓度是___________ ;
(3)每份混合物中含铁的质量是__________ 克、铜的质量是__________ 克;
(4)计算上表中实验③所用稀硝酸的体积和实验③、④产生气体的体积___________ 。
实验序号 | ① | ② | ③ | ④ |
稀硝酸体积 | 100mL | 200mL | 400mL | |
剩余固体质量 | 15.72g | 6.72g | 固体刚好全部溶解 | 0 |
气体体积 | 2.24L | 4.48L |
(1)写出实验①中化学反应的方程式
(2)计算稀硝酸的物质的量浓度是
(3)每份混合物中含铁的质量是
(4)计算上表中实验③所用稀硝酸的体积和实验③、④产生气体的体积
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】(1)在浓硝酸中放入铜片。
①开始反应的化学方程式为_____________________________________ 。
②若铜有剩余,则反应将要结束时的反应的离子方程式是_______________________ 。
③待反应停止后,再加入少量的25%的稀硫酸,这时铜片上又有气泡产生,其原因是____________ 。
(2)在100mL混合酸中,c(HNO3) = 0.4mol·L-1 ,c(H2SO4) = 0.2mol·L-1,向其中加入2.56g铜粉,微热,待充分反应后,溶液中Cu2+的物质的量浓度为______________ 。
(3)将8g Fe置于40ml硝酸中微热,生成气体的颜色由深变浅,充分反应后得到标况下1.792L的气体(假设只有NO和NO2两种成分),此时剩余2.4g固体,①反应中被还原和未被还原的硝酸的物质的量之比为___________ ,②NO和NO2体积之比为___________ 。
①开始反应的化学方程式为
②若铜有剩余,则反应将要结束时的反应的离子方程式是
③待反应停止后,再加入少量的25%的稀硫酸,这时铜片上又有气泡产生,其原因是
(2)在100mL混合酸中,c(HNO3) = 0.4mol·L-1 ,c(H2SO4) = 0.2mol·L-1,向其中加入2.56g铜粉,微热,待充分反应后,溶液中Cu2+的物质的量浓度为
(3)将8g Fe置于40ml硝酸中微热,生成气体的颜色由深变浅,充分反应后得到标况下1.792L的气体(假设只有NO和NO2两种成分),此时剩余2.4g固体,①反应中被还原和未被还原的硝酸的物质的量之比为
您最近一年使用:0次

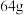 铜被一定浓度的硝酸完全溶解,产生的气体的体积为
铜被一定浓度的硝酸完全溶解,产生的气体的体积为 ,若将所得气体中混合
,若将所得气体中混合 ,则恰好能被水完全转化为硝酸;若将所得气体完全被氢氧化钠溶液吸收,会生成硝酸钠与亚硝酸钠(气体体积均在标准状况下测定),请回答:
,则恰好能被水完全转化为硝酸;若将所得气体完全被氢氧化钠溶液吸收,会生成硝酸钠与亚硝酸钠(气体体积均在标准状况下测定),请回答: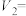
 。
。


