A与B反应生成C,假定反应由A、B开始,它们的起始浓度均为1mol/L。反应进行2min后A的浓度为0.8 mol/L,B的浓度为0.6 mol/L,C的浓度为0.6 mol/L.
(1)2min内反应的平均速率为:
v(A)=______________________ , v(B)=____________________
v (C )=__________________________
(2)三者数值之间的关系是:v (A) =_________ v (B) =_________ v(C)。
(3)该反应的化学方程式为:_________________________________
(1)2min内反应的平均速率为:
v(A)=
v (C )=
(2)三者数值之间的关系是:v (A) =
(3)该反应的化学方程式为:
12-13高二上·福建福州·期中 查看更多[3]
苏教2020版选择性必修1专题2第一单元 化学反应速率课后习题陕西省黄陵中学2019-2020学年高二上学期期中考试化学试题(已下线)2012-2013学年福建福清东张中学高二上学期期中考试理科化学试卷
更新时间:2019-01-30 18:14:09
|
相似题推荐
计算题
|
容易
(0.94)
名校
解题方法
【推荐1】在一体积固定的密闭容器中加入反应物A、B,发生如下反应:A+2B=3C。反应经2min后,A的浓度从开始时的1.0mol·L-1降到0.8mol·L-1。已知反应开始时B的浓度是1.2mol·L-1。
(1)2min末B、C的浓度____ 。
(2)用A表示该反应2min内的平均速率____ 。
(1)2min末B、C的浓度
(2)用A表示该反应2min内的平均速率
您最近一年使用:0次
计算题
|
容易
(0.94)
解题方法
【推荐2】某温度时在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。

(1)该反应的化学方程式为_____________ 。
(2)用Z的浓度变化表示0~2min间的平均反应速率v(Z)=_______________ 。
(3)反应达平衡时,容器内混合气体的总压强是起始时________ 倍。

(1)该反应的化学方程式为
(2)用Z的浓度变化表示0~2min间的平均反应速率v(Z)=
(3)反应达平衡时,容器内混合气体的总压强是起始时
您最近一年使用:0次
计算题
|
容易
(0.94)
解题方法
【推荐3】在100mL含有0.3mol氯化氢的盐酸溶液中放入5.6g铁粉,经过2min收集到干燥纯净的氢气1.12L(标准状况下)。在这2min内用盐酸表示的该反应速率为_______ ,用氯化亚铁表示的反应速率为_______ 。在此之后又经过4min,铁粉恰好完全溶解,在此之后4min内,用盐酸表示的平均反应速率为_______ 。从反应开始至铁粉完全溶解的6min内,用氯化亚铁表示的平均反应速率为_______ 。整个反应过程前2min内的平均反应速率比后4min内平均反应速率快的原因是_______ 。
您最近一年使用:0次
计算题
|
容易
(0.94)
解题方法
【推荐1】在容积为2L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率
3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率 (D)为0.2mol/(L·min)。
(D)为0.2mol/(L·min)。
计算:(1)5min末A的物质的量浓度为___ ;
(2)前5min内用B表示的化学反应速率 (B)为
(B)为___ ;
(3)化学方程式中n值为___ 。
 3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率
3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,用D表示的化学反应速率 (D)为0.2mol/(L·min)。
(D)为0.2mol/(L·min)。计算:(1)5min末A的物质的量浓度为
(2)前5min内用B表示的化学反应速率
 (B)为
(B)为(3)化学方程式中n值为
您最近一年使用:0次
计算题
|
容易
(0.94)
解题方法
【推荐2】在容积为1.00L的密闭容器中,通入一定量的N2O4,发生反应:N2O4(g) 2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
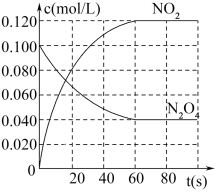
请回答:
(1)60s内,v(N2O4)=___ mol/(L•s)。
(2)若升高温度,混合气体的颜色变深,则正反应是___ (填“放热”或吸热”)反应。
(3)100℃时,该反应的化学平衡常数数值为___ 。
(4)平衡时,N2O4的转化率是___ 。
 2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
2NO2(g)。100℃时,各物质浓度随时间变化如图所示。
请回答:
(1)60s内,v(N2O4)=
(2)若升高温度,混合气体的颜色变深,则正反应是
(3)100℃时,该反应的化学平衡常数数值为
(4)平衡时,N2O4的转化率是
您最近一年使用:0次
计算题
|
容易
(0.94)
名校
【推荐1】在2L的容器中放入4mol N2O5,发生如下反应:2N2O5(g) 4NO2(g)+O2(g)。反应进行到5min时,测得N2O5转化了20%,
4NO2(g)+O2(g)。反应进行到5min时,测得N2O5转化了20%,
(1)5min时,剩余N2O5的物质的量_____ ;
(2)前5min,v(NO2)为多少_________ ;
(3)5min时,N2O5的物质的量占混合气体总物质的量的百分比(保留一位小数)________ 。
 4NO2(g)+O2(g)。反应进行到5min时,测得N2O5转化了20%,
4NO2(g)+O2(g)。反应进行到5min时,测得N2O5转化了20%,(1)5min时,剩余N2O5的物质的量
(2)前5min,v(NO2)为多少
(3)5min时,N2O5的物质的量占混合气体总物质的量的百分比(保留一位小数)
您最近一年使用:0次
计算题
|
容易
(0.94)
【推荐2】在2L的密闭容器中,充入1molSO2和1molO2,在一定条件下发生反应:2SO2+O2⇌2SO3,当反应进行了10s时,测得SO3的物质的量为0.6mol,求:
(1)用SO2表示该化学反应速率为多少?_______
(2)若改用O2表示化学反应速率又为多少?_________
(3)若要提高反应速率你认为可采取的合理措施有哪些?________
(1)用SO2表示该化学反应速率为多少?
(2)若改用O2表示化学反应速率又为多少?
(3)若要提高反应速率你认为可采取的合理措施有哪些?
您最近一年使用:0次



