钙及其化合物间有如下相互转化关系,请按要求写出指定反应的化学方程式并完成填空。

(1)反应②___________
(2)反应⑤___________
(3)反应⑥___________
(4)在反应①~⑥中,属于化合反应的是___________ (填序号,下同),属于氧化还原反应的是___________

(1)反应②
(2)反应⑤
(3)反应⑥
(4)在反应①~⑥中,属于化合反应的是
更新时间:2021-09-24 16:44:00
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】84消毒液是一种常见的含氯消毒剂,广泛用于家庭、医院的消毒。某学习小组对84消毒液的性质进行探究

查阅资料:①84消毒液的主要成分是 ,还含有少量的
,还含有少量的
②单质碘 (I2)遇淀粉变蓝。
预测性质:
(1)从物质类别看, 属于
属于_______ , 属于
属于_______ (填“强”或“弱”)酸, 可能与某些酸反应。
可能与某些酸反应。
(2)84消毒液具有氧化性,预测的依据是_______ 。
(3)实验验证:
(4)该学习小组同学对实验ⅲ进行了如下改进:
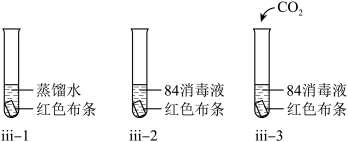
观察到ⅲ—1试管中无明显现象,ⅱ—2、ⅲ—3中红色布条均褪色,ⅲ—3中红色布条褪色更明显。
①对比ⅲ—1、ⅰ—2的现象,可得到的结论是_______ 。
②对比ⅰ—2、ⅲ—3的现象,产生该现象差异的原因是_______ 。

查阅资料:①84消毒液的主要成分是
 ,还含有少量的
,还含有少量的
②单质碘 (I2)遇淀粉变蓝。
预测性质:
(1)从物质类别看,
 属于
属于 属于
属于 可能与某些酸反应。
可能与某些酸反应。(2)84消毒液具有氧化性,预测的依据是
(3)实验验证:
| 实验序号 | 操作 | 现象 | 结论或解释 |
| ⅰ | 向稀释后的84消毒液中滴入稍过量的KI溶液和几滴淀粉 | 84消毒液具有氧化性 | |
| ⅱ | 向稀释后的84消毒液中滴入稀盐酸 | 溶液变为黄绿色 | 反应的离子方程式 |
| ⅲ | 向稀释后的84消毒液中通入 | 无明显现象 |

观察到ⅲ—1试管中无明显现象,ⅱ—2、ⅲ—3中红色布条均褪色,ⅲ—3中红色布条褪色更明显。
①对比ⅲ—1、ⅰ—2的现象,可得到的结论是
②对比ⅰ—2、ⅲ—3的现象,产生该现象差异的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】在稀硫酸、二氧化碳、铜片、食盐、石灰水、一氧化碳、纯碱、铁片和木炭粉9种物质间存在图示关系,选择其中适当的物质,使有连线的两种物质发生反应。

(1)请推断它们的化学式:①_______ ;④_______ ;⑤_______ 。
(2)写出下列物质之间发生反应的化学方程式:
①和②_______ ;
⑤和④_______ 。

(1)请推断它们的化学式:①
(2)写出下列物质之间发生反应的化学方程式:
①和②
⑤和④
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】随着新能源汽车销量逐年攀升,动力电池的制备和回收利用技术至关重要。一种锂电池的正极材料——磷酸铁锂(LiFePO4)的制备方法框图所示。

回答下列问题:
(1)LiFePO4中铁元素的化合价为___________ 。氧化铁红属于氧化物,其化学式为___________ 。上述属于酸式盐的化学式为___________ 。
(2)将Li2CO3、磷酸铁与足量炭黑混合高温灼烧制备LiFePO4,写出化学反应方程式。___________ 。炭黑的另一个作用是___________ 。
含LiFePO4的废旧电池回收制备Li2CO3的流程图如下:

(3)浸出过程中温度不宜高于40℃,原因是___________ 。
(4)操作a的名称为___________ ,需使用玻璃仪器有___________ 。
(5)“沉锂”步骤的反应原理为___________ 。已知在20℃时,S(Li2CO3)=1.3g/100g水。S(Na2CO3)=20g/100g水,简述上述反应发生的原因___________ 。
(6)欲证明Li2CO3产品中是否含LiCl,简述实验方法(包括步骤、试剂、现象和结论等)___________ 。

回答下列问题:
(1)LiFePO4中铁元素的化合价为
(2)将Li2CO3、磷酸铁与足量炭黑混合高温灼烧制备LiFePO4,写出化学反应方程式。
含LiFePO4的废旧电池回收制备Li2CO3的流程图如下:

(3)浸出过程中温度不宜高于40℃,原因是
(4)操作a的名称为
(5)“沉锂”步骤的反应原理为
(6)欲证明Li2CO3产品中是否含LiCl,简述实验方法(包括步骤、试剂、现象和结论等)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某研究性学习小组为了验证臭氧的氧化性强于氧气,进行了下述实验,请参与探究并回答相关问题.
[实验目的]验证臭氧的氧化性强于氧气
[实验原理]2KI+O3+H2O===2KOH+I2+O2,淀粉溶液遇单质碘变蓝色.
[实验用品]臭氧消毒碗柜、a溶液、碘化钾溶液、滤纸、玻璃片、温度计.
[实验步骤]①取a溶液与碘化钾溶液混合;
②取两片用滤纸剪成的纸条,在a和碘化钾的混合液中湿润后分别置于两块洁净的玻璃片上;
③将一块玻璃片(Ⅰ)置于臭氧消毒碗柜中并接通电源生成臭氧.将另一块玻璃片(Ⅱ)置于可控温度的温箱里,尽量地使温箱的温度与消毒碗柜中的温度相等;
④观察现象并进行记录:
请根据上述实验原理、步骤及你所学的知识,回答下列问题:
(1)实验原理的化学反应的反应类型是________ (填序号).
A.离子反应 B.氧化还原反应
C.复分解反应 D.置换反应
E.分解反应 F.化合反应
(2)实验药品中的a溶液是________ 溶液.
(3)写出在臭氧消毒柜中产生O3的化学方程式:__________________________________ .
(4)整个实验过程要保持两块玻璃片所在环境的温度相同的原因是:________________ .
(5)从实验数据记录不能得出的结论是________ (填序号).
A.O3的氧化性比O2强
B.氧气也能氧化碘化钾中的碘离子
C.空气中可能也有一定浓度的O3,所以实验数据不可靠,不能达到实验目的
D.O3不仅氧化I-的速率比氧气快,而且有漂白作用
(6)在O3氧化KI的反应中,若有9.6 g O3发生反应,则转移电子的物质的量为________ .
[实验目的]验证臭氧的氧化性强于氧气
[实验原理]2KI+O3+H2O===2KOH+I2+O2,淀粉溶液遇单质碘变蓝色.
[实验用品]臭氧消毒碗柜、a溶液、碘化钾溶液、滤纸、玻璃片、温度计.
[实验步骤]①取a溶液与碘化钾溶液混合;
②取两片用滤纸剪成的纸条,在a和碘化钾的混合液中湿润后分别置于两块洁净的玻璃片上;
③将一块玻璃片(Ⅰ)置于臭氧消毒碗柜中并接通电源生成臭氧.将另一块玻璃片(Ⅱ)置于可控温度的温箱里,尽量地使温箱的温度与消毒碗柜中的温度相等;
④观察现象并进行记录:
| 时间(min) | 0 | 15 | 30 | 45 | 60 | 90 | 120 | |
| 滤纸的颜色变化 | 玻璃(Ⅰ) 上的滤纸 | 白色 | 白色 | 灰色 | 浅蓝色 | 蓝色 | 蓝色 | 浅蓝色 |
| 玻璃 (Ⅱ) 上的滤纸 | 白色 | 白色 | 白色 | 白色 | 灰色 | 灰色 | 浅蓝色 | |
(1)实验原理的化学反应的反应类型是
A.离子反应 B.氧化还原反应
C.复分解反应 D.置换反应
E.分解反应 F.化合反应
(2)实验药品中的a溶液是
(3)写出在臭氧消毒柜中产生O3的化学方程式:
(4)整个实验过程要保持两块玻璃片所在环境的温度相同的原因是:
(5)从实验数据记录不能得出的结论是
A.O3的氧化性比O2强
B.氧气也能氧化碘化钾中的碘离子
C.空气中可能也有一定浓度的O3,所以实验数据不可靠,不能达到实验目的
D.O3不仅氧化I-的速率比氧气快,而且有漂白作用
(6)在O3氧化KI的反应中,若有9.6 g O3发生反应,则转移电子的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】I.铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”【化学式为Cu2(OH)2CO3】。“铜绿”能跟酸反应生成铜盐和CO2、H2O。某同学利用下述系列反应实现了:“铜→铜绿→……→铜”的转化:
铜 铜绿
铜绿 A
A Cu(OH)2
Cu(OH)2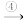 B
B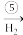 Cu
Cu
(1)请写出“铜绿”与盐酸反应的化学方程式:________ 。
(2)上述转化过程中属于化合反应的是________ (填序号,下同),属于分解反应的是________ 。
Ⅱ.1941年,我国科学家侯德榜结合地域条件改进索尔维制碱法,提出纯碱与铵肥的联合生产工艺,后被命名为“侯氏制碱法”。主要工艺流程如图。

根据以上流程回答下列问题:
(3)碳酸化这一步的原理是(用化学方程式表示)________ 。
(4)侯氏制碱法副产品的一种用途为________ 。
(5)Y物质是________ 。
(6)向母液中通氨气,加入细小食盐颗粒,降温结晶析出副产品,通氨气的作用有_______ (填字母)。
铜
 铜绿
铜绿 A
A Cu(OH)2
Cu(OH)2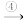 B
B Cu
Cu(1)请写出“铜绿”与盐酸反应的化学方程式:
(2)上述转化过程中属于化合反应的是
Ⅱ.1941年,我国科学家侯德榜结合地域条件改进索尔维制碱法,提出纯碱与铵肥的联合生产工艺,后被命名为“侯氏制碱法”。主要工艺流程如图。

根据以上流程回答下列问题:
(3)碳酸化这一步的原理是(用化学方程式表示)
(4)侯氏制碱法副产品的一种用途为
(5)Y物质是
(6)向母液中通氨气,加入细小食盐颗粒,降温结晶析出副产品,通氨气的作用有
| A.使Na2CO3结晶析出 |
| B.使NaHCO3转化为Na2CO3,提高析出NH4Cl的纯度 |
| C.使NaHCO3更多地析出 |
D.增大NH 的浓度,使NH4Cl更多地析出 的浓度,使NH4Cl更多地析出 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】海洋是人类巨大的资源宝库,如图为某课题小组模拟从海水中提取金属镁的简易流程图。

【信息】
某品牌不同碱的价格
请分析:
(1)海水和母液都可以作为制取氯化镁的原料,小真同学提出选择母液更好,小组同学一致同意他的观点,理由是_______ 。
(2)在工业生产中为了降低成本,步骤Ⅰ中的试剂①最好选择表格中的_______ 。
(3)步骤Ⅱ由氢氧化镁制得氯化镁反应的化学方程式为_______ ,该反应属于_______ 反应(填基本反应类型)。

【信息】
某品牌不同碱的价格
| 试剂 | NaOH |  | KOH |
| 价格(元/吨) | 3100 | 670 | 7000 |
请分析:
(1)海水和母液都可以作为制取氯化镁的原料,小真同学提出选择母液更好,小组同学一致同意他的观点,理由是
(2)在工业生产中为了降低成本,步骤Ⅰ中的试剂①最好选择表格中的
(3)步骤Ⅱ由氢氧化镁制得氯化镁反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】M是一种单质,A、B、C、D、E、F、G都是含有同一种元素的物质,这七种物质相互转变的关系如图所示:

(1)写出下列物质的颜色:M_______ F_______ ,
(2)写出下列变化的化学方程式
A→B:_______ 该反应中每消耗0.3 mol的A,可转移电子_______ mol。
E→G_______ ;
D→C_______ 。
(3)上述反应中,属于氧化还原反应的有_______ 个

(1)写出下列物质的颜色:M
(2)写出下列变化的化学方程式
A→B:
E→G
D→C
(3)上述反应中,属于氧化还原反应的有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】二氧化硫及硫酸盐在生活、生产中有重要应用。回答下列问题:
I.测定晶体结晶水含量的实验中常选择胆矾作为实验对象进行研究。
(1)结合已有知识及表格中信息解释原因_______ 。
II.《唐本草》和《天工开物》等古籍均记载中国很早就焙烧绿矾制备铁红(主要成分Fe2O3,是一种传统颜料的着色剂)和含硫气体等。
(2)对含硫气体的成分,某学生做出三种假设:①含硫气体为SO2;②含硫气体为SO3;③含硫气体为SO2和SO3。从上述三种假设中挑选一种不合理的,做出解释:_______ 。
(3)将盛有绿矾的硬质玻璃管A按下图装置,加强热使其充分反应。
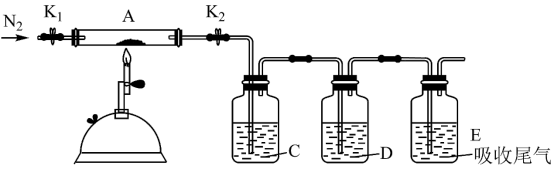
C、D中的溶液依次为_______ 、_______ (选填字母编号)。
a.品红溶液 b.Ba(OH)2溶液 c.盐酸酸化的BaCl2溶液 d.浓硫酸
III.SO2常用于食品加工中作防腐剂、漂白剂。我国规定葡萄酒中SO2最大使用量为0.26g·L-1。某研究小组测定葡萄酒中SO2含量的方法为:在300.00mL葡萄酒中加入适量稀硫酸,加热使SO2全部逸出,并用H2O2完全吸收,再将吸收了SO2的H2O2充分加热后,用0.0900mol·L-1NaOH溶液进行滴定。
(4)H2O2吸收SO2的化学方程式为_______ 。“将吸收了SO2的H2O2充分加热”目的是_______ 。
(5)若选用酚酞作指示剂,滴定终点的现象为_______ 。滴定终点时消耗NaOH溶液25.00mL,该葡萄酒中的SO2含量为_______ g·L-1。该葡萄酒的此项指标被判定为_______ 。(选填:合格、不合格)
I.测定晶体结晶水含量的实验中常选择胆矾作为实验对象进行研究。
(1)结合已有知识及表格中信息解释原因
| 明矾 | 胆矾 | 绿矾 | |
| 化学式 | KAl(SO4)2·12H2O | CuSO4·5H2O | FeSO4·7H2O |
| 色态 | 无色透明 | 蓝色 | 浅绿色 |
| 失去全部结晶水温度(℃) | 200 | 200 | 300 |
II.《唐本草》和《天工开物》等古籍均记载中国很早就焙烧绿矾制备铁红(主要成分Fe2O3,是一种传统颜料的着色剂)和含硫气体等。
(2)对含硫气体的成分,某学生做出三种假设:①含硫气体为SO2;②含硫气体为SO3;③含硫气体为SO2和SO3。从上述三种假设中挑选一种不合理的,做出解释:
(3)将盛有绿矾的硬质玻璃管A按下图装置,加强热使其充分反应。

C、D中的溶液依次为
a.品红溶液 b.Ba(OH)2溶液 c.盐酸酸化的BaCl2溶液 d.浓硫酸
III.SO2常用于食品加工中作防腐剂、漂白剂。我国规定葡萄酒中SO2最大使用量为0.26g·L-1。某研究小组测定葡萄酒中SO2含量的方法为:在300.00mL葡萄酒中加入适量稀硫酸,加热使SO2全部逸出,并用H2O2完全吸收,再将吸收了SO2的H2O2充分加热后,用0.0900mol·L-1NaOH溶液进行滴定。
(4)H2O2吸收SO2的化学方程式为
(5)若选用酚酞作指示剂,滴定终点的现象为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知物质A~I之间的转化关系符合下图所示。其中A、C、F、G、I为常见固体且焰色反应均为黄色;A为海水中主要溶质,B为常温下常见液体;E为黄绿色气体,H是无色无味且能使澄清石灰水变浑浊的气体。

试回答下列问题:
(1)写出下列物质的化学式:D______________ H______________
(2)反应①的化学方程式为:_______________________________ 。
(3)反应②的化学方程式为:_______________________________ 。

试回答下列问题:
(1)写出下列物质的化学式:D
(2)反应①的化学方程式为:
(3)反应②的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知甲、乙、丙、丁、戊为纯净物,它们之间有如下转化关系。请填空:

(1)若甲为厨房中常见的调味品,在熔融条件下电解能实现上述转化。以惰性电极电解甲的水溶液时,电解反应的离子方程式为:________________________ 。
(2)若甲为常见的离子化合物,可用作化肥,在加热条件下能实现上述转化。则反应②的化学反应方程式:_____________________________________ 。实验室测定丁的相对分子质量时,得到的实验值总是比理论值大,其原因是_______________________ 。(用方程式表示)
(3)若甲为制镜工业的常用物质,相对分子质量是甲醛的6倍,在催化剂存在条件下能实现上述转化。则反应①的化学反应方程式为:______________ ;以乙物质为燃料的微生物燃料电池结构示意图如图所示,该原电池的负极反应方程式为___________________ 。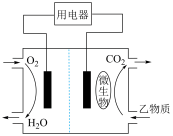

(1)若甲为厨房中常见的调味品,在熔融条件下电解能实现上述转化。以惰性电极电解甲的水溶液时,电解反应的离子方程式为:
(2)若甲为常见的离子化合物,可用作化肥,在加热条件下能实现上述转化。则反应②的化学反应方程式:
(3)若甲为制镜工业的常用物质,相对分子质量是甲醛的6倍,在催化剂存在条件下能实现上述转化。则反应①的化学反应方程式为:

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下列框图涉及到的物质所含元素中,除一种元素外,其余均为1~18号元素。

已知: A、F为无色气体单质,B为具有刺激性气味的气体,C为黑色氧化物,E为红色金属单质(部分反应的产物未列出)。请回答下列问题:
(1)D的化学式为________ ;F的电子式为________ 。
(2)A与B生成D的反应在工业上是生产________ 的反应原理之一。
(3)E与G的稀溶液反应的离子方程式为________ 。
(4)B和C反应的化学方程式为_______ 。
(5)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式_____________________________ 。

已知: A、F为无色气体单质,B为具有刺激性气味的气体,C为黑色氧化物,E为红色金属单质(部分反应的产物未列出)。请回答下列问题:
(1)D的化学式为
(2)A与B生成D的反应在工业上是生产
(3)E与G的稀溶液反应的离子方程式为
(4)B和C反应的化学方程式为
(5)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式
您最近一年使用:0次




