已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性:
已知:一般来说,两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是_________________ 。
(2)判断下列物质是离子化合物还是共价化合物? Mg3N2__________ BeCl2__________ AlCl3__________ SiC__________
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:一般来说,两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是
(2)判断下列物质是离子化合物还是共价化合物? Mg3N2
更新时间:2019-06-23 19:07:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】哈尔滨工业大学的李惠等人和加州大学洛杉矶分校的黄昱、段镶锋合作合成了具备超轻、高力学强度和超级隔热三大特点的氮化硼(hBNAGs)以及碳化硅( -SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
-SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
(1)硅原子的价电子排布图为___________ 。B、N、O、Al的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(2)硼元素深受配位化学家的喜爱,其原因在于B容易与配体形成配位键,如BF 。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O
。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O H+ + [B(OH)4]−。
H+ + [B(OH)4]−。
① 从原子结构分析B容易与配体形成配位键的原因___________ 。
② 下列有关硼酸及其相关化合物的说法正确的是___________ (填标号)。
A.硼酸的电离过程中有配位键形成
B.硼酸为三元酸
C.Na[B(OH)4]的水溶液呈碱性
D.硼酸和[B(OH)4]−中的键角相同
(3)氨硼烷(NH3BH3)具有良好的储氢能力。已知B、N、H三种元素的电负性如下:
① 下列有关氨硼烷(NH3BH3)的说法中错误的是___________ (填标号)。
A.H元素为+1价
B.氨硼烷中有配位键
C.N和B原子均为sp3杂化
D.氨硼烷在一定条件下能与水反应产生氢气
② 氨硼烷中H−N−H的键角___________ (填“>”“<”或“=”)H−B−H的键角。
 -SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:
-SiCAGs)陶瓷气凝胶材料,这种坚固的材料系统非常适用于当作极端条件下的超热绝缘体使用,主要用于航天器领域。回答下列问题:(1)硅原子的价电子排布图为
(2)硼元素深受配位化学家的喜爱,其原因在于B容易与配体形成配位键,如BF
 。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O
。硼酸[B(OH)3]在水中电离产生H+过程为:B(OH)3 + H2O H+ + [B(OH)4]−。
H+ + [B(OH)4]−。① 从原子结构分析B容易与配体形成配位键的原因
② 下列有关硼酸及其相关化合物的说法正确的是
A.硼酸的电离过程中有配位键形成
B.硼酸为三元酸
C.Na[B(OH)4]的水溶液呈碱性
D.硼酸和[B(OH)4]−中的键角相同
(3)氨硼烷(NH3BH3)具有良好的储氢能力。已知B、N、H三种元素的电负性如下:
| 元素符号 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
A.H元素为+1价
B.氨硼烷中有配位键
C.N和B原子均为sp3杂化
D.氨硼烷在一定条件下能与水反应产生氢气
② 氨硼烷中H−N−H的键角
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W、R是原子序数依次增大的前四周期元素,这五种元素的相关信息如下:
(1)基态R原子的电子排布式为________________ 。
(2)Y2分子中σ键和π键的数目比为________ 。
(3)X、Y、Z三种元素的第一电离能由小到大的顺序为____ (用元素符号表示),元素Y的简单气态氢化物的沸点比元素X的简单气态氢化物沸点高的主要原因是____ 。
(4)元素Z、W组成的微粒WZ42-的空间构型是_____ ,其中W原子的杂化轨道类型为_____ 。
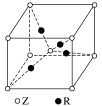
(5)已知Z、R能形成一种化合物,其晶胞结构如图所示,该化合物的化学式为______ ;若相邻的Z原子和R原子间的距离为acm,设阿伏加德常数的值为NA,则该晶体的密度为______ g·cm-3(用含a、NA的代数式表示)。
| 元素 | 相关信息 |
| X | 其中一种核素在考古时常用来鉴定一些文物的年代 |
| Y | 原子核外电子有7种不同的运动状态 |
| Z | 地壳中含量最高的元素 |
| W | 价电子排布式为(n+1)sn(n+1)pn+2 |
| R | 基态原子最外能层只有一个电子,其他能层均已充满电子 |
(1)基态R原子的电子排布式为
(2)Y2分子中σ键和π键的数目比为
(3)X、Y、Z三种元素的第一电离能由小到大的顺序为
(4)元素Z、W组成的微粒WZ42-的空间构型是
(5)已知Z、R能形成一种化合物,其晶胞结构如图所示,该化合物的化学式为

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】叠氮化钠(NaN3)是一种无色晶体,广泛用于汽车安全气囊及化工合成等.常见的两种制备方法为:
2NaNH2+N2O═NaN3+NaOH+NH3↑
3NaNH2+NaNO3═NaN3+3NaOH+NH3↑
(1)①氮原子的L层电子排布图_____________________ 。
②氮所在的周期中,第一电离能最大的元素为_____________ (填元素符号)。
③与N3互为等电子体的粒子为____________ (写出一种)。
④氨气的电子式____________ 。
(2)NH3沸点(﹣33.34℃)比N2O沸点(﹣88.49℃)高,其主要原因是____________
(3)依据价层电子对互斥理论,NO3-间构型呈__________ 形。
(4)汽车安全气囊的设计是基于反应6NaN3+Fe2O3═3Na2O+2Fe+9N2↑,生成物中的铁是一种常见物质,而铁的晶体有三种堆积方式,其中两种的堆积方式如图所示,下列有关铁及晶体的说法中正确的是_________ 。
A.金属铁的导电性是由于通电时产生的自由电子作定向移动
B.α﹣Fe、γ﹣Fe的堆积方式分别与钾和铜相同
C.空间利用率α﹣Fe大于γ﹣Fe
D.金属铁内部存在金属键
(5)铁的上述两种晶体(α﹣Fe:γ﹣Fe)的密度比值为___________ 。(写成小数,保留2位有效数字)

2NaNH2+N2O═NaN3+NaOH+NH3↑
3NaNH2+NaNO3═NaN3+3NaOH+NH3↑
(1)①氮原子的L层电子排布图
②氮所在的周期中,第一电离能最大的元素为
③与N3互为等电子体的粒子为
④氨气的电子式
(2)NH3沸点(﹣33.34℃)比N2O沸点(﹣88.49℃)高,其主要原因是
(3)依据价层电子对互斥理论,NO3-间构型呈
(4)汽车安全气囊的设计是基于反应6NaN3+Fe2O3═3Na2O+2Fe+9N2↑,生成物中的铁是一种常见物质,而铁的晶体有三种堆积方式,其中两种的堆积方式如图所示,下列有关铁及晶体的说法中正确的是
A.金属铁的导电性是由于通电时产生的自由电子作定向移动
B.α﹣Fe、γ﹣Fe的堆积方式分别与钾和铜相同
C.空间利用率α﹣Fe大于γ﹣Fe
D.金属铁内部存在金属键
(5)铁的上述两种晶体(α﹣Fe:γ﹣Fe)的密度比值为

您最近半年使用:0次
【推荐1】某硅酸盐研究所在硅酸盐材料和闪烁晶体等领域研究上取得了重大的成就。
(1)[SiO4]4-是构成硅酸盐的基本结构单元,通过共用氧相连可形成硅氧组群。
①基态硅原子价电子的轨道表示式是_____________ 。
②与[SiO4]4-互为等电子体的微粒符号是_____________ 任写一种)。
③下图为一种硅氧组群的结构示意图,其离子符号为_____________ ,其中Si原子的杂化方式为_____________ 。
④电负性:Si______ O(填“>”、 “=”或“<” )。
(2)钨酸铅(PWO)是一种闪烁晶体,晶胞结构如图所示。
PWO中钨酸根结构式为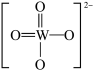 ,该离子中,σ键和π键的个数比是
,该离子中,σ键和π键的个数比是_____________ 。
②PWO晶体中含有的微粒间作用力是___________________
A.范德华力 B.离子键 C.共价键 D.金属键
③已知PWO的摩尔质量为Mg·mol-1,则该晶体的密度d=_____________ g·cm-3。
(1)[SiO4]4-是构成硅酸盐的基本结构单元,通过共用氧相连可形成硅氧组群。
①基态硅原子价电子的轨道表示式是
②与[SiO4]4-互为等电子体的微粒符号是
③下图为一种硅氧组群的结构示意图,其离子符号为

④电负性:Si
(2)钨酸铅(PWO)是一种闪烁晶体,晶胞结构如图所示。
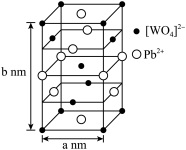
PWO中钨酸根结构式为
 ,该离子中,σ键和π键的个数比是
,该离子中,σ键和π键的个数比是②PWO晶体中含有的微粒间作用力是
A.范德华力 B.离子键 C.共价键 D.金属键
③已知PWO的摩尔质量为Mg·mol-1,则该晶体的密度d=
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
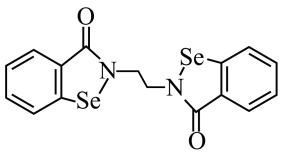
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如图:
①基态 原子的核外电子排布式为[Ar]
原子的核外电子排布式为[Ar]_______ 。
②该新药分子中有_______ 种不同化学环境的C原子。
③比较键角大小:气态SeO3分子_______ SeO 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是_______ 。
(2)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示:
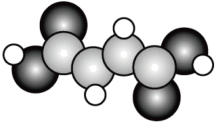
①富马酸分子中σ键与π键的数目比为_______ 。
②富马酸亚铁中各元素的电负性由大到小的顺序为_______ 。
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如图:

①基态
 原子的核外电子排布式为[Ar]
原子的核外电子排布式为[Ar]②该新药分子中有
③比较键角大小:气态SeO3分子
 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是(2)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示:

①富马酸分子中σ键与π键的数目比为
②富马酸亚铁中各元素的电负性由大到小的顺序为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W的第一电离能比氧原子的________ (填“大”或“小”),W的气态氢化物稳定性比H2O(g)_______ (填“强”或“弱”),W的单质分子中含_________ 个∏键;
(2)Z位于元素周期表第__ 周期第___ 族,Z的基态原子核外电子排布式是________ ;
(3)X、Y的最高价氧化物对应水化物相互反应的离子方程式是
_______________________________________________________________ 。
(1)W的第一电离能比氧原子的
(2)Z位于元素周期表第
(3)X、Y的最高价氧化物对应水化物相互反应的离子方程式是
您最近半年使用:0次



