成熟的苹果中含有淀粉、葡萄糖和无机盐等,某课外兴趣小组设计了一组实验证明某些成份的存在,请你参与并协助他们完成相关实验。
(1)用小试管取少量的苹果汁,加入_________ ,溶液变蓝,则苹果中含有淀粉。
(2)用小试管取少量的苹果汁,加入新制Cu(OH)2悬浊液,并加热,产生砖红色的沉淀,则苹果中含有____________ (写分子式)。
(3)葡萄糖在一定条件下可以得到化学式为C2H6O的化合物A。
A + CH3COOH→有香味的产物
① 含A的体积分数为75%的水溶液可以用做_____________ 。
②写出化合物A与CH3COOH反应的化学方程式为______________________ ,该反应的类型为_____ 。
(4)苹果中含有苹果酸,测得其相对分子质量为134。取0.02mol苹果酸,使其完全燃烧,将燃烧后的产物先后通过足量的无水CaCl2和碱石灰,两者分别增重1.08g 和 3.52g。则分子中C、H原子的个数比_______ 。苹果酸的分子式是___________ 。
(1)用小试管取少量的苹果汁,加入
(2)用小试管取少量的苹果汁,加入新制Cu(OH)2悬浊液,并加热,产生砖红色的沉淀,则苹果中含有
(3)葡萄糖在一定条件下可以得到化学式为C2H6O的化合物A。
A + CH3COOH→有香味的产物
① 含A的体积分数为75%的水溶液可以用做
②写出化合物A与CH3COOH反应的化学方程式为
(4)苹果中含有苹果酸,测得其相对分子质量为134。取0.02mol苹果酸,使其完全燃烧,将燃烧后的产物先后通过足量的无水CaCl2和碱石灰,两者分别增重1.08g 和 3.52g。则分子中C、H原子的个数比
12-13高二上·山东济宁·期中 查看更多[4]
江西省南昌市八一中学2019-2020学年高二下学期期末考试化学试题人教版高中化学必修二第三单元《有机化合物》测试卷(已下线)2012-2013学年福建省泉州一中高二上学期期中考试化学试卷(已下线)2012-2013学年山东济宁鱼台一中高二上学期期中考试化学试卷
更新时间:2012-12-25 16:46:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求回答下列问题:
(1)完全燃烧0.1mol某烃,燃烧产物依次通过浓硫酸、碱石灰,实验结束后,称得浓硫酸增重9g,碱石灰增重17.6g。该烃的化学式为_______ ,并写出其所有可能的结构简式:_______ 。
(2)某烃2.2g,在O2中完全燃烧,生成6.6gCO2和3.6gH2O,在标准状况下其密度为1.9643g∙L-1,其化学式为_______ 。
(3)某烷烃的相对分子质量为128,该烷烃的化学式为_______ 。
(1)完全燃烧0.1mol某烃,燃烧产物依次通过浓硫酸、碱石灰,实验结束后,称得浓硫酸增重9g,碱石灰增重17.6g。该烃的化学式为
(2)某烃2.2g,在O2中完全燃烧,生成6.6gCO2和3.6gH2O,在标准状况下其密度为1.9643g∙L-1,其化学式为
(3)某烷烃的相对分子质量为128,该烷烃的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常见烃的分子结构
| 烃 | 甲烷 | 乙烯 | 乙炔 |
| 电子式 |  |  | 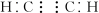 |
| 化学键 | H—C和—C≡C— | ||
| 分子结构特点 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D为常见的烃的衍生物。工业上通过乙烯水化法制取A,A催化氧化可得B,B进一步氧化得到C,C能使紫色石蕊试液变红。完成下列填空:
(1)A的俗称为__________ 。A与氧气在加热及催化剂存在下反应生成B,常用到的催化剂是_____________ ,B的结构简式为________________ 。
(2)写出A与C发生酯化反应的化学方程式。______
(3)1.5 g D在空气中完全燃烧,生成0.05 mol二氧化碳和0.05 mol H2O。在标准状况下,D是气体,密度为1.34 g/L,则D的分子式为__________ 。已知D与B具有相同的官能团,D的结构简式为________________ 。
(1)A的俗称为
(2)写出A与C发生酯化反应的化学方程式。
(3)1.5 g D在空气中完全燃烧,生成0.05 mol二氧化碳和0.05 mol H2O。在标准状况下,D是气体,密度为1.34 g/L,则D的分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)甲烷和氯气发生的一系列反应都是_________ 反应,写出第一步反应的化学方程式_________________________________________________ 。
(2)分子中含有34个氢原子的烷烃是_________ (填名称),乙烯的结构简式为_____________________ ,糖尿病患者尿液中含的糖类的分子式________________ 。
(3)现有四种试剂:A.新制的Cu(OH)2;B.浓硝酸;C.AgNO3溶液;D.碘水。为了鉴别下列四瓶无色溶液,请你选择合适的试剂,将其填入相应的括号中。
①葡萄糖溶液( ) ②食盐溶液( )
③淀粉溶液( ) ④鸡蛋清溶液( )
(4)将下列各组金属与其对应的最佳冶炼方法用线连起来:_______________
金属组 冶炼方法
Fe、Zn、Cu等中等活泼的金属 利用铝热反应原理用Al还原
Na、Mg、Al等活泼金属 以C、CO或 H2作还原剂还原
Hg、Ag等不活泼金属 电解法
V、Cr、Mn、W等高熔点金属 热分解法
(2)分子中含有34个氢原子的烷烃是
(3)现有四种试剂:A.新制的Cu(OH)2;B.浓硝酸;C.AgNO3溶液;D.碘水。为了鉴别下列四瓶无色溶液,请你选择合适的试剂,将其填入相应的括号中。
①葡萄糖溶液
③淀粉溶液
(4)将下列各组金属与其对应的最佳冶炼方法用线连起来:
金属组 冶炼方法
Fe、Zn、Cu等中等活泼的金属 利用铝热反应原理用Al还原
Na、Mg、Al等活泼金属 以C、CO或 H2作还原剂还原
Hg、Ag等不活泼金属 电解法
V、Cr、Mn、W等高熔点金属 热分解法
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)化学与生活息息相关。下列叙述正确的是________(填字母代号,下同)。
(2)把新制的Cu(OH)2悬浊液加入到某病人的尿液中并微热,如果观察到砖红色沉淀,说明尿液中可能含有的物质是________。
(3)生活中常用药品很多,如:A.碘酒、B.麻黄碱、C.青霉素、D.阿司匹林、E.葡萄糖注射液、F.胃舒平(含氢氧化铝、淀粉等)。
①上述物质中属于抗生素的是________ (填字母代号,下同),具有止咳平喘作用的天然药物是________ 胃舒平可防治胃酸分泌过多,其发挥功效时的离子方程式 为________ 。
②低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是________ (填字母代号)。
A.加成反应 B.取代反应 C.氧化反应 D.聚合反应
(4)研究发现,长期使用铁锅炒菜,可有效减少缺铁性________ 病症的发生,为了提高补铁效果,在炒菜时可经常加入适量的__________ (填“食醋”或“料酒”)。炒完菜之后不洗锅,铁锅通常会生锈,此过程中主要发生________ 腐蚀(填“化学”或“电化学”),请写出金属防护的一种方法__________ 。
(1)化学与生活息息相关。下列叙述正确的是________(填字母代号,下同)。
| A.鲜榨橙汁遇到碘水会变蓝 | B.馒头越嚼越甜 |
| C.油脂经水解可变成葡萄糖 | D.土豆中的淀粉经水解可变成酒 |
| A.食醋 | B.白酒 |
| C.食盐 | D.葡萄糖 |
①上述物质中属于抗生素的是
②低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是
A.加成反应 B.取代反应 C.氧化反应 D.聚合反应
(4)研究发现,长期使用铁锅炒菜,可有效减少缺铁性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】目前,我国已经有上百个地区的加油站可提供标号为E90、E93的乙醇汽油,它们是在90#、93#汽油中加入了一定量的乙醇而制得。
(1)用玉米生产燃料乙醇的生产如下图表示:

①粉碎玉米的目的是____ 。步骤a的操作是___ 。
②以玉米等淀粉原料生产乙醇的化学反应可用下式表示:
(C6H10O5)n+ nH2O→nC6H12O6
C6H12O6→2C2H5OH + 2CO2↑
100 kg玉米淀粉最多可生产无水乙醇____ kg。
(2)乙醇汽油在储存和运输过程中应特别注意防水。如果乙醇汽油中混入了水,可能出现______ 现象。
(3)常温下,1g乙醇完全燃烧释放29.71kJ热量,请写出乙醇完全燃烧的热化学方程式______ 。
(4)由玉米等农产品为原料制得的乙醇作燃料,是否是增加大气中CO2的含量,为什么?______ 。
(1)用玉米生产燃料乙醇的生产如下图表示:

①粉碎玉米的目的是
②以玉米等淀粉原料生产乙醇的化学反应可用下式表示:
(C6H10O5)n+ nH2O→nC6H12O6
C6H12O6→2C2H5OH + 2CO2↑
100 kg玉米淀粉最多可生产无水乙醇
(2)乙醇汽油在储存和运输过程中应特别注意防水。如果乙醇汽油中混入了水,可能出现
(3)常温下,1g乙醇完全燃烧释放29.71kJ热量,请写出乙醇完全燃烧的热化学方程式
(4)由玉米等农产品为原料制得的乙醇作燃料,是否是增加大气中CO2的含量,为什么?
您最近一年使用:0次
【推荐2】我国传统酿醋工艺主要包括以下过程:①“蒸”——将大米、高粱、小米等原料蒸熟后放至冷却;②“酵”——拌曲入坛发酵,使淀粉经糖化发酵生成乙醇,然后在醋酸菌的作用下生成乙酸;③“沥”——除去醋坛底层的糟,此时可以闻到酒和醋混合在一起的香味;④“陈”——将醋陈放1~3年,以增强其风味,在此过程中乙酸与乙醇缓慢地发生反应生成一种具有果香味的有机化合物。
(1)请写出上述过程中涉及主要反应的化学方程式_______ 。
(2)目前在市场上,除了酿造食醋外,还有配制食醋,它是在酿造食醋中加入乙酸等混合配制而成的。请对市场上出售的食醋进行调查,并查阅资料,了解酿造食醋和配制食醋在生产工艺和成分上有何异同,分析两者在风味上有所区别的原因。购买食醋时,你是如何辨别两者的_______ 。
(1)请写出上述过程中涉及主要反应的化学方程式
(2)目前在市场上,除了酿造食醋外,还有配制食醋,它是在酿造食醋中加入乙酸等混合配制而成的。请对市场上出售的食醋进行调查,并查阅资料,了解酿造食醋和配制食醋在生产工艺和成分上有何异同,分析两者在风味上有所区别的原因。购买食醋时,你是如何辨别两者的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综合症,以高血糖为主要标志。长期摄入高热量食品和缺少运动都易导致糖尿病。
(1)血糖是指血液中的葡萄糖 ( C6H12O6)。下列说法不正确的是_______ (填序号);
A.糖尿病人尿糖偏高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
B.葡萄糖属于碳水化合物,分子可表示为 C6(H2O)6,则每个葡萄糖分子中含6个H2O
C.葡萄糖可用于制镜工业
D.淀粉水解的最终产物是葡萄糖
(2)含糖类丰富的农产品通过发酵法可以制取乙醇,但随着石油化工的发展,工业上主要是以乙烯为原料,在加热、加压和有催化剂存在的条件下跟水反应生成乙醇,这种方法叫做乙烯水化法。试写出该反应的化学方程式:__________________ 。
(3)烯烃加到溴水中能使溴水褪色,现将丙烯和溴水褪色后的有机物与氢氧化钠的醇溶液混合加热,又能得到一种烃类物质,该反应的化学方程式为:_______________________ 。
(4)卤代烃的一些数据如下表,分析表中数据可以得出的结论是(写出2条即可)_____________________________________________________________________ 。
(1)血糖是指血液中的葡萄糖 ( C6H12O6)。下列说法不正确的是
A.糖尿病人尿糖偏高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
B.葡萄糖属于碳水化合物,分子可表示为 C6(H2O)6,则每个葡萄糖分子中含6个H2O
C.葡萄糖可用于制镜工业
D.淀粉水解的最终产物是葡萄糖
(2)含糖类丰富的农产品通过发酵法可以制取乙醇,但随着石油化工的发展,工业上主要是以乙烯为原料,在加热、加压和有催化剂存在的条件下跟水反应生成乙醇,这种方法叫做乙烯水化法。试写出该反应的化学方程式:
(3)烯烃加到溴水中能使溴水褪色,现将丙烯和溴水褪色后的有机物与氢氧化钠的醇溶液混合加热,又能得到一种烃类物质,该反应的化学方程式为:
(4)卤代烃的一些数据如下表,分析表中数据可以得出的结论是(写出2条即可)
| 烷 基 | 氟化物 | 氯化物 | 溴化物 | 碘化物 |
| 沸点℃ | 沸点℃ | 沸点℃ | 沸点℃ | |
| CH3— | -78.4 | -24.2 | 3.6 | 42.4 |
| CH3—CH2— | -37.7 | 12.3 | 38.40 | 72.3 |
| CH3—CH2—CH2— | 2.5 | 46.60 | 71.0 | 102.4 |
| (CH3)2—CH— | -9.4 | 35.7 | 59.48 | 89.14 |
| CH3—CH2—CH2—CH2— | 32.5 | 78.44 | 101.6 | 130.5 |
| (CH3)2—CH CH2— | 16.0 | 68.7 | 91.7 | 120.4 |
| (CH3)3C— | 12.1 | 52 | 73.25 | 120.8 |
您最近一年使用:0次
【推荐1】如图为C、H、O、N、P等元素构成大分子物质甲~丙的示意图。

(1)若图中物质甲能与碘液发生反应显蓝色,则单体3为___________ ,由物质甲生成单体3的化学方程式为___________ 。
(2)若图中丁是由蛋白质和核糖核酸组成的细胞器,则单体1为___________ ,单体2为___________ 。
(3)若物质丙可控制物质乙的合成,则物质丙通常为___________ ,物质丙水解得到的糖为___________ 。

(1)若图中物质甲能与碘液发生反应显蓝色,则单体3为
(2)若图中丁是由蛋白质和核糖核酸组成的细胞器,则单体1为
(3)若物质丙可控制物质乙的合成,则物质丙通常为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.氰化钠(NaCN)是一种重要的基本化工原料,用于化学合成、电镀、冶金和有机合成医药、农药,同时也是一种剧毒物质,一旦泄漏需要及时处理。一般可以用二氧化氯(ClO2)水溶液或硫代硫酸钠(Na2S2O3)溶液来处理,以减轻环境污染。
(1)NaCN用二氧化氯(ClO2)水溶液处理后,CN-被氧化为CO2和N2,该反应的离子方程式为____ 。
II.工业制备硫代硫酸钠的反应原理:2Na2S+Na2CO3+4SO2=3Na2S2O3 +CO2。某化学小组利用上述原理在实验室制备硫代硫酸钠,并用硫代硫酸钠溶液处理含氰化钠废水。
【实验一】实验室通过如图所示装置制备硫代硫酸钠。
关闭K1,打开K2,打开分液漏斗,缓慢滴加硫酸,控制好反应速率。

(2)①装置A中盛放浓硫酸的仪器名称是____ ;②装置B的作用是____ ;③实验结束后装置D烧杯中的溶质除NaOH之外,还可能有____ 。
(3)实验结束后,在E处可连接盛有____ (填序号)溶液的注射器,再关闭K2,打开K1,以防止拆除装置时装置中的有害气体逸出污染空气。
【实验二】测定硫代硫酸钠产品纯度并处理废水中的氰化钠。
制备的硫代硫酸钠产品一般为Na2S2O3•5H2O,一般可用I2的标准溶液测定产品纯度原理为:2Na2S2O3+I2= Na2S4O6+2NaI。
(4)上述滴定操作中应该选用____ 作为反应的指示剂。
(1)NaCN用二氧化氯(ClO2)水溶液处理后,CN-被氧化为CO2和N2,该反应的离子方程式为
II.工业制备硫代硫酸钠的反应原理:2Na2S+Na2CO3+4SO2=3Na2S2O3 +CO2。某化学小组利用上述原理在实验室制备硫代硫酸钠,并用硫代硫酸钠溶液处理含氰化钠废水。
【实验一】实验室通过如图所示装置制备硫代硫酸钠。
关闭K1,打开K2,打开分液漏斗,缓慢滴加硫酸,控制好反应速率。

(2)①装置A中盛放浓硫酸的仪器名称是
(3)实验结束后,在E处可连接盛有
| A.BaCl2溶液 | B.浓硫酸 | C.酸性KMnO4溶液 | D.NaOH溶液 |
【实验二】测定硫代硫酸钠产品纯度并处理废水中的氰化钠。
制备的硫代硫酸钠产品一般为Na2S2O3•5H2O,一般可用I2的标准溶液测定产品纯度原理为:2Na2S2O3+I2= Na2S4O6+2NaI。
(4)上述滴定操作中应该选用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】亚硝酸钠可使肉制品色泽粉红,外观上好看诱人,大量食用会致癌。
(1)NaNO2 俗称“工业盐”,外观与食盐相似,误食会中毒,可通过化学实验加以鉴别。如 向 NaNO2 的酸性溶液中加入 KI 固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验 NO2 。
①该反应中被氧化的元素是_______ (填符号)。
②完成下列反应的化学方程式并配平。
____ NaNO2+____ KI+____ H2SO4=____ +_____ +____ I2+____ NO↑+____
③标准状况下,该反应中每转移 1 mol e-,生成气体的体积是_______ 。
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为: 2NO2+Na2CO3=NaNO2+NaNO3+CO2↑氧化剂与还原剂的物质的量之比为_______ 。每产生 33.6 L(标准状况下)CO2,吸收液质量将增加 _______ g。
(3)某同学把 NaNO2 加到硫酸酸化的 KMnO4 溶液中,观察到 KMnO4 溶液褪色且无沉 淀生成,同时生成 KNO3 和 MnSO4,写出该反应的离子方程式:_______
(1)NaNO2 俗称“工业盐”,外观与食盐相似,误食会中毒,可通过化学实验加以鉴别。如 向 NaNO2 的酸性溶液中加入 KI 固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验 NO2 。
①该反应中被氧化的元素是
②完成下列反应的化学方程式并配平。
③标准状况下,该反应中每转移 1 mol e-,生成气体的体积是
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为: 2NO2+Na2CO3=NaNO2+NaNO3+CO2↑氧化剂与还原剂的物质的量之比为
(3)某同学把 NaNO2 加到硫酸酸化的 KMnO4 溶液中,观察到 KMnO4 溶液褪色且无沉 淀生成,同时生成 KNO3 和 MnSO4,写出该反应的离子方程式:
您最近一年使用:0次



