由一种短周期金属元素和一种非金属元素组成的化合物X可与水发生复分解反应。某校兴趣小组用如图所示装置(夹持装置略去)对其进行探究实验。
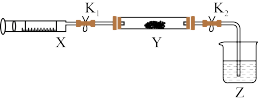
(1) 中红色石蕊试纸变蓝,则单质
中红色石蕊试纸变蓝,则单质 的电子式为
的电子式为___________ 。
(2)化合物 中含组成单质
中含组成单质 的元素的质量分数为16.9%,写出
的元素的质量分数为16.9%,写出 与水反应的化学方程式:
与水反应的化学方程式:___________ 。
(3) 中的试剂名称为
中的试剂名称为___________ 。
(4)实验时,装置 中硬质玻璃管内的现象为
中硬质玻璃管内的现象为___________ 。
(5)装置 中试剂
中试剂 为
为___________ (填化学式),装置 的作用是
的作用是___________ 。
(6)若不通过 、
、 两装置,请设计实验方案证明
两装置,请设计实验方案证明 中发生了反应(不通过观察
中发生了反应(不通过观察 中固体颜色变化:
中固体颜色变化:___________ 。
(7)若装置 中固体样品含有杂质(杂质不参与反应),某同学通过测定
中固体样品含有杂质(杂质不参与反应),某同学通过测定 中单质
中单质 在标准状况下的体积和固体样品的质量,以确定固体样品中
在标准状况下的体积和固体样品的质量,以确定固体样品中 的质量分数,判断该方案是否可行,并说明原因:
的质量分数,判断该方案是否可行,并说明原因:___________ 。


(1)
 中红色石蕊试纸变蓝,则单质
中红色石蕊试纸变蓝,则单质 的电子式为
的电子式为(2)化合物
 中含组成单质
中含组成单质 的元素的质量分数为16.9%,写出
的元素的质量分数为16.9%,写出 与水反应的化学方程式:
与水反应的化学方程式:(3)
 中的试剂名称为
中的试剂名称为(4)实验时,装置
 中硬质玻璃管内的现象为
中硬质玻璃管内的现象为(5)装置
 中试剂
中试剂 为
为 的作用是
的作用是(6)若不通过
 、
、 两装置,请设计实验方案证明
两装置,请设计实验方案证明 中发生了反应(不通过观察
中发生了反应(不通过观察 中固体颜色变化:
中固体颜色变化:(7)若装置
 中固体样品含有杂质(杂质不参与反应),某同学通过测定
中固体样品含有杂质(杂质不参与反应),某同学通过测定 中单质
中单质 在标准状况下的体积和固体样品的质量,以确定固体样品中
在标准状况下的体积和固体样品的质量,以确定固体样品中 的质量分数,判断该方案是否可行,并说明原因:
的质量分数,判断该方案是否可行,并说明原因:
更新时间:2021-10-14 12:34:53
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上用以下转化过程生产硝酸及其相关产品。请回答:

(1)写出步骤①的化学方程式:___________ 。
(2)下列说法正确的是___________。
(3)室温下, 极易溶于水,原因是
极易溶于水,原因是___________ 。请设计实验证明 极易溶于水:
极易溶于水:___________ 。
(4)步骤⑦同时释放出转化流程中的一种气体,写出步骤⑦的化学方程式:___________ 。

(1)写出步骤①的化学方程式:
(2)下列说法正确的是___________。
| A.步骤③O2过量有利于提高硝酸浓度 | B.步骤④⑤中硫酸所起的作用完全相同 |
| C.硝化纤维洗净后隔绝空气大火烘干 | D.通过①②③制得的硝酸的质量分数不超过 |
(3)室温下,
 极易溶于水,原因是
极易溶于水,原因是 极易溶于水:
极易溶于水:(4)步骤⑦同时释放出转化流程中的一种气体,写出步骤⑦的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】物质类别和元素价态是学习元素及其化合物性质的重要认识视角。如图是某元素M 的价类二维图。其中X是一种强碱,A为正盐,B能使湿润的红色石蕊试纸变蓝,通常条件下 Z是无色液体,D的相对分子质量比E小 16, 图中呈现了各物质的转化关系。
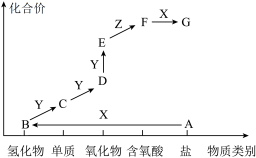
(1)下列说法正确的是_______。
(2)请写出B在加热和有催化剂条件下与Y反应生成D的化学方程式_______ 。
(3)设计检验正盐 A 中阳离子的实验方案_______ 。

(1)下列说法正确的是_______。
| A.物质 A 中只含离子键 |
| B.物质 B 可以和Y 反应直接转化为 E |
| C.物质D、E均可以用向上排空气法收集 |
| D.通过水可以除去 D 中含有的少量E |
(2)请写出B在加热和有催化剂条件下与Y反应生成D的化学方程式
(3)设计检验正盐 A 中阳离子的实验方案
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上制取硝酸铵的流程图如图,请回答下列问题:
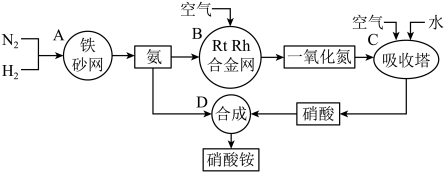
(1)在工业制硝酸的生产中,B中发生反应的化学方程式为_______ 。
(2)在合成硝酸的吸收塔中通入空气的目的是_______ 。
(3)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法: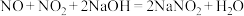
 还原法:_______
还原法:_______ +_______
+_______ =_______
=_______ +_______
+_______
①配平上述反应的化学方程式_______ 。
②以上两种方法中,更符合绿色化学的是_______ 。
③ 还原法中氧化产物和还原产物的物质的量之比为
还原法中氧化产物和还原产物的物质的量之比为_______ 。
(4)过量的铁与稀硝酸反应的离子方程式为_______ 。
(5)密度为1.40g/mL、质量分数为63%的浓硝酸的物质的量浓度为_______ 。

(1)在工业制硝酸的生产中,B中发生反应的化学方程式为
(2)在合成硝酸的吸收塔中通入空气的目的是
(3)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:
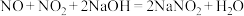
 还原法:_______
还原法:_______ +_______
+_______ =_______
=_______ +_______
+_______
①配平上述反应的化学方程式
②以上两种方法中,更符合绿色化学的是
③
 还原法中氧化产物和还原产物的物质的量之比为
还原法中氧化产物和还原产物的物质的量之比为(4)过量的铁与稀硝酸反应的离子方程式为
(5)密度为1.40g/mL、质量分数为63%的浓硝酸的物质的量浓度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】化合物X由四种常见元素组成,摩尔质量为100g/mol~150g/mol,其焰色反应为黄色,X的水溶液能使紫色石蕊试液变红色。取一定量的X进行下图实验:
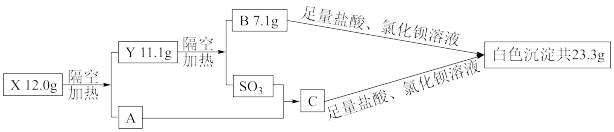
回答下列问题:
(1)X溶于水的电离方程式是____________________________________________________
(2)简述气体A的检验方法______________________________________________________
(3)Y→B+SO3的化学反应方程式___________________________________________________

回答下列问题:
(1)X溶于水的电离方程式是
(2)简述气体A的检验方法
(3)Y→B+SO3的化学反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】亚硫酰氯(SOCl2)又名氯化亚砜,是一种无色或淡黄色发烟液体,有强烈刺激性气味,常用作脱水剂,主要用于制造酰基氯化物,还用于医药、农药、染料等的生产。某实验小组设计实验制备氯化亚砜并探究其性质。
已知:①实验室制备原理为 。
。
②资料卡片:
实验一:制备并探究SOCl2的性质,制备SOCl2的装置如图(夹持装置已略去)。
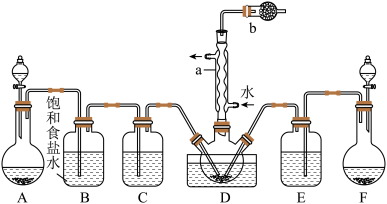
(1)a仪器的名称为_______ ,b装置的作用是_______ 。
(2) 可通过
可通过 固体与70%浓
固体与70%浓 反应制取,
反应制取, 可通过
可通过 固体与浓盐酸反应制取,则上图中制取
固体与浓盐酸反应制取,则上图中制取 的装置为
的装置为_______ (填字母)。
(3)将上述装置制得的SOCl2通过蒸馏方法提取出来(加热及夹持装置略),装置安装顺序为①⑨⑧_______ (填序号)。

(4)甲同学认为SOCl2可用作热分解 制取无水
制取无水 的脱水剂,反应的化学方程式为
的脱水剂,反应的化学方程式为_______ ;但乙同学认为该实验可能发生副反应使产品不纯,所以乙同学取少量 在不断通入SOCl2蒸气的条件下加热,充分反应后通入N2,加水溶解,取溶解后的溶液少许,加入
在不断通入SOCl2蒸气的条件下加热,充分反应后通入N2,加水溶解,取溶解后的溶液少许,加入_______ (填写试剂和实验现象),说明发生了副反应。
实验二:测定某SOCl2样品中SOCl2的纯度。
①准确称量称量瓶和盖的总质量 ,迅速加入
,迅速加入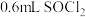 样品,立即盖紧,称量,质量为
样品,立即盖紧,称量,质量为 。
。
②连同称量瓶一起放入盛有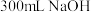 溶液的密封水解瓶中,盖紧并用蒸馏水封口,轻轻摇动,待称量瓶盖打开,将水解瓶放入冰水浴,浸泡水解1h后,将水解瓶中的溶液全部转移到
溶液的密封水解瓶中,盖紧并用蒸馏水封口,轻轻摇动,待称量瓶盖打开,将水解瓶放入冰水浴,浸泡水解1h后,将水解瓶中的溶液全部转移到 容量瓶中,洗涤水解瓶2~3次,洗涤液一并转入容量瓶中,静置至室温,定容,摇匀,得到溶液M。
容量瓶中,洗涤水解瓶2~3次,洗涤液一并转入容量瓶中,静置至室温,定容,摇匀,得到溶液M。
③准确量取 溶液M于
溶液M于 碘量瓶中,加入两滴指示剂,用
碘量瓶中,加入两滴指示剂,用 的盐酸中和过量的
的盐酸中和过量的 溶液至恰好完全。
溶液至恰好完全。
④准确加入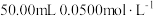 碘标准溶液,充分反应后,用淀粉溶液作指示剂,用
碘标准溶液,充分反应后,用淀粉溶液作指示剂,用 的
的 溶液滴定过量的碘,反应为
溶液滴定过量的碘,反应为 。平行测定两次,反应消耗
。平行测定两次,反应消耗 溶液的平均体积为
溶液的平均体积为 。
。
(5)判断滴定终点的方法为_______ ,样品中SOCl2的质量分数为_______ ;下列情况会导致测定的SOCl2的质量分数偏高的是_______ (填标号)。
A.实际碘标准溶液浓度偏低
B.实际 溶液浓度偏低
溶液浓度偏低
C.水解过程,气体吸收不充分,有部分气体逸出
D.滴定达终点时发现滴定管尖嘴内有气泡生成
已知:①实验室制备原理为
 。
。②资料卡片:
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
 |  | 76.1 | 137.5 | 遇水剧烈水解,易与 反应 反应 |
 | 1.25 | 105.8 | 153.5 | 遇水剧烈水解,能溶于 |
 | 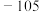 | 78.8 | 119 | 遇水剧烈水解,受热易分解 |

(1)a仪器的名称为
(2)
 可通过
可通过 固体与70%浓
固体与70%浓 反应制取,
反应制取, 可通过
可通过 固体与浓盐酸反应制取,则上图中制取
固体与浓盐酸反应制取,则上图中制取 的装置为
的装置为(3)将上述装置制得的SOCl2通过蒸馏方法提取出来(加热及夹持装置略),装置安装顺序为①⑨⑧

(4)甲同学认为SOCl2可用作热分解
 制取无水
制取无水 的脱水剂,反应的化学方程式为
的脱水剂,反应的化学方程式为 在不断通入SOCl2蒸气的条件下加热,充分反应后通入N2,加水溶解,取溶解后的溶液少许,加入
在不断通入SOCl2蒸气的条件下加热,充分反应后通入N2,加水溶解,取溶解后的溶液少许,加入实验二:测定某SOCl2样品中SOCl2的纯度。
①准确称量称量瓶和盖的总质量
 ,迅速加入
,迅速加入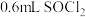 样品,立即盖紧,称量,质量为
样品,立即盖紧,称量,质量为 。
。②连同称量瓶一起放入盛有
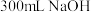 溶液的密封水解瓶中,盖紧并用蒸馏水封口,轻轻摇动,待称量瓶盖打开,将水解瓶放入冰水浴,浸泡水解1h后,将水解瓶中的溶液全部转移到
溶液的密封水解瓶中,盖紧并用蒸馏水封口,轻轻摇动,待称量瓶盖打开,将水解瓶放入冰水浴,浸泡水解1h后,将水解瓶中的溶液全部转移到 容量瓶中,洗涤水解瓶2~3次,洗涤液一并转入容量瓶中,静置至室温,定容,摇匀,得到溶液M。
容量瓶中,洗涤水解瓶2~3次,洗涤液一并转入容量瓶中,静置至室温,定容,摇匀,得到溶液M。③准确量取
 溶液M于
溶液M于 碘量瓶中,加入两滴指示剂,用
碘量瓶中,加入两滴指示剂,用 的盐酸中和过量的
的盐酸中和过量的 溶液至恰好完全。
溶液至恰好完全。④准确加入
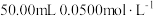 碘标准溶液,充分反应后,用淀粉溶液作指示剂,用
碘标准溶液,充分反应后,用淀粉溶液作指示剂,用 的
的 溶液滴定过量的碘,反应为
溶液滴定过量的碘,反应为 。平行测定两次,反应消耗
。平行测定两次,反应消耗 溶液的平均体积为
溶液的平均体积为 。
。(5)判断滴定终点的方法为
A.实际碘标准溶液浓度偏低
B.实际
 溶液浓度偏低
溶液浓度偏低C.水解过程,气体吸收不充分,有部分气体逸出
D.滴定达终点时发现滴定管尖嘴内有气泡生成
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】 氯丙酸(CH3CHClCOOH)主要用于生产农药除草剂,还用于生产乳酸及有工业价值的低级醇酯。如图为实验室制备
氯丙酸(CH3CHClCOOH)主要用于生产农药除草剂,还用于生产乳酸及有工业价值的低级醇酯。如图为实验室制备 氯丙酸的装置。
氯丙酸的装置。


已知:相关物质的物理性质如下表所示:
制备方法:在三颈烧瓶中放置148g (2mol)丙酸和1.5g三氯化磷 作催化剂
作催化剂 ,加热至
,加热至 ,缓慢通入氯气,保持温度在
,缓慢通入氯气,保持温度在 之间大约反应
之间大约反应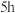 。
。
回答下列问题:
(1)A装置中反应的离子方程式为_____________________________________________ ,当生成6.72LCl2(标准状况)时,转移电子的数目为________________ 。
(2)某同学分析发现D装置有两处缺陷,分别是_____________ 、________________ 。
(3)测定产品纯度。
步骤Ⅰ:称取1.20g样品(杂质不含PCl3)于烧瓶中,加入100.00mL 4mol/L氢氧化钠溶液共热,冷却至室温。加入100.00mL 4mol/L硝酸,一段时间后,将烧瓶中的溶液全部转移至250mL容量瓶中,加水定容(溶液中为乳酸和NaCl)。
步骤Ⅱ:从容量瓶中各取50.00mL溶液于锥形瓶中,用Na2CrO4作指示剂,用0.2000mol/LAgNO3溶液分别滴定溶液中的Cl—(已知:Ag2CrO4为砖红色沉淀、乳酸银不沉淀),平行三次实验,所得滴定数据如表所示:
①加入硝酸的目的是_______________________________________ 。
②步骤Ⅱ操作中,达到滴定终点的现象是________________________ 。
③样品中 氯丙酸的质量分数为
氯丙酸的质量分数为__________  保留三位有效数字
保留三位有效数字 。
。
 氯丙酸(CH3CHClCOOH)主要用于生产农药除草剂,还用于生产乳酸及有工业价值的低级醇酯。如图为实验室制备
氯丙酸(CH3CHClCOOH)主要用于生产农药除草剂,还用于生产乳酸及有工业价值的低级醇酯。如图为实验室制备 氯丙酸的装置。
氯丙酸的装置。 

已知:相关物质的物理性质如下表所示:
| 物质 | 熔点 | 沸点 | 溶解性 |
 氯丙酸 氯丙酸 | 14 | 190 | 能与水、乙醇互溶 |
| 丙酸 | 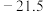 | 141 | 能与水、乙醇互溶 |
| PCl3 | 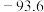 |  | 与水剧烈反应,能溶于乙醇 |
 作催化剂
作催化剂 ,加热至
,加热至 ,缓慢通入氯气,保持温度在
,缓慢通入氯气,保持温度在 之间大约反应
之间大约反应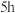 。
。回答下列问题:
(1)A装置中反应的离子方程式为
(2)某同学分析发现D装置有两处缺陷,分别是
(3)测定产品纯度。
步骤Ⅰ:称取1.20g样品(杂质不含PCl3)于烧瓶中,加入100.00mL 4mol/L氢氧化钠溶液共热,冷却至室温。加入100.00mL 4mol/L硝酸,一段时间后,将烧瓶中的溶液全部转移至250mL容量瓶中,加水定容(溶液中为乳酸和NaCl)。
步骤Ⅱ:从容量瓶中各取50.00mL溶液于锥形瓶中,用Na2CrO4作指示剂,用0.2000mol/LAgNO3溶液分别滴定溶液中的Cl—(已知:Ag2CrO4为砖红色沉淀、乳酸银不沉淀),平行三次实验,所得滴定数据如表所示:
| 实验序号 实验数据 | 第一次 | 第二次 | 第三次 | |
AgNO3溶液体积读数 | 滴定前 | 0 | 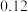 | 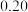 |
| 滴定后 | 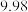 |  |  | |
②步骤Ⅱ操作中,达到滴定终点的现象是
③样品中
 氯丙酸的质量分数为
氯丙酸的质量分数为 保留三位有效数字
保留三位有效数字 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】浓硫酸和木炭在加热条件下发生反应。下图所示装置可用来检验浓硫酸与木炭在加热条件下反应产生的气体产物。

(1)浓硫酸与木炭反应的化学方程式为____________________ 。
(2)装置B中试剂的作用是___________ 。
(3)能证明装置中存在CO2的现象是___________ 。
(4)将木炭与浓硫酸共热后得到的气体通入下列溶液中,得不到无色澄清溶液的是_________ (填序号)。
A.品红溶液 B.滴加酚酞的氨水 C.Ba(OH)2溶液 D. 溴水
(5)若实验检验出有SO2生成,则相应的实验现象为:________________________ 。

(1)浓硫酸与木炭反应的化学方程式为
(2)装置B中试剂的作用是
(3)能证明装置中存在CO2的现象是
(4)将木炭与浓硫酸共热后得到的气体通入下列溶液中,得不到无色澄清溶液的是
A.品红溶液 B.滴加酚酞的氨水 C.Ba(OH)2溶液 D. 溴水
(5)若实验检验出有SO2生成,则相应的实验现象为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
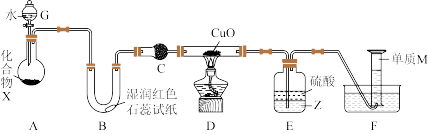
【推荐2】人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
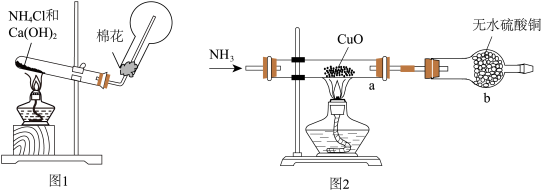
I.实验室制取氨气。
(1)图1装置中生成 的化学方程式为
的化学方程式为__________________________________________ 。检验圆底烧瓶中已收集满氨气的方法是__________________________________________ 。
II.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
(2)无水硫酸铜的作用是_____________________ ;有同学认为需要在无水硫酸铜的后面再接一个装有 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是_____________________ 。
(3)实验中观察到a中CuO粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为_________________________________ 。
(4)若a中消耗标准状况下3.36L的氨气,理论得到铜的质量为______________ g。

I.实验室制取氨气。
(1)图1装置中生成
 的化学方程式为
的化学方程式为II.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
(2)无水硫酸铜的作用是
 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是(3)实验中观察到a中CuO粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
(4)若a中消耗标准状况下3.36L的氨气,理论得到铜的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某学习小组按如图所示的甲、乙两种实验方案制备碘:
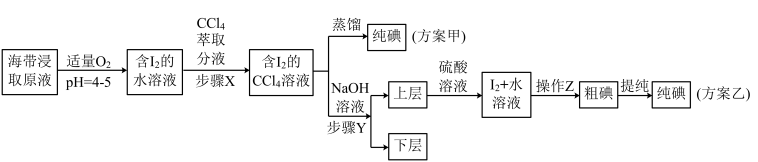
已知: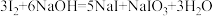 。
。
请回答下列问题:
(1)分液漏斗使用前须检漏,检漏方法为_____________ 。
(2)步骤X中,萃取后分液漏斗内观察到的现象是_________ 。
(3)下列有关步骤Y的说法,正确的是_____ (填标号,双选)。
A 应控制NaOH溶液的浓度和体积
B 将碘转化成离子进入水层
C 主要是除去海带浸取原液中的有机杂质
D NaOH溶液可以由乙醇代替
(4)操作Z的名称是_______ 。
(5)方案甲中采用蒸馏不合理,理由是_____________ 。

已知:
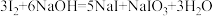 。
。请回答下列问题:
(1)分液漏斗使用前须检漏,检漏方法为
(2)步骤X中,萃取后分液漏斗内观察到的现象是
(3)下列有关步骤Y的说法,正确的是
A 应控制NaOH溶液的浓度和体积
B 将碘转化成离子进入水层
C 主要是除去海带浸取原液中的有机杂质
D NaOH溶液可以由乙醇代替
(4)操作Z的名称是
(5)方案甲中采用蒸馏不合理,理由是
您最近一年使用:0次



