回答下列问题:
(1)标况下等质量的O2与O3的体积之比为_______ ,氧原子个数之比为_______ 。
(2)1.7gH2O2中含有O原子的物质的量为_______ ,质子数目为_______ ,已知agH2O2中含原子数为b,则阿伏加德罗常数数值为_______ (用含a、b的代数式表示)
(3)12.4 g Na2X中含有0.4 mol Na+,则Na2X的摩尔质量是_______ , X的相对原子质量是_______ 。
(1)标况下等质量的O2与O3的体积之比为
(2)1.7gH2O2中含有O原子的物质的量为
(3)12.4 g Na2X中含有0.4 mol Na+,则Na2X的摩尔质量是
更新时间:2021-10-15 21:31:54
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】标准状况下有以下四种气体:①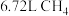 ;②
;② 个HBr分子 ;③
个HBr分子 ;③ ;④
;④ 。回答下列问题:
。回答下列问题:
(1) 与
与_______ g O2的物质的量相同。
(2)标准状况下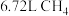 分子中所含氢原子数为
分子中所含氢原子数为_______ 个,与_______ 个 分子中所含氢原子数相等。
分子中所含氢原子数相等。
(3)以上四种气体中,密度最大的是_______ (填序号,下同),体积由小到大的顺序是_______ 。
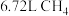 ;②
;② 个HBr分子 ;③
个HBr分子 ;③ ;④
;④ 。回答下列问题:
。回答下列问题:(1)
 与
与(2)标准状况下
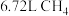 分子中所含氢原子数为
分子中所含氢原子数为 分子中所含氢原子数相等。
分子中所含氢原子数相等。(3)以上四种气体中,密度最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有14.4 g CO和CO2的混合气体,在标准状况下,其体积为8.96 L。回答下列问题:
(1)该混合气体的平均摩尔质量为________________ 。
(2)混合气体中碳原子的个数为______________ (用NA表示阿伏加 德罗常数的值)。
(3)将混合气体依次通过如图所示装置,剩余气体最后收集在气球中(实验在标准状况下测定)。

①气球中收集到的气体中,电子总数为________ (用NA表示阿伏加 德罗常数的值)。
②气球的体积为________ L。
(1)该混合气体的平均摩尔质量为
(2)混合气体中碳原子的个数为
(3)将混合气体依次通过如图所示装置,剩余气体最后收集在气球中(实验在标准状况下测定)。

①气球中收集到的气体中,电子总数为
②气球的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题:
(1)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比为__________ ;
(2)同质量的氨气和硫化氢气体在相同条件下的体积比为________ ,其中含有的氢原子数目比为________ ;
(3)若氨气和硫化氢(H2S)气体的氢原子数相等,则它们在相同条件下的体积比为________ 。
(4)由氨气和氢气组成的混合气体的平均相对分子质量为14,则氨气与氢气的物质的量为:________ 。
(1)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比为
(2)同质量的氨气和硫化氢气体在相同条件下的体积比为
(3)若氨气和硫化氢(H2S)气体的氢原子数相等,则它们在相同条件下的体积比为
(4)由氨气和氢气组成的混合气体的平均相对分子质量为14,则氨气与氢气的物质的量为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)147gH2SO4的物质的量是_______ ;
(2)氧化铜在高温下发生分解反应:4CuO 2Cu2O +O2↑,若反应过程中生成1molO2分子,则转移电子数为
2Cu2O +O2↑,若反应过程中生成1molO2分子,则转移电子数为________ mol。
(3)反应:2FeCl3+2KI=2FeCl2+2KCl+I2,其中_____ 元素化合价升高,则该元素被_____ ,_____ 元素化合价降低;______ 作还原剂,_____ 发生还原反应。
(4)钠在空气中燃烧的化学方程式:_____ ,1mol钠完全燃烧转移电子的个数为______ (阿伏加 德罗常数为NA)。
(2)氧化铜在高温下发生分解反应:4CuO
 2Cu2O +O2↑,若反应过程中生成1molO2分子,则转移电子数为
2Cu2O +O2↑,若反应过程中生成1molO2分子,则转移电子数为(3)反应:2FeCl3+2KI=2FeCl2+2KCl+I2,其中
(4)钠在空气中燃烧的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】过二硫酸盐[例:(NH4)2S2O8、Na2S2O8]都具有强氧化性,可作为氧化剂和漂白剂,(NH4)2S2O8被广泛用于蓄电池工业,在照相工业上用来除去海波。
I.(NH4)2S2O8的制备原理为H2O2+2H2SO4+2NH3=(NH4)2S2O8+2H2O。实验室模拟制备(NH4)2S2O8的装置如图所示。
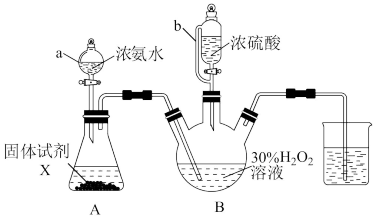
(1)仪器a的名称是________ 。
(2)充分反应后,将B中混合液经一系列操作得到晶体,用无水乙醚洗涤,目的是______ 。
(3)烘干产品时,用红外灯低温供干,可能的原因是_______ 。
II.(NH4)2S2O8的性质及应用。
(4)过二硫酸(H2S2O8)是一种强氧化性酸,在Ag+催化作用下, 能与Mn2+在水溶液中发生反应生成
能与Mn2+在水溶液中发生反应生成 和
和 ,1mol
,1mol 能氧化的Mn2+的物质的量为
能氧化的Mn2+的物质的量为_____ mol。过二硫酸铵可用于检验废水中的Cr3+是否超标,如果超标,溶液会变成橙色(还原产物为 ),写出该反应的离子方程式
),写出该反应的离子方程式______ 。
III.标定(NH4)2S2O8溶液的浓度。
(5)称取一定质量的(NH4)2S2O8,配制成溶液,并用碘量法标定该溶液的浓度,移取20.00mL(NH4)2S2O8溶液于锥形瓶中,加入过量的KI,然后加入几滴淀粉溶液,再用0.1mol·L-1的Na2S2O3溶液滴定,发生反应:I2+2 =2I-+
=2I-+ 。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为
。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为______ ,所标定的(NH4)2S2O8的浓度为________ mol∙L-1。
I.(NH4)2S2O8的制备原理为H2O2+2H2SO4+2NH3=(NH4)2S2O8+2H2O。实验室模拟制备(NH4)2S2O8的装置如图所示。

(1)仪器a的名称是
(2)充分反应后,将B中混合液经一系列操作得到晶体,用无水乙醚洗涤,目的是
(3)烘干产品时,用红外灯低温供干,可能的原因是
II.(NH4)2S2O8的性质及应用。
(4)过二硫酸(H2S2O8)是一种强氧化性酸,在Ag+催化作用下,
 能与Mn2+在水溶液中发生反应生成
能与Mn2+在水溶液中发生反应生成 和
和 ,1mol
,1mol 能氧化的Mn2+的物质的量为
能氧化的Mn2+的物质的量为 ),写出该反应的离子方程式
),写出该反应的离子方程式III.标定(NH4)2S2O8溶液的浓度。
(5)称取一定质量的(NH4)2S2O8,配制成溶液,并用碘量法标定该溶液的浓度,移取20.00mL(NH4)2S2O8溶液于锥形瓶中,加入过量的KI,然后加入几滴淀粉溶液,再用0.1mol·L-1的Na2S2O3溶液滴定,发生反应:I2+2
 =2I-+
=2I-+ 。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为
。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为
您最近一年使用:0次

 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是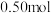 异丁烷分子中共价键的数目为
异丁烷分子中共价键的数目为
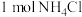 含有的共价键数目为
含有的共价键数目为

 含
含 键数目为
键数目为
 乙烷和丙烯的混合气体中所含碳氢键数为
乙烷和丙烯的混合气体中所含碳氢键数为
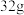 环状
环状 (
( )分子中含有的
)分子中含有的 键数为
键数为


