 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.(2023·全国卷)
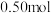 异丁烷分子中共价键的数目为
异丁烷分子中共价键的数目为
B.(2023·广东卷)
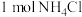 含有的共价键数目为
含有的共价键数目为
C.(2023·湖北卷)1molSi含Si-Si键的数目约为

D.(2023·辽宁卷)
 含
含 键数目为
键数目为
E.(2022·浙江卷)32g甲醇的分子中含有C—H键的数目为4NA
F.(2022·浙江卷)
 乙烷和丙烯的混合气体中所含碳氢键数为
乙烷和丙烯的混合气体中所含碳氢键数为
G.(2021·全国卷)
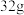 环状
环状 (
(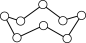 )分子中含有的
)分子中含有的 键数为
键数为
2024高三·全国·专题练习 查看更多[1]
(已下线)题型02 阿伏加德罗常数的判断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
更新时间:2024-01-06 08:11:20
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】11.2g铁的物质的量为_______ mol;标准状况下,2molCl2的体积是_______ L;0.2molN2中含有的分子数约为_______ 个;5L0.4mol·L-1NaOH溶液中含有_______ molNa+。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】10 g 46%的乙醇水溶液所含氢原子的数目为0.6NA___
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应是一类重要的化学反应,广泛存在于生产和生活中。对我们的生产和生活中可能同时具有正负两方面的影响,如果我们能够掌握化学变化的规律,就有可能做到趋利避害,使之更好地为社会的发展服务。
(1)黑火药是我国古代的四大发明之一、黑火药着火时,发生如下氧化还原反应: 。在此反应中,还原产物是
。在此反应中,还原产物是___________ (填化学式),当该反应转移 电子时,产生气体的体积为
电子时,产生气体的体积为___________ L(标况下)。
(2)汽车剧烈碰撞时,安全气囊中发生反应: 。在此反应中,氧化剂是
。在此反应中,氧化剂是___________ (填化学式);氧化产物是___________ (填化学式);若反应得到的氧化产物比还原产物多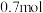 ,则此过程中转移电子的物质的量为
,则此过程中转移电子的物质的量为___________ mol。
(3)葡萄糖氧化反应( )放出的热量是人体生命活动所需能量的重要来源。医学上葡萄糖溶液可作为药物的溶媒,同时能给病人补充体液和能量。
)放出的热量是人体生命活动所需能量的重要来源。医学上葡萄糖溶液可作为药物的溶媒,同时能给病人补充体液和能量。
①葡萄糖是___________ (填“强电解质”或“弱电解质”或“非电解质”或“都不是”)。
②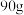 葡萄糖在人体内完全氧化供能,理论上需要消耗标准状况下的
葡萄糖在人体内完全氧化供能,理论上需要消耗标准状况下的
___________ L。
③人体血糖(血液中的葡萄糖)正常值为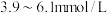 。某人体检报告血糖值为
。某人体检报告血糖值为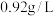 的血糖
的血糖___________ (填“偏高”“正常”或“偏低”)。
(1)黑火药是我国古代的四大发明之一、黑火药着火时,发生如下氧化还原反应:
 。在此反应中,还原产物是
。在此反应中,还原产物是 电子时,产生气体的体积为
电子时,产生气体的体积为(2)汽车剧烈碰撞时,安全气囊中发生反应:
 。在此反应中,氧化剂是
。在此反应中,氧化剂是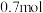 ,则此过程中转移电子的物质的量为
,则此过程中转移电子的物质的量为(3)葡萄糖氧化反应(
 )放出的热量是人体生命活动所需能量的重要来源。医学上葡萄糖溶液可作为药物的溶媒,同时能给病人补充体液和能量。
)放出的热量是人体生命活动所需能量的重要来源。医学上葡萄糖溶液可作为药物的溶媒,同时能给病人补充体液和能量。①葡萄糖是
②
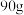 葡萄糖在人体内完全氧化供能,理论上需要消耗标准状况下的
葡萄糖在人体内完全氧化供能,理论上需要消耗标准状况下的
③人体血糖(血液中的葡萄糖)正常值为
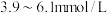 。某人体检报告血糖值为
。某人体检报告血糖值为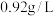 的血糖
的血糖
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据所学知识,回答下列问题:
(1)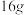 由O2和O3组成的混合气体中氧原子的数目为
由O2和O3组成的混合气体中氧原子的数目为______________ .
(2) 中所含的氢原子数与
中所含的氢原子数与__________ 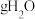 中所含的氢原子数相等.
中所含的氢原子数相等.
(3)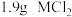 中含
中含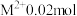 ,则
,则 的摩尔质量为
的摩尔质量为__________ ,M的相对原子质量为__________ .
(4)标准状况下, 由二氧化碳和一氧化碳组成的混合气体,其体积为
由二氧化碳和一氧化碳组成的混合气体,其体积为 ,若将此混合气体通入足量的澄清石灰水中,则生成沉淀的质量为
,若将此混合气体通入足量的澄清石灰水中,则生成沉淀的质量为______________ g.
(1)
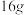 由O2和O3组成的混合气体中氧原子的数目为
由O2和O3组成的混合气体中氧原子的数目为(2)
 中所含的氢原子数与
中所含的氢原子数与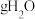 中所含的氢原子数相等.
中所含的氢原子数相等.(3)
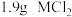 中含
中含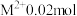 ,则
,则 的摩尔质量为
的摩尔质量为(4)标准状况下,
 由二氧化碳和一氧化碳组成的混合气体,其体积为
由二氧化碳和一氧化碳组成的混合气体,其体积为 ,若将此混合气体通入足量的澄清石灰水中,则生成沉淀的质量为
,若将此混合气体通入足量的澄清石灰水中,则生成沉淀的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在H2O、NH3、CS2、CH4、BF3分子中:
(1)存在π键的共价化合物分子是_______ (填分子式,下同)。
(2)具有直线形结构的分子是_______ 。
(3)具有正四面体形结构的分子是_______ 。
(4)具有三角锥形结构的分子是_______ 。
(5)具有sp2杂化轨道类型的分子是_______ 。
(6)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ 。OF2分子的空间构型为_______ 。
(1)存在π键的共价化合物分子是
(2)具有直线形结构的分子是
(3)具有正四面体形结构的分子是
(4)具有三角锥形结构的分子是
(5)具有sp2杂化轨道类型的分子是
(6)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】三乙酸锰([Mn(CH3COO)3])是一种锰的配合物,在有机合成中有重要的应用价值。CH3COO―为该配合物的配体,其所含元素的电负性最大的是___________ ;FCH2COO-、ClCH2COO-也可作为配体使用,相同条件下,FCH2COO-、ClCH2COO-结合H+的能力较强的是___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】过氧化氢(H2O2)为淡蓝色粘稠液体,是中学常见试剂。
(1)H2O2含有的共价键类型为___________________ 。
(2)H2O2能与水任意比混合,且纯净的H2O2具有较高的沸点,这可能与H2O2与水以及H2O2分子间能形成_________ 有关。
(3)实验室可用稀硫酸与BaO2反应来制取H2O2,该反应的化学方程式为:________________
(4)经测定H2O2为二元弱酸,酸性比碳酸还弱,不稳定易分解。已知Na2O2中通入干燥的CO2不反应,但通入潮湿的CO2却可以产O2,试用化学方程式表示这一过程:__________________ 。
(5)现有一份H2O2溶液,某学习小组想测定其浓度,查阅资料得知方法如下:用移液管吸取10.00mL的H2O2样品,置于l00mL)容量瓶中,加水稀释至刻度线,取25.00mL溶液置于锥形瓶再加入l0mL 3mol/L的稀硫酸(过量),用0.02mol/L的标准浓度的KMnO4溶液滴定,所用体积为20.00mL,则上述滴定过程发生的离子反应方程式为:___________ ,原H2O2溶液的浓度为____________ g/L。
(1)H2O2含有的共价键类型为
(2)H2O2能与水任意比混合,且纯净的H2O2具有较高的沸点,这可能与H2O2与水以及H2O2分子间能形成
(3)实验室可用稀硫酸与BaO2反应来制取H2O2,该反应的化学方程式为:
(4)经测定H2O2为二元弱酸,酸性比碳酸还弱,不稳定易分解。已知Na2O2中通入干燥的CO2不反应,但通入潮湿的CO2却可以产O2,试用化学方程式表示这一过程:
(5)现有一份H2O2溶液,某学习小组想测定其浓度,查阅资料得知方法如下:用移液管吸取10.00mL的H2O2样品,置于l00mL)容量瓶中,加水稀释至刻度线,取25.00mL溶液置于锥形瓶再加入l0mL 3mol/L的稀硫酸(过量),用0.02mol/L的标准浓度的KMnO4溶液滴定,所用体积为20.00mL,则上述滴定过程发生的离子反应方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】二草酸根合铜(II)酸钾 可用于无机合成、功能材料制备。回答下列有关问题:
可用于无机合成、功能材料制备。回答下列有关问题:
(1)基态氧原子的电子排布式为_______ ,以下氧原子的激发态中能量最高的是_______ (填字母)。
a.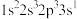 b.
b. c.
c.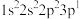
(2)二草酸根合铜(II)酸钾是一种配合物。
①其中配位体的化学式是_______ ,配位原子是氧而不是碳的原因是_______ 。
②草酸分子的结构为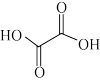 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为_______ , 草酸分子中含有的
草酸分子中含有的 键数目为
键数目为_______ (阿伏加德罗常数的值为 ),
), 键能大于
键能大于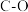 键能的判断依据是
键能的判断依据是_______ 。
 可用于无机合成、功能材料制备。回答下列有关问题:
可用于无机合成、功能材料制备。回答下列有关问题:(1)基态氧原子的电子排布式为
a.
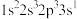 b.
b. c.
c.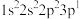
(2)二草酸根合铜(II)酸钾是一种配合物。
①其中配位体的化学式是
②草酸分子的结构为
 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为 草酸分子中含有的
草酸分子中含有的 键数目为
键数目为 ),
), 键能大于
键能大于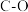 键能的判断依据是
键能的判断依据是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是_______ 、_______ 。
(2)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是_________ 、中心原子的杂化形式为_________ 。
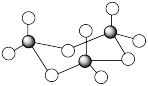
(3)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是___________ ,气态三氧化硫以单分子形式存在,其分子的立体构型为___________ 形;固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为___________ 。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为___________ ,C原子的杂化形式为___________ 。
(2)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是
(3)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是

(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】该反应曾用于检测司机是否酒后驾驶:2Cr2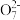 +3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH
(1)基态Cr3+的核外电子排布式为_______ ;配合离子[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是_______ (填元素符号)。
(2)CH3COOH中C原子的杂化轨道类型为_______ 和_______ ;1molCH3COOH分子中含有σ键的数目为_______ 。
(3)H2O与CH3CH2OH可以任意比例互溶,原因是_______ 、_______ (回答两点)。
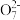 +3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O=4[Cr(H2O)6]3++3CH3COOH(1)基态Cr3+的核外电子排布式为
(2)CH3COOH中C原子的杂化轨道类型为
(3)H2O与CH3CH2OH可以任意比例互溶,原因是
您最近一年使用:0次

 分子中所含原子数与
分子中所含原子数与 和
和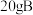 恰好完全反应生成
恰好完全反应生成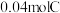 和
和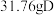 ,则C的摩尔质量为
,则C的摩尔质量为 和
和 中所含有的电子数之比为
中所含有的电子数之比为 反应转移的电子数为
反应转移的电子数为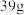
 中
中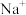 的数目为
的数目为 个水分子的质量为
个水分子的质量为 混合气体6.72L,其质量为10g,则此混合气体中,CO和
混合气体6.72L,其质量为10g,则此混合气体中,CO和 中N原子的物质的量为0.2mol,则x的数值为
中N原子的物质的量为0.2mol,则x的数值为

