按要求填写下列空格。
(1)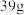
 中
中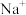 的数目为
的数目为_______ 。
(2) 个水分子的质量为
个水分子的质量为_______ g。
(3)现有标准状况下CO和 混合气体6.72L,其质量为10g,则此混合气体中,CO和
混合气体6.72L,其质量为10g,则此混合气体中,CO和 的物质的量之比是
的物质的量之比是_______ 。
(4)9.2g氮的氧化物 中N原子的物质的量为0.2mol,则x的数值为
中N原子的物质的量为0.2mol,则x的数值为_______ 。
(1)
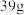
 中
中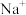 的数目为
的数目为(2)
 个水分子的质量为
个水分子的质量为(3)现有标准状况下CO和
 混合气体6.72L,其质量为10g,则此混合气体中,CO和
混合气体6.72L,其质量为10g,则此混合气体中,CO和 的物质的量之比是
的物质的量之比是(4)9.2g氮的氧化物
 中N原子的物质的量为0.2mol,则x的数值为
中N原子的物质的量为0.2mol,则x的数值为
更新时间:2022-11-24 18:16:46
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在标准状况下,某气体密度为2.86g/L,则其相对分子质量为____ 。(取整数值)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】物质的量是联系宏观和微观的桥梁,也是定量研究化学的基础。
Ⅰ.甲烷(CH4)是一种无色无味的气体,是天然气的主要成分。
(1)现有2 mol CH4,它的摩尔质量是_______ ,要把CH4完全燃烧,消耗氧气_______ g。
(2)标准状况下,CH4的密度为_______ (保留3位有效数字)。如果11.2 L CH4中含有x个氢原子,则阿伏加德罗常数的值为_______ 。
(3)相同温度和压强下,质量相等的氢气和甲烷,它们的体积之比为_______ ,密度之比为_______ 。若把质量相等的这两种气体混合,则混合气体的平均相对分子质量为_______ (保留2位有效数字)。
(4)某沼气成分是CH4和CO2.取2 L该沼气与4 L O2点燃充分反应后,除去水分,剩余气体的体积为3 L。该沼气中CH4和CO2的物质的量之比为_______ (气体体积均在同温同压下测定)。
Ⅱ.溶液中所含溶质的多少可用不同的浓度来表示。
(5)下列各溶液中,Na+ 浓度最小的是_______
(6)98%的浓硫酸(密度为1.84 g·mL-1),可采取不同的形式表示。以下根据表示方法的定义,错误 的是_______
Ⅰ.甲烷(CH4)是一种无色无味的气体,是天然气的主要成分。
(1)现有2 mol CH4,它的摩尔质量是
(2)标准状况下,CH4的密度为
(3)相同温度和压强下,质量相等的氢气和甲烷,它们的体积之比为
(4)某沼气成分是CH4和CO2.取2 L该沼气与4 L O2点燃充分反应后,除去水分,剩余气体的体积为3 L。该沼气中CH4和CO2的物质的量之比为
Ⅱ.溶液中所含溶质的多少可用不同的浓度来表示。
(5)下列各溶液中,Na+ 浓度最小的是_______
| A.4L 0.5 mol·L-1 NaCl 溶液 | B.1L 0.3 mol·L-1 Na2SO4 溶液 |
| C.8L 0.4 mol·L-1 NaOH 溶液 | D.2L 0.15 mol·L-1 Na3PO4 溶液 |
| A.物质的量浓度:单位体积溶液中含溶质的物质的量:18.4 mol·L-1 |
| B.质量浓度:单位体积溶液中含溶质的质量:1.84 kg·L-1 |
C.把浓硫酸当作硫酸的水合物,用化学式表示:H2SO4·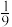 H2O H2O |
D.把浓硫酸当作复合氧化物,用化学式表示:SO3· H2O H2O |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有mgX元素的单质气体 (其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:
(其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:
(1)该气体的物质的量为___________ mol。
(2)该气体所含原子总数为___________ 。
(3)该气体在标准状况下的体积为___________ L。
(4)该气体全部溶于1L水中(不考虑与水反应,水的密度为1g/cm3),其溶液中溶质的质量分数为___________ 。
(5)X元素的另一单质气体 与
与 的关系是
的关系是___________ 。mg 气体的物质的量为
气体的物质的量为___________ mol,所含原子总数为___________ 。
 (其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:
(其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:(1)该气体的物质的量为
(2)该气体所含原子总数为
(3)该气体在标准状况下的体积为
(4)该气体全部溶于1L水中(不考虑与水反应,水的密度为1g/cm3),其溶液中溶质的质量分数为
(5)X元素的另一单质气体
 与
与 的关系是
的关系是 气体的物质的量为
气体的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】用NA表示阿伏伽德罗常数的数值。请回答下列问题:
(1)0.5mol SO2共含有约_______ 个原子,它与_______ g SO3所含硫原子数相等。
(2)质量相同的①HCl、②NH3、③CO2、④O2四种气体中,在同温同压条件下,所占体积最小的是(填序号)___________ 。
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是_____ ;
(4)标准状况下某种O2和N2的混合气体m g,含有b个分子,则n g该混合气体在相同状况下所占的体积应是___________ 。
(1)0.5mol SO2共含有约
(2)质量相同的①HCl、②NH3、③CO2、④O2四种气体中,在同温同压条件下,所占体积最小的是(填序号)
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是
(4)标准状况下某种O2和N2的混合气体m g,含有b个分子,则n g该混合气体在相同状况下所占的体积应是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。能导电的是_______ ;(填序号,下同)属于电解质的是_______ ;属于非电解质的是_______ 。
(2)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常见的消毒药品:84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。回答下面问题:
①38g过氧乙酸(CH3COOOH)中含有的O原子数为_______ NA(设NA代表阿伏加德罗常数的值),含有的H原子的物质的量为_______ 。
②40.5g某金属氯化物MCl2中含有0.6molCl-,则该金属氯化物的摩尔质量为_______ 。
③NaClO可通过Cl2跟NaOH溶液反应制得,该反应的离子方程式为:_______ 。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。能导电的是
(2)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常见的消毒药品:84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。回答下面问题:
①38g过氧乙酸(CH3COOOH)中含有的O原子数为
②40.5g某金属氯化物MCl2中含有0.6molCl-,则该金属氯化物的摩尔质量为
③NaClO可通过Cl2跟NaOH溶液反应制得,该反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】填写下列空白:
(1)要使NH3与CH4含相同数目的H原子,则NH3和CH4的质量之比为______ 。
(2)标准状况下,密度为0.75g·L−1的NH3与CH4组成的混合气体中,NH3的体积分数为______ 。
(3)某结晶水合物的化学式为A·nH2O,A的相对分子质量为M。如将ag该结晶水合物加热至结晶水全部失去,剩余的残渣为bg,则n=______ 。
(4)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mLA受热完全分解生成15mLO2和10mLF2,则A的化学式为_____ 。
(5)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为______ 。
(6)一氧化碳和二氧化碳的混合气体18g,完全燃烧后测得二氧化碳的体积为11.2L(标准状况),混合气体中二氧化碳在标准状况下的体积是______ 。
(1)要使NH3与CH4含相同数目的H原子,则NH3和CH4的质量之比为
(2)标准状况下,密度为0.75g·L−1的NH3与CH4组成的混合气体中,NH3的体积分数为
(3)某结晶水合物的化学式为A·nH2O,A的相对分子质量为M。如将ag该结晶水合物加热至结晶水全部失去,剩余的残渣为bg,则n=
(4)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mLA受热完全分解生成15mLO2和10mLF2,则A的化学式为
(5)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为
(6)一氧化碳和二氧化碳的混合气体18g,完全燃烧后测得二氧化碳的体积为11.2L(标准状况),混合气体中二氧化碳在标准状况下的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】航天飞机释放出的CO2通过含有LiOH(LiOH与NaOH的化学性质相似)的滤毒罐而被除去,完成下列问题:
(1)CO2与足量LiOH反应的化学方程式为___________ ,该化学反应的类型为___________ 反应(填“复分解”,“非氧化还原”或“氧化还原”)。
(2)若有标况下4.48×104L的CO2被足量的LiOH吸收,则消耗LiOH___________ 克。(写出具体解题过程)
(1)CO2与足量LiOH反应的化学方程式为
(2)若有标况下4.48×104L的CO2被足量的LiOH吸收,则消耗LiOH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】填空题。请完成以下有关计算:
(1)标准状况下,m g A气体与n g B气体分子数相等,25℃时,1 kg气体A与1 kg气体B的分子数之比为________ 。
(2)m g某M溶于盐酸中,放出的气体在标准状况下的体积为n L,并生成氯化物MCl2,则金属M的相对原子质量是________ 。
(3)如图有三只气球,其中VA=VB=1.12 L。

①A、B中气体的物质的量____ (填“一定”或“不一定”)是0.05 mol。
②标准状况下,A、B气球中的分子个数比为_________ 。
③相同温度和压强下,A、C气球中气体的质量相等,则V(A)∶V(C)=__________
(4)取100 mL 0.3 mol·L-1和300 mL 0.25 mol·L-1的硫酸注入500 mL容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是________ 。
(1)标准状况下,m g A气体与n g B气体分子数相等,25℃时,1 kg气体A与1 kg气体B的分子数之比为
(2)m g某M溶于盐酸中,放出的气体在标准状况下的体积为n L,并生成氯化物MCl2,则金属M的相对原子质量是
(3)如图有三只气球,其中VA=VB=1.12 L。

①A、B中气体的物质的量
②标准状况下,A、B气球中的分子个数比为
③相同温度和压强下,A、C气球中气体的质量相等,则V(A)∶V(C)=
(4)取100 mL 0.3 mol·L-1和300 mL 0.25 mol·L-1的硫酸注入500 mL容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题。
(1)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量之比为___________ ,密度之比为___________ 。
(2)同温同压下,同质量的氨气和硫化氢气体的体积之比为___________ ,其中含有的氢原子数目之比为___________ 。
(3)同温同压下,氨气和硫化氢气体含有的氢原子数相等,则氨气和硫化氢气体的体积之比为___________ ,电子数之比为___________ 。
(1)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量之比为
(2)同温同压下,同质量的氨气和硫化氢气体的体积之比为
(3)同温同压下,氨气和硫化氢气体含有的氢原子数相等,则氨气和硫化氢气体的体积之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有mgX元素的单质气体 (其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:
(其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:
(1)该气体的物质的量为___________ mol。
(2)该气体所含原子总数为___________ 。
(3)该气体在标准状况下的体积为___________ L。
(4)该气体全部溶于1L水中(不考虑与水反应,水的密度为1g/cm3),其溶液中溶质的质量分数为___________ 。
(5)X元素的另一单质气体 与
与 的关系是
的关系是___________ 。mg 气体的物质的量为
气体的物质的量为___________ mol,所含原子总数为___________ 。
 (其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:
(其摩尔质量为Mg/mol)。若阿伏加德罗常数的数值用NA表示,则:(1)该气体的物质的量为
(2)该气体所含原子总数为
(3)该气体在标准状况下的体积为
(4)该气体全部溶于1L水中(不考虑与水反应,水的密度为1g/cm3),其溶液中溶质的质量分数为
(5)X元素的另一单质气体
 与
与 的关系是
的关系是 气体的物质的量为
气体的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】据所学知识填空:
(1)4.9g H2SO4含_________ 个H2SO4分子,含氧原子数为_________ ,能和_________ molNaOH完全反应。
(2)含有相同碳原子数的CO和CO2,其质量比为_________ 。
(3)73gHCl的物质的量为________ ,含分子数为________ 。
(4)有①2 mol CH4,②9.03×1023个NH3分子,③85gH2S三种气体,对这三种气体的物质的量从大到小的顺序是___________ 。
(5)7.8g Na2X含有Na+ 0.2mol,则Na2X的摩尔质量为_______ ,X的相对原子质量为________ 。
(6)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4mol/L,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4mol/L,则c( )=
)=_______ 。
(1)4.9g H2SO4含
(2)含有相同碳原子数的CO和CO2,其质量比为
(3)73gHCl的物质的量为
(4)有①2 mol CH4,②9.03×1023个NH3分子,③85gH2S三种气体,对这三种气体的物质的量从大到小的顺序是
(5)7.8g Na2X含有Na+ 0.2mol,则Na2X的摩尔质量为
(6)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、
 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4mol/L,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4mol/L,则c( )=
)=
您最近一年使用:0次

 表示阿伏加德罗常数。则:
表示阿伏加德罗常数。则: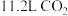 的质量为
的质量为 ,用双线桥表示该反应
,用双线桥表示该反应 的
的 参与反应,转移
参与反应,转移 溶液,需要
溶液,需要
 个X气体分子的质量是
个X气体分子的质量是 。则X气体的摩尔质量是
。则X气体的摩尔质量是

