据所学知识填空:
(1)4.9g H2SO4含_________ 个H2SO4分子,含氧原子数为_________ ,能和_________ molNaOH完全反应。
(2)含有相同碳原子数的CO和CO2,其质量比为_________ 。
(3)73gHCl的物质的量为________ ,含分子数为________ 。
(4)有①2 mol CH4,②9.03×1023个NH3分子,③85gH2S三种气体,对这三种气体的物质的量从大到小的顺序是___________ 。
(5)7.8g Na2X含有Na+ 0.2mol,则Na2X的摩尔质量为_______ ,X的相对原子质量为________ 。
(6)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4mol/L,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4mol/L,则c( )=
)=_______ 。
(1)4.9g H2SO4含
(2)含有相同碳原子数的CO和CO2,其质量比为
(3)73gHCl的物质的量为
(4)有①2 mol CH4,②9.03×1023个NH3分子,③85gH2S三种气体,对这三种气体的物质的量从大到小的顺序是
(5)7.8g Na2X含有Na+ 0.2mol,则Na2X的摩尔质量为
(6)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、
 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4mol/L,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4mol/L,则c( )=
)=
更新时间:2023-12-06 18:27:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)质量比为51:32:34的NH3、CH4、H2S,其物质的量之比为__________ ,它们所含氢原子数之比为_________ ,所含质子数之比为__________ 。
(2)有7.8gNa2R含Na+为0.2mol,则Na2R的摩尔质量为__________ ,R的相对原子质量为_________ 。
(3)在150°C,m gNH4HCO3固体完全分解生成NH3、CO2、H2O,若所得混合气体对H2的相对密度为d,则用含m、d的代数式表示混合气体的物质的量为_________ ;用含m、d的代数式表示NH4HCO3的摩尔质量为________________ 。
(4)某化学兴趣小组对“农夫山泉”矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,则该矿泉水中Mg2+的物质的量浓度为_______ 。
(2)有7.8gNa2R含Na+为0.2mol,则Na2R的摩尔质量为
(3)在150°C,m gNH4HCO3固体完全分解生成NH3、CO2、H2O,若所得混合气体对H2的相对密度为d,则用含m、d的代数式表示混合气体的物质的量为
(4)某化学兴趣小组对“农夫山泉”矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,则该矿泉水中Mg2+的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用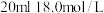 的浓硫酸和铜共热一段时间后,待反应混合物冷却后倒入冷水中,滤去多余的铜,将滤液加水定容到
的浓硫酸和铜共热一段时间后,待反应混合物冷却后倒入冷水中,滤去多余的铜,将滤液加水定容到 ,溶液中
,溶液中 的浓度为
的浓度为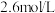 。
。
(1)反应后溶液中 的浓度是
的浓度是_______ 
(2)假设反应后得到的 气体全部逸出,则这些气体的体积在标况下是
气体全部逸出,则这些气体的体积在标况下是_______ 升。
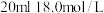 的浓硫酸和铜共热一段时间后,待反应混合物冷却后倒入冷水中,滤去多余的铜,将滤液加水定容到
的浓硫酸和铜共热一段时间后,待反应混合物冷却后倒入冷水中,滤去多余的铜,将滤液加水定容到 ,溶液中
,溶液中 的浓度为
的浓度为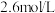 。
。(1)反应后溶液中
 的浓度是
的浓度是
(2)假设反应后得到的
 气体全部逸出,则这些气体的体积在标况下是
气体全部逸出,则这些气体的体积在标况下是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在隔绝空气的条件下,某同学将一块被氧化钠覆盖的钠块用一-张刺有小孔的纯净铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待反应完全后,在容器中收集到1.12LH2(标准状况,忽略溶解的氢气的量),测得铝箔质量比反应前减少了0.27g,水槽和容器.内溶液的总体积为2.0L,溶液中NaOH的浓度为0.050mol·L-1。
请回答下列问题:
(1)写出有关反应的化学方程式___ 。
(2)分别计算收集到的H2和参加反应的Al的物质的量___ 、___ 。
(3)该钠块中钠元素的质量分数是(精确到0.1%)___ 。
请回答下列问题:
(1)写出有关反应的化学方程式
(2)分别计算收集到的H2和参加反应的Al的物质的量
(3)该钠块中钠元素的质量分数是(精确到0.1%)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请按要求回答下列问题。
(1)钠和水的反应的化学方程式为:________ ,溶液呈______ 性(酸/碱)。
(2)1molH2O含有________ 个水分子,1.204×1023个水分子的物质的量为________ mol。
(3)H2SO4的摩尔质量是________ ,147gH2SO4的物质的量是________ mol。
(4)在标准状况下,33.6LCO2的物质的量是________ mol,含有________ 分子。
(1)钠和水的反应的化学方程式为:
(2)1molH2O含有
(3)H2SO4的摩尔质量是
(4)在标准状况下,33.6LCO2的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)下列数量的各物质所含原子数按由大到小的顺序排列是________ 。
①0.5 mol氨气
②标准状况下22.4 L氦气
③4 ℃时9 mL水
④0.2 mol磷酸钠(Na3PO4)
(2)现有m g某气体,它是三原子分子,其摩尔质量为M g·mol-1。若阿伏伽德罗常数用NA表示,请用以上符号及相应数字填写下列空格。
①该气体的物质的量为________ mol。
②该气体所含原子总数为________ 个。
③该气体在标准状况下的体积为________ L。
④该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为________ mol·L-1。
①0.5 mol氨气
②标准状况下22.4 L氦气
③4 ℃时9 mL水
④0.2 mol磷酸钠(Na3PO4)
(2)现有m g某气体,它是三原子分子,其摩尔质量为M g·mol-1。若阿伏伽德罗常数用NA表示,请用以上符号及相应数字填写下列空格。
①该气体的物质的量为
②该气体所含原子总数为
③该气体在标准状况下的体积为
④该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】判断正误:
1.常温常压下,3.2gO2所含的原子数为0.2NA。(_______)
2.标准状况下,18gH2O所含的氧原子数目为NA。(_______)
3.室温下,1molCH4中含有5NA原子。(_______)
4.常温常压下,1molCO2与SO2的混合气体中含氧原子数为2NA。(_______)
5.2g石墨晶体中,含有的质子数目为6NA。(_______)
6.2molSO2和1molO2在一定条件下充分反应后,混合物的分子数为2NA。(_______)
7.密闭容器中2amolNO与amolO2充分反应,产物的分子数为2aNA。(_______)
8.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA。(_______)
9.1L0.1mol·L-1的氨水中有NA个NH 。(_______)
。(_______)
10.向含4molHCl的浓盐酸中,加入足量的MnO2,加热,充分反应后,生成NA个Cl2。(_______)
11.用含有1molFeCl3的溶液充分反应后得的Fe(OH)3胶体中含有NA个Fe(OH)3胶粒。(_______)
1.常温常压下,3.2gO2所含的原子数为0.2NA。(_______)
2.标准状况下,18gH2O所含的氧原子数目为NA。(_______)
3.室温下,1molCH4中含有5NA原子。(_______)
4.常温常压下,1molCO2与SO2的混合气体中含氧原子数为2NA。(_______)
5.2g石墨晶体中,含有的质子数目为6NA。(_______)
6.2molSO2和1molO2在一定条件下充分反应后,混合物的分子数为2NA。(_______)
7.密闭容器中2amolNO与amolO2充分反应,产物的分子数为2aNA。(_______)
8.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA。(_______)
9.1L0.1mol·L-1的氨水中有NA个NH
 。(_______)
。(_______)10.向含4molHCl的浓盐酸中,加入足量的MnO2,加热,充分反应后,生成NA个Cl2。(_______)
11.用含有1molFeCl3的溶液充分反应后得的Fe(OH)3胶体中含有NA个Fe(OH)3胶粒。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】利用“化学计量在实验中的应用”的相关知识进行填空(NA 表示阿伏加德罗常数的值)。
(1)49g的H2SO4能与_______ mol NaOH恰好完全反应。
(2)在一定的温度和压强下,1体积气体X2跟2体积气体Y2化合生成2体积化合物,则该化合物的化学式是_______ 。
(3)1mol H2O所含电子个数为:_______ ;
(4)现有mg某X2气体,它的摩尔质量为M g/mol,则:
①该气体的物质的量为_______ mol。
②一个X原子的质量_______ g。
③该气体在标准状况下的体积为_______ L。
④相同温度与压强下,若X2与氮气以体积比1:4混合,该混合气体相对氢气密度为14.4,X2的相对分子质量为_______ 。
⑤若标况下X2的密度为1.25 g/L,X原子最外层有_______ 个电子。
(1)49g的H2SO4能与
(2)在一定的温度和压强下,1体积气体X2跟2体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(3)1mol H2O所含电子个数为:
(4)现有mg某X2气体,它的摩尔质量为M g/mol,则:
①该气体的物质的量为
②一个X原子的质量
③该气体在标准状况下的体积为
④相同温度与压强下,若X2与氮气以体积比1:4混合,该混合气体相对氢气密度为14.4,X2的相对分子质量为
⑤若标况下X2的密度为1.25 g/L,X原子最外层有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在标准状况下,①5 g H2 ②11.2 L O2 ③2 mol H2O ④6.02×1023个 CO2分子。
(1)5gH2 的物质的量是_______ ,体积是_______ ;
(2)6.02×1023个CO2分子的物质的量是_____ ,质量是______ ,
(3)所含分子数最多的是______ (请用序号回答,后同);
(4)所含原子数最多的是______ ;
(5)质量最大的是_______ ;
(6)体积最大的是_______ ;
(7)气体密度最大的是_______ ;
(8)体积最小的是_______ ;
(1)5gH2 的物质的量是
(2)6.02×1023个CO2分子的物质的量是
(3)所含分子数最多的是
(4)所含原子数最多的是
(5)质量最大的是
(6)体积最大的是
(7)气体密度最大的是
(8)体积最小的是
您最近一年使用:0次



