向体积均为10mL、物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2,得到溶液甲和乙。向甲、乙两溶液中分别滴加0.1mol/L的盐酸,此时反应生成CO2体积(标准状况)与所加盐酸体积的关系如图所示。则下列叙述中不正确的是
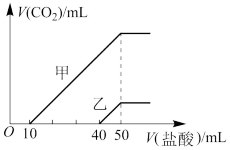

| A.原NaOH溶液的物质的量浓度为 0.5mol/L |
B.当0<V(盐酸)<10mL时,甲溶液中发生反应的离子方程式为H++ CO =HCO =HCO |
| C.乙溶液中含有的溶质是Na2CO3和NaOH且二者物质的量比值是3:1 |
| D.向乙溶液中滴加过量盐酸后产生CO2体积的最大值为224mL |
更新时间:2021-10-16 09:24:38
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
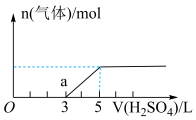
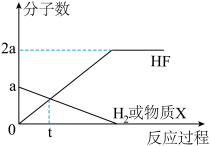
【推荐1】标准状况下,将VL 气体通入2L的NaOH溶液中,在所得溶液中逐滴加入
气体通入2L的NaOH溶液中,在所得溶液中逐滴加入 稀硫酸全过量,产生的气体与消耗的
稀硫酸全过量,产生的气体与消耗的 体积关系如图所示(忽略
体积关系如图所示(忽略 的溶解)。下列说法正确的是
的溶解)。下列说法正确的是
说法正确的是
 气体通入2L的NaOH溶液中,在所得溶液中逐滴加入
气体通入2L的NaOH溶液中,在所得溶液中逐滴加入 稀硫酸全过量,产生的气体与消耗的
稀硫酸全过量,产生的气体与消耗的 体积关系如图所示(忽略
体积关系如图所示(忽略 的溶解)。下列说法正确的是
的溶解)。下列说法正确的是
说法正确的是
A.标准状况下 |
B.O到a点过程中发生反应先后顺序为: 、 、 |
C.a点溶液中所含溶质的化学式为 |
D.NaOH溶液的物质的量浓度为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】ClO2是一种国际公认的安全、无毒的绿色消毒剂,沸点11℃,凝固点-59℃。工业上,可用下列原理制备ClO2(液相反应):2FeS2+30NaClO3+14H2SO4=Fe2(SO4)3+15Na2SO4+30ClO2↑+14H2O。设NA是阿伏加德罗常数的值。下列说法正确的是
| A.在标准状况下,2240mLClO2含有原子数为0.3NA |
B.若生成1.5molNa2SO4,则反应后的溶液中SO 数目为1.8NA 数目为1.8NA |
| C.48.0gFeS2完全反应,则上述反应中转移电子数为6NA |
| D.每消耗30molNaClO3,生成的水中氢原子数目为14NA |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】向体积均为 100 mL 且物质的量浓度相同的两份NaOH 溶液中分别通入一定量的 CO2得到溶液甲和乙。向甲、乙两溶液中分别滴加 0.1 mol·L-1盐酸。此时反应生成 CO2 体积(标准状况)与所加盐酸体积间的关系如图所示。下列叙述中正确的是
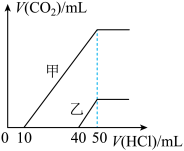

| A.原 NaOH 溶液的物质的量浓度为 0.5 mol·L-1 |
| B.当 0<V(HCl)<40 mL 时,乙溶液中发生反应的离子方程式为:OH-+H+=H2O |
| C.甲溶液中含有的溶质是 Na2CO3和NaHCO3 |
| D.乙溶液中滴加盐酸后产生 CO2 体积的最大值为 22.4 mL(标准状况) |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】把含有 和
和 的混合溶液V L分成两等份,一份加入含
的混合溶液V L分成两等份,一份加入含 BaCl2的溶液,恰好使
BaCl2的溶液,恰好使 完全反应生成m克沉淀;另一份加入含
完全反应生成m克沉淀;另一份加入含 KOH的溶液,恰好使
KOH的溶液,恰好使 完全转化为沉淀,则原混合溶液中
完全转化为沉淀,则原混合溶液中 的浓度为
的浓度为
 和
和 的混合溶液V L分成两等份,一份加入含
的混合溶液V L分成两等份,一份加入含 BaCl2的溶液,恰好使
BaCl2的溶液,恰好使 完全反应生成m克沉淀;另一份加入含
完全反应生成m克沉淀;另一份加入含 KOH的溶液,恰好使
KOH的溶液,恰好使 完全转化为沉淀,则原混合溶液中
完全转化为沉淀,则原混合溶液中 的浓度为
的浓度为A.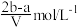 | B. | C.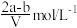 | D. |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】研究多元酸碱反应的分步过程可借助于pH曲线。向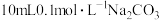 溶液中逐滴滴加
溶液中逐滴滴加 某二元酸H2B溶液,得溶液pH随加入的H2B体积
某二元酸H2B溶液,得溶液pH随加入的H2B体积 的变化如图所示。已知:H2CO3的
的变化如图所示。已知:H2CO3的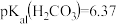 ,
,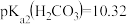 下列说法错误的是
下列说法错误的是

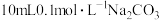 溶液中逐滴滴加
溶液中逐滴滴加 某二元酸H2B溶液,得溶液pH随加入的H2B体积
某二元酸H2B溶液,得溶液pH随加入的H2B体积 的变化如图所示。已知:H2CO3的
的变化如图所示。已知:H2CO3的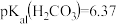 ,
,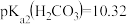 下列说法错误的是
下列说法错误的是
| A.该曲线有两处pH突变,突变分别出现在V=5mL和V=20mL处 |
B. 在0~5mL区间,发生的反应是 在0~5mL区间,发生的反应是 |
C.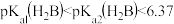 |
D. 在5~20mL区间,HB-的物质的量一直在增加 在5~20mL区间,HB-的物质的量一直在增加 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列关于Na2CO3和NaHCO3的性质比较中,不正确的是( )
| A.热稳定性:Na2CO3>NaHCO3 |
| B.常温下在水中的溶解性:NaHCO3>Na2CO3 |
| C.等物质的量浓度的溶液与稀盐酸反应的产生气体的速率:Na2CO3>NaHCO3 |
| D.等质量的固体与足量盐酸反应放出CO2的质量:Na2CO3<NaHCO3 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】既能与盐酸反应又能与NaOH溶液反应的物质是( )
| A.Al | B.Al2O3 | C.Al(OH)3 | D.NaHCO3 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式不正确的是
A.少量Na2CO3溶液滴入到硝酸中: H++CO =HCO =HCO |
| B.过量CO2通入到澄清的石灰水中:2CO2+Ca2++2OH-=CaCO3↓+H2O |
C.烧碱溶液与碳酸氢钙溶液混合:2OH—+Ca2++2HCO =CaCO3↓+CO =CaCO3↓+CO +2H2O +2H2O |
D.小苏打溶液与氢氧化钡溶液反应:HCO +Ba2++OH-=BaCO3↓+H2O +Ba2++OH-=BaCO3↓+H2O |
您最近一年使用:0次

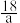 g
g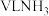 完全溶于1L水,所得溶液的密度为
完全溶于1L水,所得溶液的密度为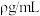 ,溶质质量分数为w,物质的量浓度为
,溶质质量分数为w,物质的量浓度为 ,下列叙述正确的是
,下列叙述正确的是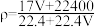
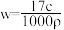
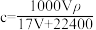
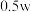

 溶液中滴入
溶液中滴入 溶液至产生的
溶液至产生的
 溶液:
溶液:
 +2H2O=4OH-+O2↑
+2H2O=4OH-+O2↑ 与稀盐酸反应:
与稀盐酸反应:


