回答下列问题:
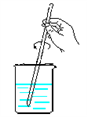
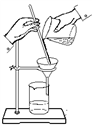
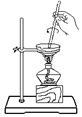
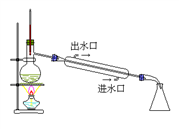
(1)写出图中相应仪器的名称:
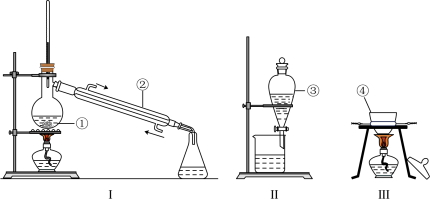
①___ ;④___ 。
(2)查资料得知:ρ(H2O)>ρ(苯),苯与水不互溶,碘单质在苯中溶解度很大。已知碘和苯的熔沸点数据如表所示:
若用苯萃取碘水中的碘单质,分液时,有机层应从分液漏斗的___ 端口倒出(填“上”或“下”,下同)。所得的有机层混合物可选用装置___ (填“Ⅰ”“Ⅱ”或“Ⅲ”)进一步分离,锥形瓶中收集到的物质的是___ 。
(3)依据粗盐提纯的原理,除去氯化钾溶液中少量的氯化镁、硫酸镁等杂质,可选用氢氧化钡溶液、稀盐酸和碳酸钾溶液三种试剂,按如图步骤操作:
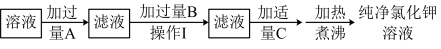
B的化学式是___ ,操作Ⅰ为过滤,为了提高KCl的提取率,过滤后还需对滤渣进一步进行洗涤,洗涤的操作方法为___ 。
(1)写出图中相应仪器的名称:

①
(2)查资料得知:ρ(H2O)>ρ(苯),苯与水不互溶,碘单质在苯中溶解度很大。已知碘和苯的熔沸点数据如表所示:
| 熔点 | 沸点 | |
| 碘 | 113.7℃ | 184.3℃ |
| 苯 | 5.5℃ | 80.1℃ |
(3)依据粗盐提纯的原理,除去氯化钾溶液中少量的氯化镁、硫酸镁等杂质,可选用氢氧化钡溶液、稀盐酸和碳酸钾溶液三种试剂,按如图步骤操作:

B的化学式是
更新时间:2021-10-20 18:12:23
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某NaCl溶液样品中含有Na2SO4、CaCl2杂质(该溶液用X表示),除去杂质的实验方案如图所示。

请回答:
(1)溶液B中存在的阳离子为____________ ,阴离子为___________ 。
(2)固体C中所含物质的化学式为__________ 。
(3)溶液D中加入适量盐酸后,大量减少的微粒为__________ 。
(4)①和②不能调换顺序的理由为______________ 。

请回答:
(1)溶液B中存在的阳离子为
(2)固体C中所含物质的化学式为
(3)溶液D中加入适量盐酸后,大量减少的微粒为
(4)①和②不能调换顺序的理由为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】为落实“五水共治”,某工厂拟综合处理含 废水和工业废气(主要含
废水和工业废气(主要含 、
、 、
、 、NO、CO,不考虑其他成分),设计如图流程:
、NO、CO,不考虑其他成分),设计如图流程:

已知: 的氧化性弱于
的氧化性弱于
回答下列问题:
(1)气体1中的有毒气体可通过催化剂直接转化为无污染气体,反应的化学方程式为_______ 。
(2)气体2中捕获剂所捕获的气体主要是_______ 。
(3)若X是 ,上述反应中NO和
,上述反应中NO和 的物质的量之比最好为
的物质的量之比最好为_______ ,才能恰好转化为 溶液;若通入
溶液;若通入 过量,导致的结果会是
过量,导致的结果会是_______ 。
(4)检验废水中含 的方法是
的方法是_______ ,流程中处理含废水时 反应的离子方程式为
反应的离子方程式为_______ 。
 废水和工业废气(主要含
废水和工业废气(主要含 、
、 、
、 、NO、CO,不考虑其他成分),设计如图流程:
、NO、CO,不考虑其他成分),设计如图流程:
已知:
 的氧化性弱于
的氧化性弱于
回答下列问题:
(1)气体1中的有毒气体可通过催化剂直接转化为无污染气体,反应的化学方程式为
(2)气体2中捕获剂所捕获的气体主要是
(3)若X是
 ,上述反应中NO和
,上述反应中NO和 的物质的量之比最好为
的物质的量之比最好为 溶液;若通入
溶液;若通入 过量,导致的结果会是
过量,导致的结果会是(4)检验废水中含
 的方法是
的方法是 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。某班同学在粗盐提纯实验中,为把少量可溶性杂质 、
、 一并除去,设计了如下方案:
一并除去,设计了如下方案:

回答下列问题:
(1)为了加快粗盐的溶解,可采取的措施有_______ (填一种即可)。
(2)写出步骤Ⅳ中发生反应的化学方程式:_______ 。
(3)沉淀B的主要成分为_______ (填化学式)。
(4)在步骤Ⅵ中,_______ (填“能”或“不能”)用稀硝酸代替稀盐酸进行该实验,理由为_______ 。
(5)步骤Ⅶ中操作b指的是_______ 。
(6)该方案实际得到的氯化钠比粗盐中含有的氯化钠要多,理由为_______ 。
 、
、 一并除去,设计了如下方案:
一并除去,设计了如下方案:
回答下列问题:
(1)为了加快粗盐的溶解,可采取的措施有
(2)写出步骤Ⅳ中发生反应的化学方程式:
(3)沉淀B的主要成分为
(4)在步骤Ⅵ中,
(5)步骤Ⅶ中操作b指的是
(6)该方案实际得到的氯化钠比粗盐中含有的氯化钠要多,理由为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】已知苯与液溴的反应是放热反应,某校学生为探究苯与液溴发生反应的原理,用如图装置进行实验。(夹持装置已略去)
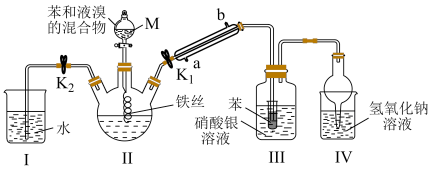
请回答下列问题:
(1)仪器M的名称为_______ ;写出装置II中发生反应的化学方程式_______ 。
(2)装置III 溶液中出现的现象为
溶液中出现的现象为_______ ,由此证明该反应的类型为_______ 。
(3)冷凝管冷凝水由_______ 口进(填“a”或“b”);装置III小试管中苯的作用是_______ 。
(4)实验装置IV中球形干燥管的作用是_______ 。
(5)反应结束后提纯产物,粗溴苯经过碱洗与水洗,可除去溶解的溴,再经无水硫酸镁干燥后,可选择下列操作中_______ 除去溶解的苯。
a.重结晶 b.过滤 c.蒸馏 d.萃取

请回答下列问题:
(1)仪器M的名称为
(2)装置III
 溶液中出现的现象为
溶液中出现的现象为(3)冷凝管冷凝水由
(4)实验装置IV中球形干燥管的作用是
(5)反应结束后提纯产物,粗溴苯经过碱洗与水洗,可除去溶解的溴,再经无水硫酸镁干燥后,可选择下列操作中
a.重结晶 b.过滤 c.蒸馏 d.萃取
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】如图是中学化学中常用于混合物的分离和提纯装置,请根据装置回答问题:
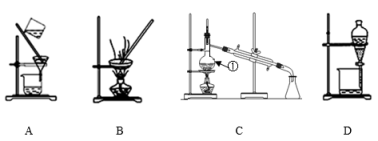
(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是___ 。
(2)装置C中①的名称是___ ,此装置中冷凝水进出方向是___ (填“上进下出”还是“下进上出”)。装置D中的分液漏斗在使用之前应该___ ,在分液时为使液体顺利滴下,应进行的具体操作是___ 。
(3)某硝酸钠固体中混有少量硫酸钠杂质,现设计一实验方案,既除去杂质,又配成硝酸钠溶液。实验方案:先将固体溶于蒸馏水配成溶液,选择合适的试剂和操作完成表格中各步实验。
所加入的试剂①可以是___ (填化学式),证明溶液中SO42-已经除尽的方法是___ 。加入Na2CO3溶液的目的是___ ,所加入的试剂④可以是___ (填化学式)。

(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是
(2)装置C中①的名称是
(3)某硝酸钠固体中混有少量硫酸钠杂质,现设计一实验方案,既除去杂质,又配成硝酸钠溶液。实验方案:先将固体溶于蒸馏水配成溶液,选择合适的试剂和操作完成表格中各步实验。
| 选择适当试剂按顺序添加 | ① | Na2CO3溶液 | ④ |
| 实验操作 | ② | ③ | 加热 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】海洋约占地球表面积的71%,具有巨大的开发潜力。
Ⅰ.海水淡化的方法主要有蒸馏法、电渗法和离子交换法等。如图为海水蒸馏原理示意图,请回答下列问题:

(1)冷却水的进水口_______ (填“a”或“b”)。
(2)碎瓷片的作用是_______ (填“防止暴沸”或“作催化剂”)。
Ⅱ.目前,从海水提取的溴占世界溴年产量的三分之一左右,空气吹出法是工业上海水提溴的常用方法。其中一种工艺流程为:
①水浓缩,酸化;
②通入 ,使
,使 转化为
转化为 ;
;
③通入空气、水蒸气,将 吹入吸收塔,与吸收剂
吹入吸收塔,与吸收剂 反应转化为HBr;
反应转化为HBr;
④通入 ,再经过一系列处理得到产品
,再经过一系列处理得到产品 。
。
请回答下列问题:
(3)步骤②、③操作的目的是_______ (填“富集溴”或“萃取溴”)。
(4)在步骤③中,生成HBr的化学方程式是_______ 。
(5)在步骤②中,若通入 (标准状况),理论上可得
(标准状况),理论上可得
_______ g。
Ⅲ.目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下:

请回答下列问题:
(6)写出在沉淀池中发生反应的离子方程式_______ 。
(7)石灰乳是生石灰与水形成的化合物,从充分利用海洋化学资源,提高经济效益的角度,生产生石灰的主要原料来源于海洋中的_______ 。
(8)操作A是_______ ,操作B是_______ 。
(9)加入的足量试剂a是_______ (填化学式)。
(10)无水 在熔融状态下通电后会产生Mg和
在熔融状态下通电后会产生Mg和 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。从考虑成本和废物循环利用的角度,副产物氯气可以用于_______ 。
Ⅰ.海水淡化的方法主要有蒸馏法、电渗法和离子交换法等。如图为海水蒸馏原理示意图,请回答下列问题:

(1)冷却水的进水口
(2)碎瓷片的作用是
Ⅱ.目前,从海水提取的溴占世界溴年产量的三分之一左右,空气吹出法是工业上海水提溴的常用方法。其中一种工艺流程为:
①水浓缩,酸化;
②通入
 ,使
,使 转化为
转化为 ;
;③通入空气、水蒸气,将
 吹入吸收塔,与吸收剂
吹入吸收塔,与吸收剂 反应转化为HBr;
反应转化为HBr;④通入
 ,再经过一系列处理得到产品
,再经过一系列处理得到产品 。
。请回答下列问题:
(3)步骤②、③操作的目的是
(4)在步骤③中,生成HBr的化学方程式是
(5)在步骤②中,若通入
 (标准状况),理论上可得
(标准状况),理论上可得
Ⅲ.目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下:

请回答下列问题:
(6)写出在沉淀池中发生反应的离子方程式
(7)石灰乳是生石灰与水形成的化合物,从充分利用海洋化学资源,提高经济效益的角度,生产生石灰的主要原料来源于海洋中的
(8)操作A是
(9)加入的足量试剂a是
(10)无水
 在熔融状态下通电后会产生Mg和
在熔融状态下通电后会产生Mg和 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。

I.请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)从碳酸钙悬浊液中分离出碳酸钙_______________ 。
(2)从氯化钠溶液中分离出氯化钠_______________ 。
(3)分离植物油和水_______________ 。
(4)由海水获得蒸馏水________________ 。
Ⅱ.从碘水中提取碘单质的方法如下:
(1)萃取分液
①下列可作为碘水中提取碘单质萃取剂的是________________ 。
A 乙醇 B 苯
②分液漏斗在使用前必须先________________ 。
③查资料得知: ,若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应从分液漏斗的
,若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应从分液漏斗的_____________ (填“上”或“下”,下同)端口放出,有机层应从分液漏斗的__________ 端口倒出。
(2)蒸馏
①装置A中a的名称是_____________ ,冷凝装置中冷凝水应该从_____________ (填“上”或“下”)口进,这样做的目的是__________ ,装置C在分液时为使液体顺利滴下,除打开漏斗下端的旋塞外,还应进行的具体操作是____________ 。
②已知碘和四氯化碳的熔沸点数据如表所示:
若用蒸馏法分离碘和四氯化碳的混合物,锥形瓶中先收集到的物质的名称是_______________ 。

I.请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)从碳酸钙悬浊液中分离出碳酸钙
(2)从氯化钠溶液中分离出氯化钠
(3)分离植物油和水
(4)由海水获得蒸馏水
Ⅱ.从碘水中提取碘单质的方法如下:
(1)萃取分液
①下列可作为碘水中提取碘单质萃取剂的是
A 乙醇 B 苯
②分液漏斗在使用前必须先
③查资料得知:
 ,若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应从分液漏斗的
,若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应从分液漏斗的(2)蒸馏
①装置A中a的名称是
②已知碘和四氯化碳的熔沸点数据如表所示:
| 熔点 | 沸点 | |
| 碘 | 113.7℃ | 184.3℃ |
| 四氯化碳 | -22.6℃ | 76.8℃ |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】青蒿素是烃的含氧衍生物,为无色针状晶体,可溶于乙醇、乙醚,在水中几乎不溶,熔点为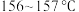 ,是高效的抗疟药。已知:乙醚的沸点为
,是高效的抗疟药。已知:乙醚的沸点为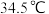 。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。
。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。
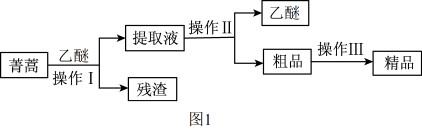
(1)实验室用乙醚提取青蒿素的流程如图1所示。___________ 。
②操作I所用到的主要玻璃仪器是___________ ,操作II的名称是___________ 。
③操作III的主要过程是:加95%的乙醇,___________ 、___________ 、过滤、洗涤、干燥。
(2)用如图2所示的实验装置测定青蒿素实验式的方法如下:将 青蒿素样品放在装置C的硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
青蒿素样品放在装置C的硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。 溶液,则装置B中盛放的试剂是
溶液,则装置B中盛放的试剂是___________ ,装置E中盛放的物质是___________ ,装置F中盛放的物质是___________ 。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是___________ 。
③用合理改进后的装置进行实验,测得的数据如表所示:
则青蒿素的实验式是___________ 。
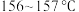 ,是高效的抗疟药。已知:乙醚的沸点为
,是高效的抗疟药。已知:乙醚的沸点为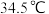 。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。
。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法。(1)实验室用乙醚提取青蒿素的流程如图1所示。
②操作I所用到的主要玻璃仪器是
③操作III的主要过程是:加95%的乙醇,
(2)用如图2所示的实验装置测定青蒿素实验式的方法如下:将
 青蒿素样品放在装置C的硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
青蒿素样品放在装置C的硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
 溶液,则装置B中盛放的试剂是
溶液,则装置B中盛放的试剂是②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是
③用合理改进后的装置进行实验,测得的数据如表所示:
| 装置 | 实验前/g | 实验后/g |
| E | 22.6 | 32.5 |
| F | 80.2 | 113.2 |
您最近一年使用:0次
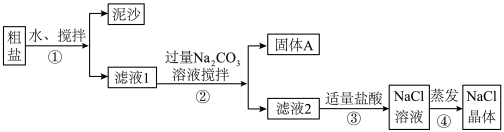
【推荐1】某同学用某种粗盐进行提纯实验,步骤见下图。
请回答下列问题:
(1)步骤①和②的操作名称是_______ 。
(2)步骤④加热蒸发时要用玻璃棒不断搅拌,目的是_______ 。
(3)猜想和验证:

请回答下列问题:
(1)步骤①和②的操作名称是
(2)步骤④加热蒸发时要用玻璃棒不断搅拌,目的是
(3)猜想和验证:
| 猜想 | 验证的方法 | 现象 | 结论 |
猜想I:固体A中含 、 、 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | 猜想I成立 | |
猜想II:固体A中含 | 取少量固体A于试管中,先滴入 溶液 溶液 | 有气泡放出,无白色沉淀 | 猜想II不成立 |
猜想III:最后制得的 晶体中还含有 晶体中还含有 | 取少量 晶体溶于试管中的蒸馏水, 晶体溶于试管中的蒸馏水, | 猜想III成立 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某同学设计如下实验,测定Na2CO3、NaHCO3和CaCO3固体混合物中钠元素的质量分数。实验过程如图所示:
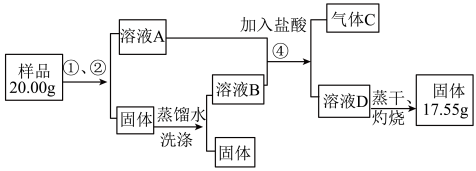
请回答:
(1)操作①、②的名称依次为_________ 。
(2)气体C是_________ (填化学式);溶液D是_________ (填化学式);
(3)原样品中钠元素的质量分数为_________________ 。

请回答:
(1)操作①、②的名称依次为
(2)气体C是
(3)原样品中钠元素的质量分数为
您最近一年使用:0次