能够说明 反应在密闭容器中已达到平衡状态的是:
反应在密闭容器中已达到平衡状态的是:_____ 。(填入序号)
①容器内 、
、 、
、 三者共存
三者共存
②容器内 、
、 、
、 三者浓度相等
三者浓度相等
③容器内 、
、 、
、 的浓度比恰为1:3:2
的浓度比恰为1:3:2
④tmin内生成
 同时消耗
同时消耗

⑤tmin内,生成
 同时消耗
同时消耗

⑥某时间内断裂
 键的同时,断裂
键的同时,断裂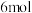 N-H键
N-H键
⑦容器内质量不随时间的变化而变化
⑧容器内压强不随时间的变化而变化
⑨容器内密度不再发生变化
⑩容器内的平均摩尔质量不再发生变化
 反应在密闭容器中已达到平衡状态的是:
反应在密闭容器中已达到平衡状态的是:①容器内
 、
、 、
、 三者共存
三者共存②容器内
 、
、 、
、 三者浓度相等
三者浓度相等③容器内
 、
、 、
、 的浓度比恰为1:3:2
的浓度比恰为1:3:2 ④tmin内生成

 同时消耗
同时消耗

⑤tmin内,生成

 同时消耗
同时消耗

⑥某时间内断裂

 键的同时,断裂
键的同时,断裂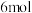 N-H键
N-H键⑦容器内质量不随时间的变化而变化
⑧容器内压强不随时间的变化而变化
⑨容器内密度不再发生变化
⑩容器内的平均摩尔质量不再发生变化
更新时间:2021-10-30 20:05:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某温度时,在2L恒容密闭容器中X、Y、Z三种气体的物质的量随时间的变化关系如图所示。
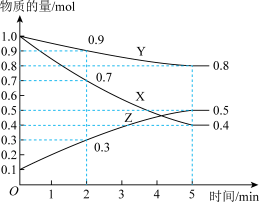
(1)由图中的数据分析可知,该反应的化学方程式为_______ 。
(2)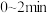 内X的平均反应速率为
内X的平均反应速率为_______ , 内Z的平均反应速率为
内Z的平均反应速率为_______ 。
(3) 后Z的生成速率
后Z的生成速率_______ (填“大于”、“小于”或“等于”) 时Z的生成速率。
时Z的生成速率。
(4)反应前的压强与平衡时的压强之比为_______ 。
(5)对于该反应,改变其中一个条件,则生成Z的速率怎样变化?(填“增大”、“减小”或“不变”)
①升高温度:_______ 。
②加入X:_______ 。
③增大容器容积:_______ 。

(1)由图中的数据分析可知,该反应的化学方程式为
(2)
 内X的平均反应速率为
内X的平均反应速率为 内Z的平均反应速率为
内Z的平均反应速率为(3)
 后Z的生成速率
后Z的生成速率 时Z的生成速率。
时Z的生成速率。(4)反应前的压强与平衡时的压强之比为
(5)对于该反应,改变其中一个条件,则生成Z的速率怎样变化?(填“增大”、“减小”或“不变”)
①升高温度:
②加入X:
③增大容器容积:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】向某容积固定的密闭容器中加入0.3mol A、0.1mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答下列问题:
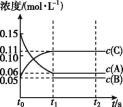
(1)密闭容器的容积是_______ L。
(2)若t1=15时,则t0~t1s内以C物质浓度变化表示的反应速率v(C)=_______ 。
(3)写出反应的化学方程式:_______ 。
(4)t2s时,C在平衡混合气体中的百分含量为_______ ,此时v正(A)_______ v逆(B)(选填“>”“<”或“=”)。
(5)B的起始的物质的量是_______ 。

(1)密闭容器的容积是
(2)若t1=15时,则t0~t1s内以C物质浓度变化表示的反应速率v(C)=
(3)写出反应的化学方程式:
(4)t2s时,C在平衡混合气体中的百分含量为
(5)B的起始的物质的量是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)在固定体积的密闭容器中,进行如下化学反应: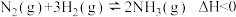 该反应的化学平衡常数表达式是K=
该反应的化学平衡常数表达式是K=_________ 。已知平衡常数K与温度T的关系如表:
①试判断K1_________ K2(填写“>”“=”或“<”)。
②下列各项能说明该反应已达到平衡状态的是_________ (填字母)。
a.容器内N2、H2、NH3的浓度之比为1∶3∶2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是_________ (填字母)。
a.采用较高温度(400~500℃)b.将生成的氨液化并及时从体系中分离出来
c.用铁触媒加快化学反应速率d.采用较高压强(20~50MPa)
(2)对反应 ,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是
,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是_________ 。

a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点N2O4的转化率:A<C
d.由状态B到状态A,可以用加热的方法
(1)在固定体积的密闭容器中,进行如下化学反应:
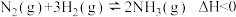 该反应的化学平衡常数表达式是K=
该反应的化学平衡常数表达式是K=T/℃ | 400 | 300 |
平衡常数K | K1 | K2 |
②下列各项能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1∶3∶2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③合成氨在农业和国防中有很重要的意义,在实际工业生产中,常采用下列措施,其中可以用勒夏特列原理解释的是
a.采用较高温度(400~500℃)b.将生成的氨液化并及时从体系中分离出来
c.用铁触媒加快化学反应速率d.采用较高压强(20~50MPa)
(2)对反应
 ,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是
,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点N2O4的转化率:A<C
d.由状态B到状态A,可以用加热的方法
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在某一容积为5 L的密闭容器内,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g)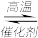 CO2(g)+H2(g)(正反应为吸热反应),反应中CO2的浓度随时间变化情况如图所示。
CO2(g)+H2(g)(正反应为吸热反应),反应中CO2的浓度随时间变化情况如图所示。

(1)根据图中数据,反应开始至达到平衡时,CO的反应速率为___________ ;反应达到平衡时,c(H2)=___________ 。
(2)判断该反应达到平衡的依据是___________ 。
①CO减少的化学反应速率和CO2减少的化学反应速率相等
②CO、H2O、CO2、H2的浓度都相等
③CO、H2O、CO2、H2的浓度都不再发生变化
④正、逆反应速率都为零
(3)如一开始加入0.1 mol的CO、0.1 mol的H2O、0.1 mol的CO2和0.1 mol的H2,在相同的条件下,反应达到平衡时,c(H2O)=___________ 。
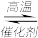 CO2(g)+H2(g)(正反应为吸热反应),反应中CO2的浓度随时间变化情况如图所示。
CO2(g)+H2(g)(正反应为吸热反应),反应中CO2的浓度随时间变化情况如图所示。
(1)根据图中数据,反应开始至达到平衡时,CO的反应速率为
(2)判断该反应达到平衡的依据是
①CO减少的化学反应速率和CO2减少的化学反应速率相等
②CO、H2O、CO2、H2的浓度都相等
③CO、H2O、CO2、H2的浓度都不再发生变化
④正、逆反应速率都为零
(3)如一开始加入0.1 mol的CO、0.1 mol的H2O、0.1 mol的CO2和0.1 mol的H2,在相同的条件下,反应达到平衡时,c(H2O)=
您最近半年使用:0次
【推荐2】汽车排放的尾气是大气污染气体之一。如何减少污染气体的排放是科学家研究的热门课题。请回答下列问题:
使汽车排放的CO和NO在一定条件下发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6 mol NO、8 mol CO充入10 L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6 mol NO、8 mol CO充入10 L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
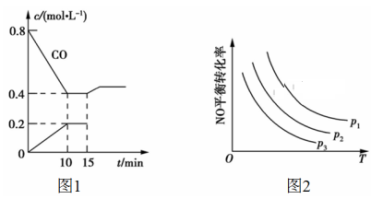
(1)该反应的化学平衡常数K=____ 。NO的平衡转化率=______ 。
(2)15 min时,若改变反应条件,导致CO浓度发生如图1所示的变化,则改变的条件可能是____ (填标号)。
a.缩小容器体积 b.增加CO2的量 c.体积不变通入少量氩气 d.加入催化剂
(3)当NO与CO的起始浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图2所示,则下列说法正确的是____ (填标号)。
A.该反应ΔH<0 B.p1<p2<p3
C.升高温度正反应速率减小,逆反应速率增大
D.温度不变,增大压强,平衡常数增大
(4)以下说法中能判断反应2NO(g)+2CO(g) N2 (g)+2CO2 (g)达到平衡的是
N2 (g)+2CO2 (g)达到平衡的是____ (填标号)。
A.反应物和生成物的物质的量相等
B.单位时间内生成1 mol NO同时生成1 mol CO2
C.混合气体压强不再发生变化
D.NO的浓度不再变化
(5)向反应容器中再分别充入下列气体,能使NO转化率增大的是____ (填标号)。
A.O2 B.N2 C.CO D.NO
使汽车排放的CO和NO在一定条件下发生反应:2NO(g)+2CO(g)
 N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6 mol NO、8 mol CO充入10 L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6 mol NO、8 mol CO充入10 L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
(1)该反应的化学平衡常数K=
(2)15 min时,若改变反应条件,导致CO浓度发生如图1所示的变化,则改变的条件可能是
a.缩小容器体积 b.增加CO2的量 c.体积不变通入少量氩气 d.加入催化剂
(3)当NO与CO的起始浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图2所示,则下列说法正确的是
A.该反应ΔH<0 B.p1<p2<p3
C.升高温度正反应速率减小,逆反应速率增大
D.温度不变,增大压强,平衡常数增大
(4)以下说法中能判断反应2NO(g)+2CO(g)
 N2 (g)+2CO2 (g)达到平衡的是
N2 (g)+2CO2 (g)达到平衡的是A.反应物和生成物的物质的量相等
B.单位时间内生成1 mol NO同时生成1 mol CO2
C.混合气体压强不再发生变化
D.NO的浓度不再变化
(5)向反应容器中再分别充入下列气体,能使NO转化率增大的是
A.O2 B.N2 C.CO D.NO
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】氮及其化合物在生产生活中有广泛的应用,按要求回答下列问题:
(1)工业合成氨的反应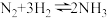 是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知断裂
是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知断裂 相应化学键需要的能量如下。若反应生成
相应化学键需要的能量如下。若反应生成 ,可
,可_______ (填“吸收”或“放出”)热量_______  。
。
(2)恒温下,将1 mol N2和3 mol H2置于体积为2L的密闭容器中进行反应。若5min时测得氢气浓度为0.9 mol/L,则用氨气表示5min内的化学反应速率为 _______ mol/(Lmin),5min时反应过程体系总压强与初始时的总压强之比为_______
(3)消除NO污染物,可在一定条件下,用CO与NO反应生成CO2和N2,在恒容密闭容中充入4 mol CO和4 mol NO发生2 CO(g)+2 NO(g)⇌N2 (g)+2 CO2(g)反应。
①为提高此反应的速率,下列措施可行的是_______ (填字母)。
A.充入氦气 B.降低温度 C.使用适合催化剂 D.移出CO2
②下列事实能说明该反应达到平衡状态的是_______ (填字母)
A.容器中NO和CO的体积分数之比不再变化
B.容器中混合气体的平均相对分子质量不再变化
C.2V正(NO)=V逆(N2)
D.相同时间内断裂N2中 数与形成CO2中C=O数之比为1:2
数与形成CO2中C=O数之比为1:2
(4)汽车尾气中含有的 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气中
传感器可监测汽车尾气中 含量,其工作原理如图所示:
含量,其工作原理如图所示:

 电极为
电极为_______ (填“正极”或“负极”), 电极上发生的电极反应式为
电极上发生的电极反应式为_______ 。
(1)工业合成氨的反应
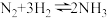 是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知断裂
是一个可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知断裂 相应化学键需要的能量如下。若反应生成
相应化学键需要的能量如下。若反应生成 ,可
,可 。
。| 化学键 |  |  |  |
| 能量 |  | 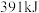 |  |
(3)消除NO污染物,可在一定条件下,用CO与NO反应生成CO2和N2,在恒容密闭容中充入4 mol CO和4 mol NO发生2 CO(g)+2 NO(g)⇌N2 (g)+2 CO2(g)反应。
①为提高此反应的速率,下列措施可行的是
A.充入氦气 B.降低温度 C.使用适合催化剂 D.移出CO2
②下列事实能说明该反应达到平衡状态的是
A.容器中NO和CO的体积分数之比不再变化
B.容器中混合气体的平均相对分子质量不再变化
C.2V正(NO)=V逆(N2)
D.相同时间内断裂N2中
 数与形成CO2中C=O数之比为1:2
数与形成CO2中C=O数之比为1:2(4)汽车尾气中含有的
 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气中
传感器可监测汽车尾气中 含量,其工作原理如图所示:
含量,其工作原理如图所示:
 电极为
电极为 电极上发生的电极反应式为
电极上发生的电极反应式为
您最近半年使用:0次



