向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol·L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示:

(1)原NaOH溶液的浓度为_______
(2)通入CO2在标准状况下的体积为_______ mL
(3)所得溶液的溶质成分及物质的量之比为_______
(4)在配制盐酸溶液时,将标况下VLHCl气体溶于100mL水中,所得溶液密度为d g·cm-3,则此溶液的物质的量浓度为_______ mol·L-1

(1)原NaOH溶液的浓度为
(2)通入CO2在标准状况下的体积为
(3)所得溶液的溶质成分及物质的量之比为
(4)在配制盐酸溶液时,将标况下VLHCl气体溶于100mL水中,所得溶液密度为d g·cm-3,则此溶液的物质的量浓度为
更新时间:2021-10-26 14:47:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.实验室配制490mL0.3mol/L的NaOH溶液
(1)需称量NaOH固体_____ g
(2)在该溶液的配制过程中,用到的玻璃仪器:量筒、烧杯、玻璃棒_____ 。
(3)如果在定容时仰视,溶液浓度将_____ ;(填“偏大”“偏小”“不影响” )
Ⅱ、取上述实验中配制的NaOH溶液200mL,缓慢通入一定量的CO2,充分反应,测最后溶液的pH>7。在上述所得溶液中,逐滴缓慢滴加一定浓度的盐酸,所得气体的体积与所加盐酸的体积(不考虑溶解于水)关系如图所示:

(4)加入盐酸200mL之前,无气体产生,写出OA段发生反应的离子方程式_____ 。
(5)A点时,反应所得溶液中溶质的成分有______
(6)产生的CO2在标准状况下的体积为_____ mL。
(1)需称量NaOH固体
(2)在该溶液的配制过程中,用到的玻璃仪器:量筒、烧杯、玻璃棒
(3)如果在定容时仰视,溶液浓度将
Ⅱ、取上述实验中配制的NaOH溶液200mL,缓慢通入一定量的CO2,充分反应,测最后溶液的pH>7。在上述所得溶液中,逐滴缓慢滴加一定浓度的盐酸,所得气体的体积与所加盐酸的体积(不考虑溶解于水)关系如图所示:

(4)加入盐酸200mL之前,无气体产生,写出OA段发生反应的离子方程式
(5)A点时,反应所得溶液中溶质的成分有
(6)产生的CO2在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)胶体分散质粒子直径范围:___________ 。
(2)写出硫酸与氢氧化钡溶液反应的离子反应方程式:___________ 。
(3)写出盐酸与纯碱溶液反应的离子反应方程式:___________ ;
(4)写出碳酸钙与盐酸溶液反应的离子方程式:___________ ;
(5)写出Al2(SO4)3的电离方程式___________
(2)写出硫酸与氢氧化钡溶液反应的离子反应方程式:
(3)写出盐酸与纯碱溶液反应的离子反应方程式:
(4)写出碳酸钙与盐酸溶液反应的离子方程式:
(5)写出Al2(SO4)3的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】以下三例是常见的化学实验:
①CO2通入澄清的石灰水,溶液先浑浊后澄清;
②将稀盐酸逐滴滴入Na2CO3溶液,开始时无现象,后产生气体;
③将NaOH溶液逐滴滴入AlCl3溶液,先产生白色沉淀,后沉淀消失;
回答下列问题:
(1)每例中均可用前后两个化学方程式来说明变化的规律,试用简要文字,说明这两个反应间的关系:______
(2)每例中若要保证后一个反应发生,必须具备的条件是什么?______ 。
(3)将各例中前后两个反应方程式叠加,写出一个总的方程式______ 。
①CO2通入澄清的石灰水,溶液先浑浊后澄清;
②将稀盐酸逐滴滴入Na2CO3溶液,开始时无现象,后产生气体;
③将NaOH溶液逐滴滴入AlCl3溶液,先产生白色沉淀,后沉淀消失;
回答下列问题:
(1)每例中均可用前后两个化学方程式来说明变化的规律,试用简要文字,说明这两个反应间的关系:
(2)每例中若要保证后一个反应发生,必须具备的条件是什么?
(3)将各例中前后两个反应方程式叠加,写出一个总的方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】正误判断,正确的打“√”,错误的打“×”
1.碳酸氢钠药片是抗酸药,服用时喝些醋能提高药效。(_______)
2.钠在空气中燃烧可生成多种氧化物,23 g Na燃烧转移电子为1NA。(_______)
3.将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产生气泡。(_______)
4.用热的烧碱溶液洗去油污,是因为Na2CO3可直接与油污反应。(_______)
5.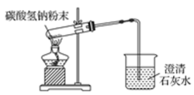 碳酸氢钠受热分解。(_______)
碳酸氢钠受热分解。(_______)
6.金属钠着火时,使用泡沫灭火器灭火。(_______)
7.热稳定性Na2CO3>NaHCO3。(_______)
8.溶解度:小苏打<苏打。(_______)
9.分别加热Na2CO3和NaHCO3固体,观察到试管内壁均有水珠,结论:两种物质均受热分解。(_______)
10.除去Na2CO3固体中的NaHCO3固体可用灼烧的方法。(_______)
1.碳酸氢钠药片是抗酸药,服用时喝些醋能提高药效。(_______)
2.钠在空气中燃烧可生成多种氧化物,23 g Na燃烧转移电子为1NA。(_______)
3.将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产生气泡。(_______)
4.用热的烧碱溶液洗去油污,是因为Na2CO3可直接与油污反应。(_______)
5.
 碳酸氢钠受热分解。(_______)
碳酸氢钠受热分解。(_______)6.金属钠着火时,使用泡沫灭火器灭火。(_______)
7.热稳定性Na2CO3>NaHCO3。(_______)
8.溶解度:小苏打<苏打。(_______)
9.分别加热Na2CO3和NaHCO3固体,观察到试管内壁均有水珠,结论:两种物质均受热分解。(_______)
10.除去Na2CO3固体中的NaHCO3固体可用灼烧的方法。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将一小块钠投入CuSO4溶液中,观察到的现象是__ (填序号)。
①钠浮于液面上;②熔化成小球;③发出嘶嘶的响声,放出气体;④有蓝色沉淀产生;⑤析出大量红色的铜。
请写出Na和H2O反应的离子方程式__ ,NaHCO3俗称__ ,写出NaHCO3和HCl反应的离子方程式__ 。
①钠浮于液面上;②熔化成小球;③发出嘶嘶的响声,放出气体;④有蓝色沉淀产生;⑤析出大量红色的铜。
请写出Na和H2O反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内。当胃酸过多时就会出现“咯酸水”“烧心”“胃部隐隐作痛”等症状。目前市场上的抗酸药主要有①吸收性抗酸药,如NaHCO3.②非吸收性抗酸药,如CaCO3、MgO、Al(OH)3。
(1)上述所举抗酸药中有_______ 个是电解质。
(2)写出NaHCO3在水溶液中的电离方程式_______ 。
(3)Al(OH)3作抗酸药时发生反应的离子方程式为_______ 。
(4)___ (填“可以”或“不可以”)服用BaCO3来治疗胃酸过多,理由是____ (用离子方程式表示)。
(1)上述所举抗酸药中有
(2)写出NaHCO3在水溶液中的电离方程式
(3)Al(OH)3作抗酸药时发生反应的离子方程式为
(4)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】取等物质的量浓度的NaOH溶液两份A和B,每份100 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol·L-1的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
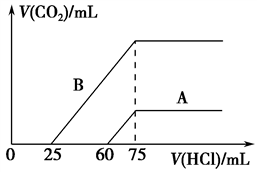
(1)原NaOH溶液的物质的量浓度为________ 。
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为________ L。
(3)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是________________ ,其物质的量之比为________ 。
(4)曲线B表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是________________ ,其物质的量之比为________ 。

(1)原NaOH溶液的物质的量浓度为
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为
(3)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是
(4)曲线B表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求回答下列问题:
(1)对含有K2CO3的样品进行焰色试验,需要准备的仪器和试剂有:铂丝、酒精灯、___________ 和___________ 。
(2)高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: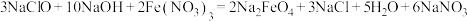 。回答下列问题:
。回答下列问题:
①用氯气制备 的反应原理为
的反应原理为___________ (化学方程式)
②制备高铁酸钠的反应中 体现了
体现了___________ (填“还原性”、“氧化性”或“氧化性和还原性”)
(3)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少了3.1g,所得固体与足量盐酸充分反应(假设CO2完全逸出)。计算:
①混合物中Na2CO3和NaHCO3的物质的量之比为___________ 。
②加入足量盐酸充分反应后产生的CO2在标准状况下的体积为___________ L。
(1)对含有K2CO3的样品进行焰色试验,需要准备的仪器和试剂有:铂丝、酒精灯、
(2)高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: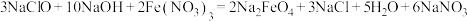 。回答下列问题:
。回答下列问题:①用氯气制备
 的反应原理为
的反应原理为②制备高铁酸钠的反应中
 体现了
体现了(3)加热13.7g碳酸钠和碳酸氢钠的固体混合物,使碳酸氢钠完全分解,混合物质量减少了3.1g,所得固体与足量盐酸充分反应(假设CO2完全逸出)。计算:
①混合物中Na2CO3和NaHCO3的物质的量之比为
②加入足量盐酸充分反应后产生的CO2在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)在密闭容器中加入NaHCO3和NaOH的混合物共18.4g,加热至300℃,经充分反应后排出气体,冷却得到剩余固体质量为16.6g。试确定混合物的组成:m(NaHCO3)=__ g。
(2)为测定镁铝合金的成分,取13.5g合金全部溶于500mL3mol/L的H2SO4中,充分反应后,再加入400mL8mol/L的NaOH溶液,结果得到了白色沉淀和滤液B。
①滤液B中n(NaAlO2)=__ mol。
②若白色沉淀只有一种成分,则合金中镁的质量分数范围为__ 。
(1)在密闭容器中加入NaHCO3和NaOH的混合物共18.4g,加热至300℃,经充分反应后排出气体,冷却得到剩余固体质量为16.6g。试确定混合物的组成:m(NaHCO3)=
(2)为测定镁铝合金的成分,取13.5g合金全部溶于500mL3mol/L的H2SO4中,充分反应后,再加入400mL8mol/L的NaOH溶液,结果得到了白色沉淀和滤液B。
①滤液B中n(NaAlO2)=
②若白色沉淀只有一种成分,则合金中镁的质量分数范围为
您最近一年使用:0次



