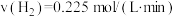用Na2FeO4溶液氧化废水中的还原性污染物M。为研究降解效果,设计如下对比实验探究温度、浓度、pH、催化剂对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示。
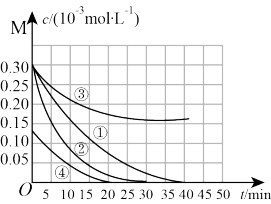
下列说法不正确的是
| 实验编号 | 温度/℃ | pH |
| ① | 25 | 1 |
| ② | 45 | 1 |
| ③ | 25 | 7 |
| ④ | 25 | 7 |

下列说法不正确的是
| A.实验①在0~15 min内M的平均降解速率为1.33×10-5 mol·L-1·min-1 |
| B.若其他条件相同,实验①②说明升高温度,M降解速率增大 |
| C.若其他条件相同,实验①③证明pH越高,越不利于M的降解 |
| D.实验①④说明M的浓度越小,降解的速率越快 |
更新时间:2021-10-26 20:30:23
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在一定条件下,将3 molA和 1 molB混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xCg)+2D(g)。2 min末该反应达到平衡,生成0.8 molD,得C的浓度为0.2mol/L,下列判断错误的是
xCg)+2D(g)。2 min末该反应达到平衡,生成0.8 molD,得C的浓度为0.2mol/L,下列判断错误的是
 xCg)+2D(g)。2 min末该反应达到平衡,生成0.8 molD,得C的浓度为0.2mol/L,下列判断错误的是
xCg)+2D(g)。2 min末该反应达到平衡,生成0.8 molD,得C的浓度为0.2mol/L,下列判断错误的是| A.x=1 |
| B.0~2min内A的平均反应速率为0.1mol/(L·min) |
| C.A的转化率为40% |
| D.若混合气体的平均相对分子质量不变,则表明该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在两个容积均为4L的恒容密闭容器中,起始时均充入0.4mol乙苯,以温度、催化剂为实验条件变量,发生反应:
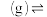
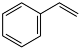
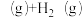 。测得的结果如图所示。曲线Ⅱ、Ⅲ表示经过相同时间ts且未达到化学平衡时乙苯的转化率,下列说法正确的是
。测得的结果如图所示。曲线Ⅱ、Ⅲ表示经过相同时间ts且未达到化学平衡时乙苯的转化率,下列说法正确的是


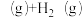 。测得的结果如图所示。曲线Ⅱ、Ⅲ表示经过相同时间ts且未达到化学平衡时乙苯的转化率,下列说法正确的是
。测得的结果如图所示。曲线Ⅱ、Ⅲ表示经过相同时间ts且未达到化学平衡时乙苯的转化率,下列说法正确的是
A.900℃时,无催化剂的容器中,ts内H2的平均反应速率为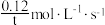 |
| B.1000℃时,有催化剂的容器中,延长反应时间乙苯的转化率可到达A点 |
| C.1100℃时,曲线Ⅱ、Ⅲ几乎重合,可能是因为催化剂失活 |
| D.其他条件不变时,升高温度或减小压强均能使平衡向右移动,均能使平衡常数K增大 |
您最近一年使用:0次
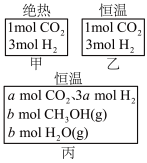
【推荐1】在初始温度为500℃、容积恒定为10L的三个密闭容器中,按图所示投入原料,发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H=-25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析不正确的是
CH3OH(g)+H2O(g) △H=-25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析不正确的是
 CH3OH(g)+H2O(g) △H=-25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析不正确的是
CH3OH(g)+H2O(g) △H=-25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析不正确的是
| A.刚开始反应时速率:甲=乙 |
| B.平衡后反应放热:甲<乙 |
| C.500℃时乙容器中反应的平衡常数:K=3×102 |
| D.若a≠0,则0.9<b<l |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】 选择性催化还原
选择性催化还原 的反应为
的反应为 ,其反应历程如图所示。一定温度下,向恒容密闭容器中充入一定量的
,其反应历程如图所示。一定温度下,向恒容密闭容器中充入一定量的 、
、 和
和 ,发生反应。下列说法错误的是
,发生反应。下列说法错误的是
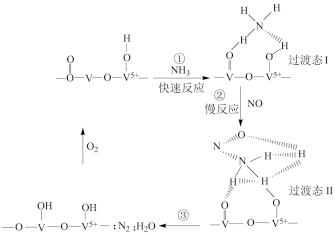
 选择性催化还原
选择性催化还原 的反应为
的反应为 ,其反应历程如图所示。一定温度下,向恒容密闭容器中充入一定量的
,其反应历程如图所示。一定温度下,向恒容密闭容器中充入一定量的 、
、 和
和 ,发生反应。下列说法错误的是
,发生反应。下列说法错误的是
A.使用催化剂, 、 、 的活化分子数增多,还原 的活化分子数增多,还原 的速率加快 的速率加快 |
| B.①的反应速率快,说明反应①的活化能大,是整个反应的决速步 |
C. 与催化剂发生强的化学吸附,而 与催化剂发生强的化学吸附,而 在此过程中几乎不被催化剂吸附 在此过程中几乎不被催化剂吸附 |
D.其他条件不变时,增大 的浓度,能使更多的 的浓度,能使更多的 转化为 转化为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】对利用甲烷消除 污染进行研究,
污染进行研究,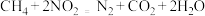 。在1L密闭容器中,控制不同温度,分别加入
。在1L密闭容器中,控制不同温度,分别加入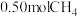 和
和 ,测得
,测得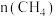 随时间变化的有关实验数据见下表。
随时间变化的有关实验数据见下表。
下列说法正确的是
 污染进行研究,
污染进行研究,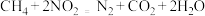 。在1L密闭容器中,控制不同温度,分别加入
。在1L密闭容器中,控制不同温度,分别加入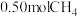 和
和 ,测得
,测得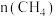 随时间变化的有关实验数据见下表。
随时间变化的有关实验数据见下表。| 组别 | 温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
| ① |  | 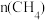 | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② |  | 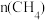 | 0.50 | 0.30 | 0.18 | 0.15 |
下列说法正确的是
A.组别①中,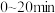 内, 内, 的降解速率为 的降解速率为 |
B.由实验数据可知实验控制的温度 |
C.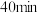 时,表格中 时,表格中 对应的数据为介于0.18-0.15之间 对应的数据为介于0.18-0.15之间 |
D. 内, 内, 的降解速率①>② 的降解速率①>② |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】向体积均为2L的A、B、C三个密闭容器中分别充入1molX气体和3molY气体,发生反应: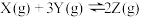 。2min后反应达到最大限度,测得A中剩余0.4molX,B中用Z表示的反应速率为v(Z)=0.3 mol/(L·min),C中Y的浓度为0.5mol/L。则0~2min内三个容器中反应速率的大小关系为
。2min后反应达到最大限度,测得A中剩余0.4molX,B中用Z表示的反应速率为v(Z)=0.3 mol/(L·min),C中Y的浓度为0.5mol/L。则0~2min内三个容器中反应速率的大小关系为
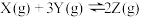 。2min后反应达到最大限度,测得A中剩余0.4molX,B中用Z表示的反应速率为v(Z)=0.3 mol/(L·min),C中Y的浓度为0.5mol/L。则0~2min内三个容器中反应速率的大小关系为
。2min后反应达到最大限度,测得A中剩余0.4molX,B中用Z表示的反应速率为v(Z)=0.3 mol/(L·min),C中Y的浓度为0.5mol/L。则0~2min内三个容器中反应速率的大小关系为| A.B>A>C | B.C>A=B | C.B>A=C | D.A>B>C |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用铁片与稀硫酸反应制取氢气时,下列措施可以加快氢气生成的是
| A.加入少量的醋酸钾固体 | B.加入浓硝酸 |
| C.滴加少量硫酸铜溶液 | D.改用浓硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室用锌与稀硫酸反应制取H2,欲使产生H2的速率加快,下列措施可行的是( )
| A.加水稀释 | B.加少量NaOH溶液 | C.降低温度 | D.锌片改为锌粉 |
您最近一年使用:0次
【推荐3】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 有白色沉淀生成,溶液红色变浅 | 证明纯碱溶液呈碱性是由 水解引起的 水解引起的 |
| B | 室温下,用pH试纸测定浓度均为0.1mol/L的NaClO溶液、CH3COONa溶液pH | NaClO溶液的pH较大 | 酸性:HClO<CH3COOH |
| C | 向1mL 0.1mol/LNaOH溶液中滴入2滴0.1mol/L MgCl2溶液,再滴入2滴0.1mol/L CuSO4溶液 | 沉淀颜色变化:白色—蓝色 | Ksp:Cu(OH)2<Mg(OH)2 |
| D | 分别向两支试管中加入同浓度、同体积的草酸溶液,再分别加入同体积、不同浓度的酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色时间不同 | 浓度不同反应速率不同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

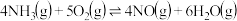 ,若反应速率分别是
,若反应速率分别是 、
、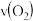 、
、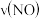 、
、 单位:
单位: 。下列反应速率的关系正确的是
。下列反应速率的关系正确的是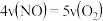
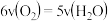
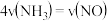
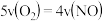
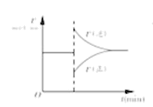 中的曲线可以表示某化学平衡体系改变温度后反应速率随时间的变化
中的曲线可以表示某化学平衡体系改变温度后反应速率随时间的变化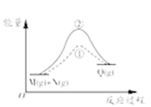 中①、②曲线分别表示反应M(g)+N(g)→Q(g),ΔH>0使用和未使用催化剂时,反应过程中的能量变化
中①、②曲线分别表示反应M(g)+N(g)→Q(g),ΔH>0使用和未使用催化剂时,反应过程中的能量变化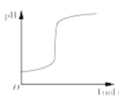 中的曲线可表示向一定量的氢氧化钠溶液中滴加一定浓度盐酸时的pH变化
中的曲线可表示向一定量的氢氧化钠溶液中滴加一定浓度盐酸时的pH变化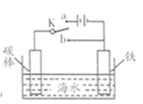 中开关K置于a或b处均可减缓铁的腐蚀
中开关K置于a或b处均可减缓铁的腐蚀 转化为甲醇的原理为
转化为甲醇的原理为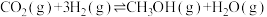
 。500℃时,在体积为1L的固定容积的密闭容器中充入1 mol
。500℃时,在体积为1L的固定容积的密闭容器中充入1 mol  ,测得
,测得 浓度随时间的变化如图所示,下列结论错误的是
浓度随时间的变化如图所示,下列结论错误的是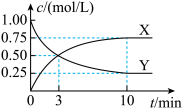

 可以表示
可以表示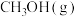 或
或 的浓度变化
的浓度变化