(1)高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学反应原理如下:
是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学反应原理如下:
 。请回答下列问题:
。请回答下列问题:
① 发生
发生______________ 反应,1个 得到
得到_____________ 个电子。
②反应时被氧化的元素是___________ (填名称),还原剂是_________________ (写化学式);氧化剂与还原剂离子数之比为_________________ 。
③生成2个 时,转移电子数为
时,转移电子数为____________________ 。
④用单线桥表示该反应转移电子的方向与数目________________ 。
(2)用“双线桥”法标出反应 的电子转移的方向与数目:
的电子转移的方向与数目: ________________ 。
(3)写出实验室制备 胶体的化学反应方程式
胶体的化学反应方程式_________________________ 。
 是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学反应原理如下:
是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学反应原理如下: 。请回答下列问题:
。请回答下列问题:①
 发生
发生 得到
得到②反应时被氧化的元素是
③生成2个
 时,转移电子数为
时,转移电子数为④用单线桥表示该反应转移电子的方向与数目
(2)用“双线桥”法标出反应
 的电子转移的方向与数目:
的电子转移的方向与数目: (3)写出实验室制备
 胶体的化学反应方程式
胶体的化学反应方程式
更新时间:2021-11-06 16:02:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)实验室制取Fe(OH)3胶体的操作方法是______________________ ;证明胶体已经制成的方法是_____________________________________________
(2)将(1)中所得分散系装入U形管内,用石墨作电极,接通直流电源,通电一段时间后发现阴极附近颜色___________ ,这表明_____________ ,这种现象称为_________
(3)提纯此分散系的方法叫__________ ,胶体与其它分散系的根本区别是_____
(2)将(1)中所得分散系装入U形管内,用石墨作电极,接通直流电源,通电一段时间后发现阴极附近颜色
(3)提纯此分散系的方法叫
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】玻璃棒是中学化学实验中常用的仪器。下列实验过程中,一般不需要用玻璃棒的是__ (填写编号)
①粗盐提纯
②配制一定物质的量浓度的氯化钠溶液
③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体
④探究Ba(OH)2•8H2O晶体和NH4Cl晶体反应过程中的能量变化
⑤实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
①粗盐提纯
②配制一定物质的量浓度的氯化钠溶液
③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体
④探究Ba(OH)2•8H2O晶体和NH4Cl晶体反应过程中的能量变化
⑤实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】关于铁化合物性质的探究。
(1)向少量Fe2O3粉末中加入适量盐酸,反应的化学方程式为_____ ;反应后得到的FeCl3溶液呈棕黄色,用此溶液进行以下实验:
(2)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为____ 。
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈_____ 色,即可制得Fe(OH)3胶体。
(4)取另一烧杯也加入20mL蒸馏水后,向烧杯中加入1mlL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到_____ (填编号)烧杯中的液体会产生丁达尔效应.这个实验可以用来区别_____ 。
(5)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,实验现象为:_______ ,试对以上现象作出合理的解释:___ 。
(1)向少量Fe2O3粉末中加入适量盐酸,反应的化学方程式为
(2)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈
(4)取另一烧杯也加入20mL蒸馏水后,向烧杯中加入1mlL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到
(5)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,实验现象为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】NA为阿伏加德罗常数的值。下列说法正确的是___________ 。
A.22.4LCl2(标准状况)与水充分反应转移1mol电子
B.1L0.1mol·L-1的Na2CO3溶液含 的数目为0.1NA
的数目为0.1NA
C.0.1molCH4与足量Cl2反应生成CH3Cl的分子数为0.1NA
D.1LpH=4的0.1mol·L-1K2Cr2O7溶液中Cr2O 离子数为0.1NA
离子数为0.1NA
E.2molNO与1molO2在密闭容器中充分反应后的分子数为2NA
F.11.2LCH4和22.4LCl2(均为标准状况)在光照下充分反应后的分子数为1.5NA
G.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
H.2.0L1.0mol·L-1AlCl3溶液中,Al3+的数目为2.0NA
I.0.1molH2和0.1molI2于密闭容器中充分反应后,其分子总数为0.2NA
A.22.4LCl2(标准状况)与水充分反应转移1mol电子
B.1L0.1mol·L-1的Na2CO3溶液含
 的数目为0.1NA
的数目为0.1NAC.0.1molCH4与足量Cl2反应生成CH3Cl的分子数为0.1NA
D.1LpH=4的0.1mol·L-1K2Cr2O7溶液中Cr2O
 离子数为0.1NA
离子数为0.1NAE.2molNO与1molO2在密闭容器中充分反应后的分子数为2NA
F.11.2LCH4和22.4LCl2(均为标准状况)在光照下充分反应后的分子数为1.5NA
G.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
H.2.0L1.0mol·L-1AlCl3溶液中,Al3+的数目为2.0NA
I.0.1molH2和0.1molI2于密闭容器中充分反应后,其分子总数为0.2NA
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】高锰酸钾是一种强氧化剂,具有很好的消炎、杀菌、抑菌的作用,因此临床上可以用于急性皮炎、湿疹、皮肤感染等疾病的治疗。
回答下列问题:
(1)某高锰酸钾外用片的部分使用说明及注意事项如下:
①高锰酸钾外用片可以治疗皮肤感染,是应用了高锰酸钾的___________ 性。
②高锰酸钾水溶液易变质的原因是___________ 。
③高锰酸钾外用片不可与碘化物接触或并用的原因是___________ 。
(2)将 溶液酸化可制得
溶液酸化可制得 ,同时生成
,同时生成 ,在此反应中氧化剂和还原剂的物质的量之比为
,在此反应中氧化剂和还原剂的物质的量之比为___________ ;当生成0.1mol还原产物时转移电子的数目为___________ 。
回答下列问题:
(1)某高锰酸钾外用片的部分使用说明及注意事项如下:
| 【注意事项】 1.本品仅供外用,切忌口服。 2.本品水溶液易变质,故使用前用温水配制,并立即使用。 【药品相互作用】 不可与碘化物、有机物接触或并用,尤其是晶体。 |
①高锰酸钾外用片可以治疗皮肤感染,是应用了高锰酸钾的
②高锰酸钾水溶液易变质的原因是
③高锰酸钾外用片不可与碘化物接触或并用的原因是
(2)将
 溶液酸化可制得
溶液酸化可制得 ,同时生成
,同时生成 ,在此反应中氧化剂和还原剂的物质的量之比为
,在此反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请按要求回答下列问题:
(1)氯气和水反应的化学方程式:___________ 。
(2)长期置于空气中的钠,最后形成的物质与氢氧化钡溶液混合后,发生反应的离子方程式为:___________ 。
(3)现有8种物质:①熔融 ②氯气③
②氯气③ ④葡萄糖⑤
④葡萄糖⑤ ⑥稀硫酸⑦
⑥稀硫酸⑦ ⑧
⑧ 。属于电解质的是
。属于电解质的是___________ ,能导电是___________ 。
(4)高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
)是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
①该反应的还原剂是___________ ;
②若生成1
 ,则反应转移的电子数为
,则反应转移的电子数为___________  。
。
(1)氯气和水反应的化学方程式:
(2)长期置于空气中的钠,最后形成的物质与氢氧化钡溶液混合后,发生反应的离子方程式为:
(3)现有8种物质:①熔融
 ②氯气③
②氯气③ ④葡萄糖⑤
④葡萄糖⑤ ⑥稀硫酸⑦
⑥稀硫酸⑦ ⑧
⑧ 。属于电解质的是
。属于电解质的是(4)高铁酸钠(
 )是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
)是一种新型绿色消毒剂,主要用于饮用水处理。一种工业制备高铁酸钠的化学反应原理如下:
①该反应的还原剂是
②若生成1

 ,则反应转移的电子数为
,则反应转移的电子数为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.化学反应按照不同的分类方法,可以分为化合反应、分解反应、置换反应、复分解反应,也可分为氧化还原反应和非氧化还原反应。有下列一组反应:
①CO2+C 2CO
2CO
②Cu2(OH)2CO3 2CuO+H2O+CO2↑
2CuO+H2O+CO2↑
③2NaOH+Cl2=NaCl+NaClO+H2O
④2CO+O2 2CO2
2CO2
⑤3Fe+4H2O(g) Fe3O4+4H2
Fe3O4+4H2
⑥CuO+CO Cu+CO2
Cu+CO2
⑦4NH3+3O2 2N2+6H2O
2N2+6H2O
⑧2H2O 2H2↑+O2↑
2H2↑+O2↑
⑨2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
⑩CO2+H2O=H2CO3
(1)其中属于化合反应的有________ (填序号,下同),属于置换反应的有________ 。
(2)在化学反应前后元素的化合价没有变化的是________ 。
(3)上述反应中,既是分解反应,又是氧化还原反应的是________ 。
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是________ 。
(5)根据你的理解,氧化还原反应的实质是 (填字母)。
Ⅱ.饮用水中的NO 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH+18H2O=10Na[Al(OH)4]+3N2↑。
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH+18H2O=10Na[Al(OH)4]+3N2↑。
请回答下列问题:
(6)上述反应中,________ 元素的化合价升高,则该元素的原子________ (填“得到”或“失去”)电子;而________ 元素的化合价降低,该元素发生________ 反应。
(7)用双线桥法表示反应中电子转移的方向和数目:_____________ 。
①CO2+C
 2CO
2CO②Cu2(OH)2CO3
 2CuO+H2O+CO2↑
2CuO+H2O+CO2↑③2NaOH+Cl2=NaCl+NaClO+H2O
④2CO+O2
 2CO2
2CO2⑤3Fe+4H2O(g)
 Fe3O4+4H2
Fe3O4+4H2⑥CuO+CO
 Cu+CO2
Cu+CO2⑦4NH3+3O2
 2N2+6H2O
2N2+6H2O⑧2H2O
 2H2↑+O2↑
2H2↑+O2↑⑨2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
⑩CO2+H2O=H2CO3
(1)其中属于化合反应的有
(2)在化学反应前后元素的化合价没有变化的是
(3)上述反应中,既是分解反应,又是氧化还原反应的是
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是
(5)根据你的理解,氧化还原反应的实质是 (填字母)。
| A.分子中的原子重新组合 |
| B.氧元素的得失 |
| C.电子的得失或共用电子对的偏移 |
| D.化合价的改变 |
Ⅱ.饮用水中的NO
 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH+18H2O=10Na[Al(OH)4]+3N2↑。
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH+18H2O=10Na[Al(OH)4]+3N2↑。请回答下列问题:
(6)上述反应中,
(7)用双线桥法表示反应中电子转移的方向和数目:
您最近一年使用:0次
【推荐2】某反应中反应物与生成物有:KMnO4、H2O2、H2SO4、O2、K2SO4、H2O和一种未知物质X。
(1)已知KMnO4在反应中得到电子,则该反应的还原剂是_______________ 。
(2)已知0.2mol KMnO4在反应中得到1mol电子生成X,则X的化学式为______________ 。
(3)根据上述反应可推知(在该条件下)__________ 。
a.氧化性:KMnO4>O2 b.氧化性: O2> KMnO4
c.还原性:H2O2>X d.还原性:X>H2O2
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:______

(1)已知KMnO4在反应中得到电子,则该反应的还原剂是
(2)已知0.2mol KMnO4在反应中得到1mol电子生成X,则X的化学式为
(3)根据上述反应可推知(在该条件下)
a.氧化性:KMnO4>O2 b.氧化性: O2> KMnO4
c.还原性:H2O2>X d.还原性:X>H2O2
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:

您最近一年使用:0次
【推荐3】FeCl3是一种用途比较广泛的盐。
(1)印刷电路板是由高分子材料和铜箔复合而成。刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。请写出反应的离子方程式____________________ 。Cu放入0.1 mol/L FeCl3溶液中,反应一段时间后取出Cu片,溶液中Fe3+与Fe2+的物质的量浓度之比为4∶3,则反应后溶液中Cu2+与Fe3+的物质的量之比为( )
A.3∶2 B.3∶8 C.4∶3 D.3∶4
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速度高于铝盐(如硫酸铝等),是城市污水及工业废水处理的高效絮凝剂。实验室制取氢氧化铁胶体的方法是________ (填字母序号)。
A.将饱和的FeCl3溶液滴入沸水中,生成棕黄色液体即可
B.在FeCl3溶液中加入足量的NaOH溶液
C.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色液体
D.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色沉淀
证明此胶体已经制成的最简单方法为____________________________________ 。
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式如下:2FeCl3+2KI===2FeCl2+I2+2KI在上式中用双线桥法标出该反应电子转移的方向和数目__________________ 。向反应后的溶液中加入CCl4溶液,振荡、静置后会发现下层液体的颜色为 ________ 色,再将混合液倒入________ (填仪器名称)中,将两层液体分离。
(1)印刷电路板是由高分子材料和铜箔复合而成。刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。请写出反应的离子方程式
A.3∶2 B.3∶8 C.4∶3 D.3∶4
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速度高于铝盐(如硫酸铝等),是城市污水及工业废水处理的高效絮凝剂。实验室制取氢氧化铁胶体的方法是
A.将饱和的FeCl3溶液滴入沸水中,生成棕黄色液体即可
B.在FeCl3溶液中加入足量的NaOH溶液
C.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色液体
D.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色沉淀
证明此胶体已经制成的最简单方法为
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式如下:2FeCl3+2KI===2FeCl2+I2+2KI在上式中用双线桥法标出该反应电子转移的方向和数目
您最近一年使用:0次
【推荐1】实验室常用KMnO4和浓盐酸制备Cl2,反应的化学方程式如下:

(1)该反应的氧化剂是________ (填化学式),还原产物是________ (填化学式)。
(2)由反应可知,氧化性:KMnO4___________ Cl2 (填“>”或“<”)。
(3)当反应生成71 g Cl2时,转移电子的物质的量是___________ mol。

(1)该反应的氧化剂是
(2)由反应可知,氧化性:KMnO4
(3)当反应生成71 g Cl2时,转移电子的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。现有下列两种制备ClO2的方法:
(1)方法一:可用亚氯酸钠和稀盐酸为原料制备,反应原理为5NaClO2+4HCl===5NaCl+4ClO2↑+2H2O。
①该反应中氧化剂和还原剂的物质的量之比是________ 。
②研究表明:若反应开始时盐酸浓度较大,则气体产物中有Cl2,用离子方程式解释产生Cl2的原因______ 。
(2)方法二:氯化钠电解法。
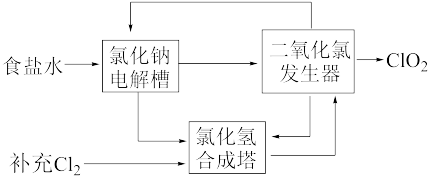
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO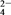 等杂质。某次除杂操作时,往粗盐水中先加入过量的
等杂质。某次除杂操作时,往粗盐水中先加入过量的_____ (填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。
②该法工艺原理示意图如图所示。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2,氯化钠电解槽中阳极反应方程式为__________________ ,二氧化氯发生器中生成ClO2的化学方程式为_______________________ 。
(1)方法一:可用亚氯酸钠和稀盐酸为原料制备,反应原理为5NaClO2+4HCl===5NaCl+4ClO2↑+2H2O。
①该反应中氧化剂和还原剂的物质的量之比是
②研究表明:若反应开始时盐酸浓度较大,则气体产物中有Cl2,用离子方程式解释产生Cl2的原因
(2)方法二:氯化钠电解法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO
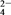 等杂质。某次除杂操作时,往粗盐水中先加入过量的
等杂质。某次除杂操作时,往粗盐水中先加入过量的②该法工艺原理示意图如图所示。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2,氯化钠电解槽中阳极反应方程式为

您最近一年使用:0次



