在容积为 的密闭容器中进行如下反应:
的密闭容器中进行如下反应: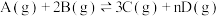 ,开始时
,开始时 为
为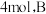 为
为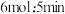 末达到平衡,测得
末达到平衡,测得 为
为 ,用
,用 表示的化学反应速率
表示的化学反应速率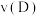 为
为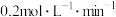 。
。
试回答下列问题:
(1) 末
末 的物质的量浓度为
的物质的量浓度为___________ ,平衡后A的转化率为___________ 。
(2) 内用
内用 表示的化学反应速率
表示的化学反应速率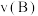 为
为___________ 。
(3)化学方程式中 为
为___________ 。
(4)反应达到平衡时压强与起始压强之比为___________ 。
 的密闭容器中进行如下反应:
的密闭容器中进行如下反应: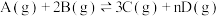 ,开始时
,开始时 为
为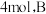 为
为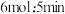 末达到平衡,测得
末达到平衡,测得 为
为 ,用
,用 表示的化学反应速率
表示的化学反应速率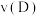 为
为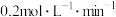 。
。试回答下列问题:
(1)
 末
末 的物质的量浓度为
的物质的量浓度为(2)
 内用
内用 表示的化学反应速率
表示的化学反应速率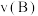 为
为(3)化学方程式中
 为
为(4)反应达到平衡时压强与起始压强之比为
更新时间:2021-11-07 10:04:03
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】气体A.B置于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌2C(g)+2D(g),反应进行到10s末,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
(1)用C表示10s内反应的平均反应速率为_______ ;
(2)反应前A的物质的量浓度是_______ ;10s末,生成物D的浓度为_______ ;
(3)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。原因是_______ 。实验室中现有Na2SO4、MgSO4、FeSO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是_______ 。
(4)目前工业制氢气的一个重要过程如图,则该反应的热化学方程式为:_______
过程Ⅱ是加入催化剂后的反应过程,则过程Ⅰ和Ⅱ的反应热_______ (填“相等”或“不相等”)。

(1)用C表示10s内反应的平均反应速率为
(2)反应前A的物质的量浓度是
(3)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。原因是
(4)目前工业制氢气的一个重要过程如图,则该反应的热化学方程式为:
过程Ⅱ是加入催化剂后的反应过程,则过程Ⅰ和Ⅱ的反应热

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】一定温度下,在容积为VL的密闭容器里进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:

(1)此反应的化学方程式中a∶b =__________________ 。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:__________________ 。
(3)t1时N的转化率为:_______________ ;
(4)下列①→⑩的说法中可以证明 H2(g)+I2(g) 2HI(g)已达平衡状态的是:
2HI(g)已达平衡状态的是:___________ 。
①单位时间内生成n molH2的同时生成n mol HI
②一个H-H 键断裂的同时有两个H-I键断裂
③质量分数:w(HI)=w(I2)
④容器内HI(g)、H2 (g) 、I2 (g)共存
⑤c(HI): c(H2): c(I2)=2:1:1
⑥温度和体积一定时,容器内压强不再变化
⑦温度和体积一定时,HI(g)浓度不再变化
⑧温度和压强一定时,混合气体的平均摩尔质量不再变化
⑨温度和压强一定时,混合气体的颜色不再发生变化
⑩温度和压强一定时,混合气体的密度不再变化
 bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中a∶b =
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:
(3)t1时N的转化率为:
(4)下列①→⑩的说法中可以证明 H2(g)+I2(g)
 2HI(g)已达平衡状态的是:
2HI(g)已达平衡状态的是:①单位时间内生成n molH2的同时生成n mol HI
②一个H-H 键断裂的同时有两个H-I键断裂
③质量分数:w(HI)=w(I2)
④容器内HI(g)、H2 (g) 、I2 (g)共存
⑤c(HI): c(H2): c(I2)=2:1:1
⑥温度和体积一定时,容器内压强不再变化
⑦温度和体积一定时,HI(g)浓度不再变化
⑧温度和压强一定时,混合气体的平均摩尔质量不再变化
⑨温度和压强一定时,混合气体的颜色不再发生变化
⑩温度和压强一定时,混合气体的密度不再变化
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.已知:反应aA(g)+bB(g) cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
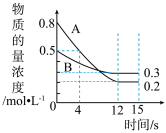
(1)经测4s时间,v(C)=0.05mol·L-1·s-1,则4s时物质C的物质的量为___________________ ,该反应的化学方程式为______________________ 。
(2)经12s时间,v(A)=___________ ,v(C)=___________ ,该反应12s时___________ 达到化学平衡(“是”或“否”)。
Ⅱ.(3)下列说法可以证明H2(g)+I2(g) 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是________ (填序号)。
A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)= v(HI)
v(HI)
 cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
(1)经测4s时间,v(C)=0.05mol·L-1·s-1,则4s时物质C的物质的量为
(2)经12s时间,v(A)=
Ⅱ.(3)下列说法可以证明H2(g)+I2(g)
 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=
 v(HI)
v(HI)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答问题:
(1)以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池中:
①H+向___________ 极移动(填“正”或“负”)。
②电子流动方向由____________ 极流向____________ 极(填:“正”、“负”)。
③若有1mole- 流过导线,则理论上负极质量减少____________ g。
④若将稀硫酸换成硫酸铜溶液,电极质量增加的是___________ (填“锌极”或“铜极”),原因是_____________ (用电极方程式表示)。
(2)一定温度下,在容积为2 L的密闭容器中进行反应:aN(g) bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:

①反应化学方程式中各物质的系数比为a∶b∶c=_________ 。
②1 min到3 min这段时刻,以M的浓度变化表示的平均反应速率为:_____________ 。
③下列叙述中能说明上述反应达到平衡状态的是____________________________ 。
A.反应中当M与N的物质的量相等时
B.混合气体的总物质的量不随时间变化而变化
C.单位时间内每消耗amolN,同时消耗bmolM
D.混合气体的压强不随时间的变化而变化
E.M的物质的量浓度保持不变
(1)以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池中:
①H+向
②电子流动方向由
③若有1mole- 流过导线,则理论上负极质量减少
④若将稀硫酸换成硫酸铜溶液,电极质量增加的是
(2)一定温度下,在容积为2 L的密闭容器中进行反应:aN(g)
 bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
①反应化学方程式中各物质的系数比为a∶b∶c=
②1 min到3 min这段时刻,以M的浓度变化表示的平均反应速率为:
③下列叙述中能说明上述反应达到平衡状态的是
A.反应中当M与N的物质的量相等时
B.混合气体的总物质的量不随时间变化而变化
C.单位时间内每消耗amolN,同时消耗bmolM
D.混合气体的压强不随时间的变化而变化
E.M的物质的量浓度保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)⇌3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的体积分数为50%,D的化学反应速率v(D)=0.2mol/(L·min)。请回答:
(1)前5min内用B表示的化学反应速率v(B)为_______ ;
(2)前5min内A的转化率为_______ ;(转化率是指某一反应物的转化百分数)
(3)反应开始时与5min后容器内压强比为_______ ;
(4)5min后容器内混合气体平均相对分子质量比起始_______ (填“大”或“小”或“相等”)。
(5)某可逆反应在体积为5 L的密闭容器中进行,0~3 min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。能说明该反应已达到平衡状态的是_______ (填正确选项前的序号)。

①v(A)=2v(B)
②容器内压强保持不变
③2v逆(A)=v正(B)
④容器内混合气体的密度保持不变
⑤c(A):c(B):c(C)=2:1:2
⑥混合气体的平均相对分子质量保持不变
(1)前5min内用B表示的化学反应速率v(B)为
(2)前5min内A的转化率为
(3)反应开始时与5min后容器内压强比为
(4)5min后容器内混合气体平均相对分子质量比起始
(5)某可逆反应在体积为5 L的密闭容器中进行,0~3 min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。能说明该反应已达到平衡状态的是

①v(A)=2v(B)
②容器内压强保持不变
③2v逆(A)=v正(B)
④容器内混合气体的密度保持不变
⑤c(A):c(B):c(C)=2:1:2
⑥混合气体的平均相对分子质量保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在一定温度下,在一定条件下,将3 mol A和1 mol B 两种气体在容积固定的2 L密闭容器中混合,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g)。2 min 末时生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。
(1)x=_______ 。
(2)2min内A的反应速率为_______ 。
(3)B的转化率为_______ 。
(4)在不同条件下,用不同物质表示其反应速率,下其中最快的是_______
①v(A)=0.6mol·L-1·min-1
②v(B)=0.45mol·L-1·min-1
③v(D)=0.45mol·L-1·s-1
④v(D)=0.45mol·L-1·min-1
(5)恒容下,下列关于达到平衡时的有关表述正确的是_______ (填标号)。
①A气体已经完全转化为D气体
②A气体的生成速率为B气体消耗速率的3倍
③2v正(A)=3v逆(D)
④c(A)∶c(B)=3∶1
⑤气体的压强不再改变
⑥气体的密度不再改变
⑦气体的平均相对分子质量不再改变
(1)x=
(2)2min内A的反应速率为
(3)B的转化率为
(4)在不同条件下,用不同物质表示其反应速率,下其中最快的是
①v(A)=0.6mol·L-1·min-1
②v(B)=0.45mol·L-1·min-1
③v(D)=0.45mol·L-1·s-1
④v(D)=0.45mol·L-1·min-1
(5)恒容下,下列关于达到平衡时的有关表述正确的是
①A气体已经完全转化为D气体
②A气体的生成速率为B气体消耗速率的3倍
③2v正(A)=3v逆(D)
④c(A)∶c(B)=3∶1
⑤气体的压强不再改变
⑥气体的密度不再改变
⑦气体的平均相对分子质量不再改变
您最近一年使用:0次
【推荐1】利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。已知:SO2(g)+1/2O2(g)⇌SO3(g) ∆H=-98 kJ·mol-1。
(1)在定温定容下进行该反应,下列可以判断该反应达到平衡状态的标志是_____ 。(填字母)
a.SO2和SO3浓度相等 b.SO2百分含量保持不变 c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等 e.容器中混合气体的密度保持不变
(2)欲提高SO2的平衡转化率,下列措施可行的是_______ 。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(3)一定温度下,向一带活塞的体积为2L的密闭容器中充入2.0molSO2和1.0molO2,达到平衡后体积变为1.6L,则SO2的平衡转化率为________ 。
(4)在(3)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是____ (填字母)。
a.保持温度和容器体积不变,充入1.0molO2
b.保持温度和容器内压强不变,充入1.0molSO3
c.降低温度
d.移动活塞压缩气体
(5)该反应中SO2的转化率的受温度和压强的影响的关系如表所示。

工业生产上,在400℃~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:_________ 。
(1)在定温定容下进行该反应,下列可以判断该反应达到平衡状态的标志是
a.SO2和SO3浓度相等 b.SO2百分含量保持不变 c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等 e.容器中混合气体的密度保持不变
(2)欲提高SO2的平衡转化率,下列措施可行的是
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(3)一定温度下,向一带活塞的体积为2L的密闭容器中充入2.0molSO2和1.0molO2,达到平衡后体积变为1.6L,则SO2的平衡转化率为
(4)在(3)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是
a.保持温度和容器体积不变,充入1.0molO2
b.保持温度和容器内压强不变,充入1.0molSO3
c.降低温度
d.移动活塞压缩气体
(5)该反应中SO2的转化率的受温度和压强的影响的关系如表所示。

工业生产上,在400℃~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g) CS2(g)+2H2S(g),某温度下,若S8完全分解成气态S2.在恒温密闭容器中,S2与CH4物质的量比为2∶1时开始反应。
CS2(g)+2H2S(g),某温度下,若S8完全分解成气态S2.在恒温密闭容器中,S2与CH4物质的量比为2∶1时开始反应。
(1)当CS2的体积分数为10%时,CH4的转化率为___________
(2)当以下数值不变时,能说明该反应达到平衡的是___________ (填序号)
a.气体密度 b.气体总压 c.CH4与S2体积比 d.CS2的体积分数
 CS2(g)+2H2S(g),某温度下,若S8完全分解成气态S2.在恒温密闭容器中,S2与CH4物质的量比为2∶1时开始反应。
CS2(g)+2H2S(g),某温度下,若S8完全分解成气态S2.在恒温密闭容器中,S2与CH4物质的量比为2∶1时开始反应。(1)当CS2的体积分数为10%时,CH4的转化率为
(2)当以下数值不变时,能说明该反应达到平衡的是
a.气体密度 b.气体总压 c.CH4与S2体积比 d.CS2的体积分数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】甲醇是重要的化工原料,应用前景广阔。研究表明,二氧化碳与氢气反应可以合成甲醇,反应如下:

(1)反应的平衡常数表达式为K=_____ 。
(2)有利于提高平衡时 转化率的措施有
转化率的措施有_____ (填字母)
a.使用催化剂 b.加压 c.增大 和
和 的初始投料比
的初始投料比
(3)研究温度对甲醇产率的影响发现,在210-290℃,保持原料气中 和
和 的初始投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的△H
的初始投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的△H _____ 0(填“>”“=”“<”),依据是_____ 。

(4)在恒温恒容条件下,增大体系的压强,平衡将向_____ 方向移动;若体系的平均摩尔质量不再发生变化,_____ (填“能”或“不能”)证明体系已达到化学平衡状态。

(1)反应的平衡常数表达式为K=
(2)有利于提高平衡时
 转化率的措施有
转化率的措施有a.使用催化剂 b.加压 c.增大
 和
和 的初始投料比
的初始投料比(3)研究温度对甲醇产率的影响发现,在210-290℃,保持原料气中
 和
和 的初始投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的△H
的初始投料比不变,得到平衡时甲醇的产率与温度的关系如图所示,则该反应的△H 
(4)在恒温恒容条件下,增大体系的压强,平衡将向
您最近一年使用:0次



