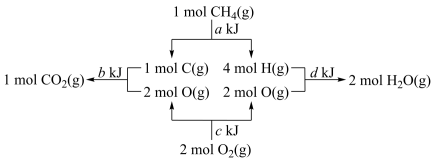
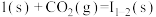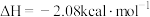某反应过程中的能量变化如图所示,下列热化学方程式正确的是

A.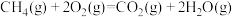 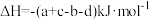 |
B.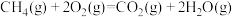  |
C.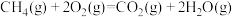 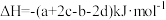 |
D.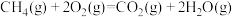 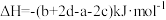 |
更新时间:2021-11-06 19:09:49
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列热化学方程式书写中正确的是(ΔH的绝对值均正确):
| A.表达燃烧热:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1367.0kJ·mol-1 |
| B.在500℃、30MPa条件下,将0.5molN2和1.5molH2置于密闭容器中充分反应后生成NH3(g)时放出19.3kJ热量,该热化学方程式为:N2(g)+3H2(g)⇌2NH3(g) ΔH=-38.6 kJ·mol-1 |
| C.表达中和热:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,据此可推出热化学方程式:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6kJ•mol﹣1 |
| D.已知热化学方程式:C(s)+O2(g)===CO2(g) ΔH1;C(s)+1/2O2(g)===CO(g) ΔH2;则ΔH1<ΔH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知辛烷的燃烧热为5518kJ·mol-1,强酸与强碱在稀溶液中发生反应时的中和热为57.3kJ·mol-1,则下列热化学方程式书写正确的是
①C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(g);△H=-5518kJ·mol-1
②2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l);△H=-11036kJ·mol-1
③H+(aq) + OH-(aq) =H2O(l); △H= +57.3kJ·mol-1
④2NaOH(aq) +H2SO4(aq)=Na2SO4(aq) + 2H2O(l);△H=-57.3kJ·mol-1
①C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(g);△H=-5518kJ·mol-1
②2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l);△H=-11036kJ·mol-1
③H+(aq) + OH-(aq) =H2O(l); △H= +57.3kJ·mol-1
④2NaOH(aq) +H2SO4(aq)=Na2SO4(aq) + 2H2O(l);△H=-57.3kJ·mol-1
| A.①③ | B.②③ | C.②④ | D.只有② |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】 和
和 均为重要的化工原料,都满足8电子结构
均为重要的化工原料,都满足8电子结构
已知:①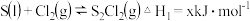
②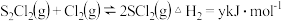
③相关化学键的键能如表所示:
下列说法错误的是
 和
和 均为重要的化工原料,都满足8电子结构
均为重要的化工原料,都满足8电子结构已知:①
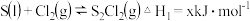
②
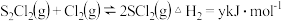
③相关化学键的键能如表所示:
| 化学键 | 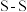 | 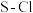 | 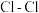 |
键能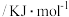 | a | b | c |

A.化学键的键能: |
B.以 的电子式为: 的电子式为: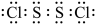 |
C.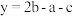 |
D.在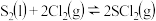 的反应中, 的反应中, |
您最近一年使用:0次
【推荐2】实验表明,在一定条件下,乙烯和水的反应可表示为:
C2H4(g) + H2O (g) = C2H5OH(g) ΔH = -45.8 kJ/mol
则下列说法中正确的是
C2H4(g) + H2O (g) = C2H5OH(g) ΔH = -45.8 kJ/mol
则下列说法中正确的是
| A.实验中,乙烯的用量不会影响该反应的反应焓变ΔH |
| B.0.5 mol H2O(l) 完全反应放出的热量为22.9 kJ |
| C.1 mol C2H5OH(g)具有的能量大于1 mol C2H4(g)和1 mol H2O (g)所具有的能量和 |
| D.1 mol C2H4(g)和1 mol H2O (g)中化学键的总键能大于1 mol C2H5OH(g)中化学键的总键能 |
您最近一年使用:0次

 氢化机理,其机理化合物l(固态催化剂)→化合物2(固态中间产物)的过程和其相对能量曲线如图所示。
氢化机理,其机理化合物l(固态催化剂)→化合物2(固态中间产物)的过程和其相对能量曲线如图所示。
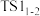 、
、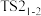 ,说明该过程包含两个基元反应
,说明该过程包含两个基元反应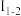 是该过程的中间产物
是该过程的中间产物