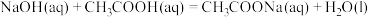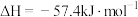下列说法或表示方法正确的是( )
A.在101kPa时,2 g  完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式为 完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式为  |
B.已知101kPa时,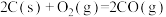 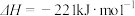 ,反应的反应热为 ,反应的反应热为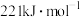 |
C.由C(s,石墨) (s,金刚石) (s,金刚石) 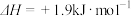 可知,石墨比金刚石稳定 可知,石墨比金刚石稳定 |
D.由:  ,可知:含1 mol ,可知:含1 mol  的溶液与含1 mo NaOH的溶液混合,放出热量为57.3kJ 的溶液与含1 mo NaOH的溶液混合,放出热量为57.3kJ |
更新时间:2021-11-09 15:05:10
|
相似题推荐
【推荐1】根据能量变化示意图,下列说法不正确的是( )
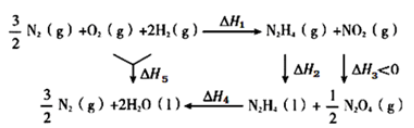
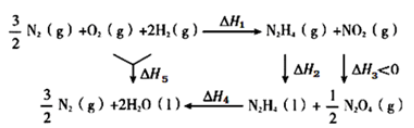
| A.相同质量的N2H4(g)和N2H4(l),前者具有的能量较高 |
| B.相同质量的NO2(g)和N2O4(g),后者含有的总键能较高 |
| C.ΔH5=ΔH1+ΔH2+ΔH3+ΔH4 |
D.N2H4(g)+NO2(g)= N2(g)+2H2O(l) ΔH,则ΔH>ΔH4 N2(g)+2H2O(l) ΔH,则ΔH>ΔH4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,下列叙述正确的是


| A.形成2molA-B键,吸收b kJ能量 |
| B.每生成2分子AB吸收bkJ热量 |
| C.反应物的总能量低于生成物的总能量 |
| D.该反应热ΔH=(b-a)kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】N2(g)与H2(g)化合生成NH3(g)的过程能量变化如下图所示,有关说法正确的是
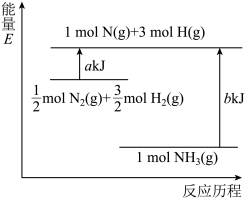

| A.使用催化剂会改变反应的热效应 |
B.反应的热化学方程式为:N2(g)+3H2(g) 2NH3(g)+2bkJ 2NH3(g)+2bkJ |
| C.1molN(g)和3molH(g)生成1molNH3(g)时,放出bkJ热量 |
| D.1molN2(g)和3molH2(g)的能量之和小于2molNH3(g)的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
A. 的燃烧热是890.3kJ/mol,则表示 的燃烧热是890.3kJ/mol,则表示 的燃烧热的热化学方程式为: 的燃烧热的热化学方程式为:  |
B.由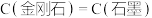 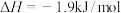 可知,石墨比金刚石稳定 可知,石墨比金刚石稳定 |
C.500℃、30MPa,将0.5mol 和1.5mol 和1.5mol 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 ,放热19.3kJ,其热化学方程式为: ,放热19.3kJ,其热化学方程式为:  |
D. 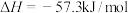 ,故1mol醋酸与1molNaOH完全反应,放出的热量一定为57.3kJ ,故1mol醋酸与1molNaOH完全反应,放出的热量一定为57.3kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】以一定浓度NaOH溶液吸收H2S可制备Na2S或NaHS。若通入H2S所引起的溶液体积变化和H2O挥发可忽略,溶液中含硫物种的浓度c总=c(H2S)+c(HS-)+c(S2-)。室温下,H2S的电离常数分别为Ka1=1.1×10-7、Ka2=1.3×10-13。下列说法正确的是
A.Na2S溶液显碱性的原因:S2-+2H2O H2S+2OH- H2S+2OH- |
| B.NaOH恰好转化为Na2S的溶液中:c(OH-)=c(H+)+c(HS-)+c(S2-) |
| C.吸收所得c总=c(Na+)的溶液中:c(H2S)>c(S2-) |
| D.NaOH溶液吸收H2S过程中,溶液的温度下降 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列按要求书写的热化学方程式正确的是(注:△H的绝对值均正确)
| A.C2H5OH(l)+3O2(g)=2CO2(g) +3H2O(g) △H= -1367.0 kJ/mol(燃烧热) |
| B.2NaOH(aq) + H2SO4(aq) = Na2SO4(aq) + 2H2O(l) △H= -114.6kJ/mol(中和热) |
| C.S(s) + O2(g) = SO2(g) △H= -269.8kJ/mol(反应热) |
| D.2NO2=O2+2NO △H= +116.2kJ/mol(反应热) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.化合反应都是放热反应,分解反应都是吸热反应 |
| B.吸热反应中反应物的键能总和大于生成物的键能总和 |
| C.1mol氢气在氯气中完全燃烧时所放出的热量是氢气的燃烧热 |
| D.稀醋酸与稀NaOH溶液反应生成1mol水放出的热量为57.3kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知氢气和碳燃烧的热化学方程式为:
①2H2(g)+O2(g)=2 H2O(1) ΔH1= -akJ/mol
②H2(g)+ O2(g)=H2O (g) ΔH2= -bkJ/mol
O2(g)=H2O (g) ΔH2= -bkJ/mol
③C(s)+ O2(g)=CO(g) ΔH3 = -ckJ/mol
O2(g)=CO(g) ΔH3 = -ckJ/mol
④C(s)+ O2 (g)=CO2(g) ΔH4= -dkJ/mol
下列说法正确的是
①2H2(g)+O2(g)=2 H2O(1) ΔH1= -akJ/mol
②H2(g)+
 O2(g)=H2O (g) ΔH2= -bkJ/mol
O2(g)=H2O (g) ΔH2= -bkJ/mol③C(s)+
 O2(g)=CO(g) ΔH3 = -ckJ/mol
O2(g)=CO(g) ΔH3 = -ckJ/mol④C(s)+ O2 (g)=CO2(g) ΔH4= -dkJ/mol
下列说法正确的是
| A.c>d | B.0.5a>b |
| C.氢气的燃烧热为ΔH= -bkJ/mol | D.CO(g)+ O2(g)= CO2(g) ΔH= -(c-d)kJ/mol. O2(g)= CO2(g) ΔH= -(c-d)kJ/mol. |
您最近一年使用:0次

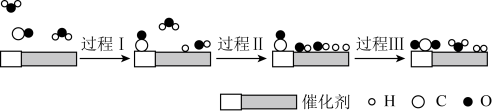
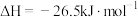 ,由此可知
,由此可知 气体在密闭容器中充分分解后可以放出
气体在密闭容器中充分分解后可以放出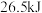 的热量
的热量
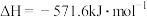 ,则氢气的摩尔燃烧焓为:
,则氢气的摩尔燃烧焓为:

 ,
,
 ,则
,则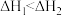
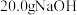 的稀溶液与稀盐酸完全中和,放出
的稀溶液与稀盐酸完全中和,放出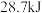 的热量,则稀醋酸和稀
的热量,则稀醋酸和稀 溶液反应的热化学方程式为:
溶液反应的热化学方程式为: