某校化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___________ 。
(2)装置V的作用是___________ 。
(3)若产生 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
① ②
② ③
③ ④
④
(5)有一种“地康法”制取氯气的反应原理如图所示:
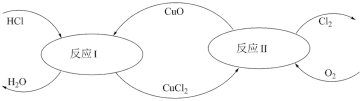
在450℃条件下,反应Ⅱ的化学方程式为___________ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
(1)装置Ⅰ中仪器c的名称是
(2)装置V的作用是
(3)若产生
 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的
①
 ②
② ③
③ ④
④
(5)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应Ⅱ的化学方程式为
更新时间:2021-11-10 08:58:29
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】下图是实验室制取、提纯氯气及研究氯气性质的装置图。请回答:
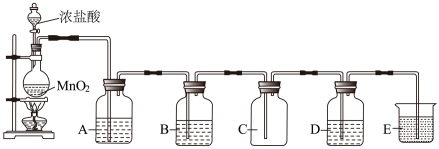
(1)装有浓盐酸的仪器的名称___________ ;A中一般应盛有___________ (填写试剂名称)。
(2)烧瓶中发生反应的化学方程式为___________ 。
(3)若D中盛有紫色石蕊试液,则D中的现象是___________ ,用离子方程式解释这种现象___________ 。
(4)若D中是FeCl2溶液,发生的现象是_______ ,反应的离子方程式为________ 。
(5)若D中盛有KI—淀粉的混合溶液,现象是___________ 。
(6)E中一般应盛有___________ ,其作用是___________ 。
(7)若有17.4gMnO2完全反应,则可生成标准状况下Cl2的体积_______ L。

(1)装有浓盐酸的仪器的名称
(2)烧瓶中发生反应的化学方程式为
(3)若D中盛有紫色石蕊试液,则D中的现象是
(4)若D中是FeCl2溶液,发生的现象是
(5)若D中盛有KI—淀粉的混合溶液,现象是
(6)E中一般应盛有
(7)若有17.4gMnO2完全反应,则可生成标准状况下Cl2的体积
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
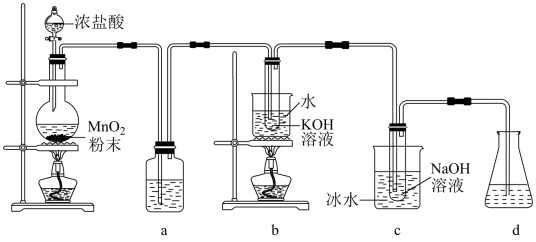
回答下列问题:
(1)盛放MnO2粉末的仪器名称是____ ,a中的试剂为____ 。b中采用的加热方式是____ ,c采用冰水浴冷却的目的是____ 。d的作用是____ ,d中盛放试剂为_____ 。
(2)反应结束后,取出b中试管,经冷却结晶,____ ,____ ,干燥,得到KClO3晶体。
(3)图中制取氯气的离子方程式为:____ ,标况下生成22.4L氯气时,被氧化的盐酸为____ mol,c中化学反应的离子方程式是____ 。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是
(2)反应结束后,取出b中试管,经冷却结晶,
(3)图中制取氯气的离子方程式为:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】我们已经学过氢气、氧气、二氧化碳、氯气、二氧化硫、氨气等气体的制备方法和化学性质.以下是实验室制备、洗涤、干燥气体及进行尾气处理的常见仪器装置.请结合所学知识回答下列问题:

(1)下列气体中,只能 用碱石灰干燥的是 ______ (填字母)
A.H2B.Cl2C.SO2D.O2
(2)实验室制取氯气反应原理的离子方程式是______ ,所选制备装置是______ 。检验氯气用______ 试纸;尾气处理的离子方程式为___________ 。
(3)实验室用氯化铵和熟石灰制取氨气,其化学反应方程式____________ 。工业上用氯气与石灰乳反应制备漂白粉的化学方程式为____________ 。

(1)下列气体中,
A.H2B.Cl2C.SO2D.O2
(2)实验室制取氯气反应原理的离子方程式是
(3)实验室用氯化铵和熟石灰制取氨气,其化学反应方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】K2FeO4为暗紫色有光泽的粉末,是一种新型绿色消毒剂,在实验室通过两步操作制备K2FeO4。回答下列问题:
I.制备KClO,装置如图:
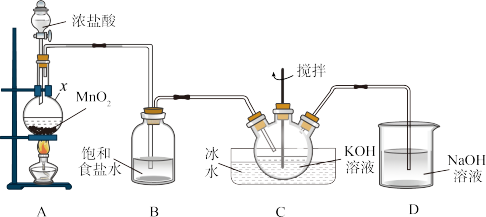
(1)仪器x的名称为_____ ,x中反应的化学方程式为_____ 。
(2)装置B的作用为_____ ;装置C中Cl2与KOH反应得到KClO,该反应离子方程式为_____ 。装置D的作用为____ 。
II.制备K2FeO4:
如图是某学生设计的实验室制备干燥Cl2及吸收多余氯气的实验装置图,请回答:
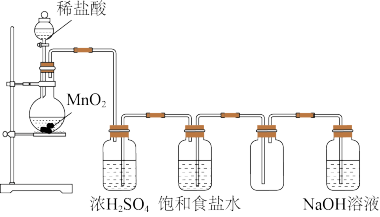
(3)指出上述图中的各处错误:①______ ;②_____ ;③_____ ;④_____ 。
(4)在改过后的装置中,下列物质的作用分别是:①饱和食盐水______ ;②浓硫酸______ ;③NaOH溶液_____ 。
(5)用NaOH溶液吸收多余尾气的离子方程式:______ 。
(6)待装置C中得到足量KClO后,将三口烧瓶上的导管取下,依次加入适量KOH溶液、Fe(NO3)3溶液并搅拌,控制水浴温度为25℃,得到紫色K2FeO4溶液,反应的离子方程式为3ClO-+2Fe3++10OH-=2FeO +3Cl-+5H2O。该过程中每制备1molK2FeO4,转移电子数目为
+3Cl-+5H2O。该过程中每制备1molK2FeO4,转移电子数目为_____ (用NA表示阿伏加德罗常数的值)。
I.制备KClO,装置如图:

(1)仪器x的名称为
(2)装置B的作用为
II.制备K2FeO4:
如图是某学生设计的实验室制备干燥Cl2及吸收多余氯气的实验装置图,请回答:

(3)指出上述图中的各处错误:①
(4)在改过后的装置中,下列物质的作用分别是:①饱和食盐水
(5)用NaOH溶液吸收多余尾气的离子方程式:
(6)待装置C中得到足量KClO后,将三口烧瓶上的导管取下,依次加入适量KOH溶液、Fe(NO3)3溶液并搅拌,控制水浴温度为25℃,得到紫色K2FeO4溶液,反应的离子方程式为3ClO-+2Fe3++10OH-=2FeO
 +3Cl-+5H2O。该过程中每制备1molK2FeO4,转移电子数目为
+3Cl-+5H2O。该过程中每制备1molK2FeO4,转移电子数目为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】如图是实验室制备氯气、收集并探究氯气是否有漂白性的装置。

据此回答下列问题:
(1)试剂X的成分是_______ ,盛放盐酸的仪器名称是_______ ,C中除观察到有气泡产生外,还可观察到的现象是_______ 。
(2)D装置用于收集Cl2,a、b两导管长度需要修改,修改的方法是_______ ,F中反应的离子方程式为_______ 。
(3)装置E的作用是验证氯气无漂白性但在水溶液中有漂白性,则装置中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是_______ ,相应的实验现象是_______ 。
(4)写出制备氯气的化学方程式_______ ,如果将40 mL、10 mol/L的浓盐酸与足量MnO2充分反应,实际能收集到的氯气在标准状况下的体积为_______ 。
A.2.24 L B.>2.24 L C.<2.24 L

据此回答下列问题:
(1)试剂X的成分是
(2)D装置用于收集Cl2,a、b两导管长度需要修改,修改的方法是
(3)装置E的作用是验证氯气无漂白性但在水溶液中有漂白性,则装置中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
| 序号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的石蕊试纸 | 碱石灰 | 湿润的石蕊试纸 |
| b | 干燥的石蕊试纸 | 无水氯化钙 | 湿润的石蕊试纸 |
| c | 湿润的石蕊试纸 | 浓硫酸 | 干燥的石蕊试纸 |
| d | 湿润的石蕊试纸 | 干燥的石蕊试纸 |
A.2.24 L B.>2.24 L C.<2.24 L
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室使用浓盐酸、二氧化锰共热制氯气,并用氯气和氢氧化钙反应制取少量漂白粉(该反应放热)。氯气和氢氧化钙在温度较高时会生成副产物氯酸钙,甲、乙、丙三位同学分别设计了三个实验装置如下图所示:
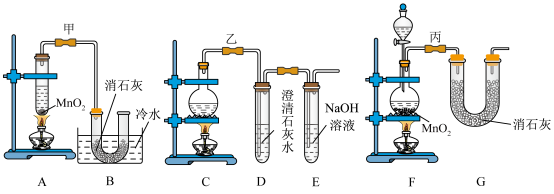
(1)请写出实验室使用浓盐酸、二氧化锰共热制氯气的离子方程式:___________ 。
(2)哪位同学的装置能够有效地防止副反应的发生?___________ 。
(3)请写出氯气和氢氧化钙制备漂白粉的化学方程式:___________ 。
(4)上述装置中,甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G两部分组成,从上述甲、乙、丙三套装置中选出合理的部分(按气流从左至右的流向)组装一套较完善的实验装置(填所选部分的字母)___________ 。
(5)实验中若用12mol·L-1的浓盐酸200mL与足量二氧化锰反应,最终生成的次氯酸钙的物质的量总小于0.3mol,其可能的主要原因是___________ (假定各步反应均无反应损耗且无副反应发生)。

(1)请写出实验室使用浓盐酸、二氧化锰共热制氯气的离子方程式:
(2)哪位同学的装置能够有效地防止副反应的发生?
(3)请写出氯气和氢氧化钙制备漂白粉的化学方程式:
(4)上述装置中,甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G两部分组成,从上述甲、乙、丙三套装置中选出合理的部分(按气流从左至右的流向)组装一套较完善的实验装置(填所选部分的字母)
(5)实验中若用12mol·L-1的浓盐酸200mL与足量二氧化锰反应,最终生成的次氯酸钙的物质的量总小于0.3mol,其可能的主要原因是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】下图为铜丝与浓硫酸反应并验证其产物性质的实验装置。
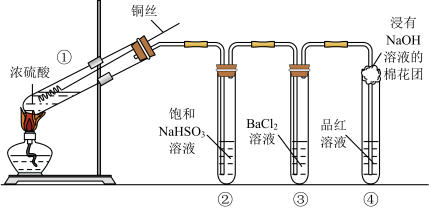
(1)①中反应的化学方程式是______ 。其中铜发生了______ (填“氧化”或“还原”)反应,判断依据为_____ 。
(2)②中饱和NaHSO3溶液的作用是除去①中挥发出的硫酸。加热一段时间后,③中溶液依然澄清,④中溶液褪色。想要立即终止铜与硫酸的反应,最恰当的方法是______ 。
a.上移铜丝,使其脱离硫酸
b.撤去酒精灯
c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
完成上述反应的离子方程式。
(4)④中棉花团的作用是_______ 。
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是______ 。

(1)①中反应的化学方程式是
(2)②中饱和NaHSO3溶液的作用是除去①中挥发出的硫酸。加热一段时间后,③中溶液依然澄清,④中溶液褪色。想要立即终止铜与硫酸的反应,最恰当的方法是
a.上移铜丝,使其脱离硫酸
b.撤去酒精灯
c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
| 加入试剂 | 现象 | 反应的离子方程式 | |
| 第一份 | 加入NaOH溶液 | 有白色沉淀生成 | |
| 第二份 | 加入氯水 | 有白色沉淀生成 |
(4)④中棉花团的作用是
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸亚铁可用于治疗缺铁性贫血症。某兴趣小组为探究硫酸亚铁的分解产物,设计实验方案如下:
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有 的硬质玻璃管;
的硬质玻璃管;
③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B、C装置中的实验现象可推测分解产物中含有___________ 和___________ 。
(2)将装置B、C顺序颠倒能否达到原来的实验目的___________ (填“能”或“不能”),原因是___________ 。
(3)D装置中发生的主要反应的离子方程式是___________ 。
(4)通过计算确定已分解的FeSO4物质的量(写出计算过程)___________ 。
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有
 的硬质玻璃管;
的硬质玻璃管;③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B、C装置中的实验现象可推测分解产物中含有
(2)将装置B、C顺序颠倒能否达到原来的实验目的
(3)D装置中发生的主要反应的离子方程式是
(4)通过计算确定已分解的FeSO4物质的量(写出计算过程)
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】资料显示,酸性介质中, 和
和 反应转化为
反应转化为 和
和 。小组探究利用该反应测定
。小组探究利用该反应测定 含量的条件。
含量的条件。
(1)实验Ⅱ中反应的离子方程式是___________ 。
(2)实验Ⅰ的条件下 能将
能将 氧化为
氧化为 ,推测实验Ⅰ未出现紫色的原因:
,推测实验Ⅰ未出现紫色的原因:________ 。
(3)经检验,棕黑色沉淀为 ,针对实验Ⅲ中的现象,提出以下假设:
,针对实验Ⅲ中的现象,提出以下假设:
假设1: 的浓度较低,不足以将
的浓度较低,不足以将 氧化为
氧化为
假设2:溶液中存在还原剂 ,将生成的
,将生成的 ,还原为
,还原为
①甲同学分析上述实验设计,认为假设1不成立,理由是___________ 。
②针对假设2,乙同学设计实验Ⅳ证实了推测合理。
请写出实验操作和现象:___________ 。
③实验Ⅲ中生成 的离子方程式是
的离子方程式是___________ ,从化学反应原理的角度分析实验Ⅲ未得到紫色溶液的原因:___________ 。
(4)资料表明 可作为
可作为 和
和 反应转化为
反应转化为 的催化剂。丙同学设计实验Ⅲ的对比实验进行了证实。向
的催化剂。丙同学设计实验Ⅲ的对比实验进行了证实。向___________ 中滴加2滴 溶液,再加入
溶液,再加入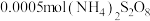 固体,加热至沸腾,观察到溶液变为紫色。
固体,加热至沸腾,观察到溶液变为紫色。
(5)根据上述实验,要利用 将
将 转化为
转化为 的反应来快速测定
的反应来快速测定 的含量,应控制的反应条件有;加热至沸腾、
的含量,应控制的反应条件有;加热至沸腾、___________ 。
 和
和 反应转化为
反应转化为 和
和 。小组探究利用该反应测定
。小组探究利用该反应测定 含量的条件。
含量的条件。| 实验 | 序号 | 物质a | 实验现象 |
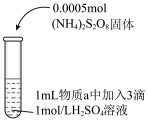 | Ⅰ |  溶液 溶液 | 无明显变化 |
| Ⅱ |  溶液 溶液 | 加热至沸腾, 后溶液变为紫色 后溶液变为紫色 | |
| Ⅲ |  溶液 溶液 | 加热至沸腾,生成大量棕黑色沉淀,静置,上层溶液未变紫色 |
(1)实验Ⅱ中反应的离子方程式是
(2)实验Ⅰ的条件下
 能将
能将 氧化为
氧化为 ,推测实验Ⅰ未出现紫色的原因:
,推测实验Ⅰ未出现紫色的原因:(3)经检验,棕黑色沉淀为
 ,针对实验Ⅲ中的现象,提出以下假设:
,针对实验Ⅲ中的现象,提出以下假设:假设1:
 的浓度较低,不足以将
的浓度较低,不足以将 氧化为
氧化为
假设2:溶液中存在还原剂
 ,将生成的
,将生成的 ,还原为
,还原为
①甲同学分析上述实验设计,认为假设1不成立,理由是
②针对假设2,乙同学设计实验Ⅳ证实了推测合理。
请写出实验操作和现象:
③实验Ⅲ中生成
 的离子方程式是
的离子方程式是(4)资料表明
 可作为
可作为 和
和 反应转化为
反应转化为 的催化剂。丙同学设计实验Ⅲ的对比实验进行了证实。向
的催化剂。丙同学设计实验Ⅲ的对比实验进行了证实。向 溶液,再加入
溶液,再加入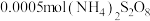 固体,加热至沸腾,观察到溶液变为紫色。
固体,加热至沸腾,观察到溶液变为紫色。(5)根据上述实验,要利用
 将
将 转化为
转化为 的反应来快速测定
的反应来快速测定 的含量,应控制的反应条件有;加热至沸腾、
的含量,应控制的反应条件有;加热至沸腾、
您最近半年使用:0次



