氯气(液氯)、漂白粉、“84”消毒液等都是含氯消毒剂。已知:在酸性条件下,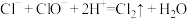 。
。
(1)工业上用电解饱和食盐水的方法制取氯气,实验室中可以用二氧化锰或高锰酸钾与浓盐酸反应制取氯气。
①写出二氧化锰与浓盐酸反应制取氯气的离子方程式:___________ ,该反应中氧化剂为,每生成7.1g气体反应中转移的电子的物质的量为___________ mol。
② 与浓盐酸的反应为
与浓盐酸的反应为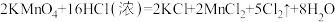 ,用
,用 和
和 分别与浓盐酸制备等量的氯气,消耗的
分别与浓盐酸制备等量的氯气,消耗的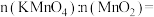
___________ 。
(2)由于氯气不便于保存,生活中常用的含氯消毒剂是漂白粉或“84”消毒液。
①常温下,将氯气通入NaOH溶液中,可以制得“84”消毒液,写出发生反应的离子方程式:___________ ,该消毒液的有效成分是___________ (填化学式)。生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是___________ 。
②将氯气通入石灰乳(主要成分是氢氧化钙)中可以制得漂白粉,漂白粉的主要成分为___________ (填化学式)。漂白粉长时间暴露在空气中会变质,请结合化学方程式解释其原因:___________ 。
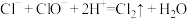 。
。(1)工业上用电解饱和食盐水的方法制取氯气,实验室中可以用二氧化锰或高锰酸钾与浓盐酸反应制取氯气。
①写出二氧化锰与浓盐酸反应制取氯气的离子方程式:
②
 与浓盐酸的反应为
与浓盐酸的反应为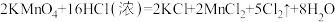 ,用
,用 和
和 分别与浓盐酸制备等量的氯气,消耗的
分别与浓盐酸制备等量的氯气,消耗的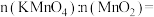
(2)由于氯气不便于保存,生活中常用的含氯消毒剂是漂白粉或“84”消毒液。
①常温下,将氯气通入NaOH溶液中,可以制得“84”消毒液,写出发生反应的离子方程式:
②将氯气通入石灰乳(主要成分是氢氧化钙)中可以制得漂白粉,漂白粉的主要成分为
更新时间:2021-12-01 16:25:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)写出制备氢氧化铁胶体的离子方程式:___________ 。
(2)自来水中的NO 对人类健康产生危害。为了降低自来水中NO
对人类健康产生危害。为了降低自来水中NO 的浓度,某研究人员提出在碱性条件下用Al粉还原NO
的浓度,某研究人员提出在碱性条件下用Al粉还原NO ,产物是N2。发生的反应可表示如下,请完成方程式的配平。
,产物是N2。发生的反应可表示如下,请完成方程式的配平。___________
___________Al+___________NO +___________OH-→___________AlO
+___________OH-→___________AlO +___________N2↑+___________H2O
+___________N2↑+___________H2O
(3)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。
①用双线桥表示反应的电子转移方向和数目:___________ 。
②反应中氧化剂与还原剂的物质的量之比为:___________ 。
(4)“84”消毒液的包装说明上有如下信息:含37.25%NaClO(次氯酸钠)、1000 mL、密度1.2g/cm3,请回答下列问题:
①上述“84”消毒液的物质的量浓度为___________ mol/L。
②该同学取100 mL上述“84”消毒液,稀释后用于消毒,稀释100倍后的溶液中c(Na+)=___________ mol/L,该消毒液长时间放置在空气中能吸收标准状况下CO2的体积为___________ L。(已知酸性顺序为H2CO3>HClO> HCO )
)
(1)写出制备氢氧化铁胶体的离子方程式:
(2)自来水中的NO
 对人类健康产生危害。为了降低自来水中NO
对人类健康产生危害。为了降低自来水中NO 的浓度,某研究人员提出在碱性条件下用Al粉还原NO
的浓度,某研究人员提出在碱性条件下用Al粉还原NO ,产物是N2。发生的反应可表示如下,请完成方程式的配平。
,产物是N2。发生的反应可表示如下,请完成方程式的配平。___________Al+___________NO
 +___________OH-→___________AlO
+___________OH-→___________AlO +___________N2↑+___________H2O
+___________N2↑+___________H2O(3)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。
①用双线桥表示反应的电子转移方向和数目:
②反应中氧化剂与还原剂的物质的量之比为:
(4)“84”消毒液的包装说明上有如下信息:含37.25%NaClO(次氯酸钠)、1000 mL、密度1.2g/cm3,请回答下列问题:
①上述“84”消毒液的物质的量浓度为
②该同学取100 mL上述“84”消毒液,稀释后用于消毒,稀释100倍后的溶液中c(Na+)=
 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。已知:工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。
完成下列填空:
(1)将二氧化氯通入品红试液中,溶液褪色的理由是___ 。
(2)请配平下列反应的化学方程式(CH3OH中H为+1价,O为-2价):___ __CH3OH+__NaClO3+__→__CO2↑+__C1O2↑+__Na2SO4+ _
(3)该反应中,被氧化的元素是___ 。还原产物与氧化产物的物质的量之比是___ 。
(4)根据上述反应可推知___ 。
a.氧化性:C1O2>NaClO3 b.氧化性:NaClO3>CH3OH
c.还原性:CH3OH>ClO2 d.还原性:CH3OH>Na2SO4
(5)若转移的电子数目为0.3NA(NA为阿伏加 德罗常数),则反应产生气体(标准状况)为__ L。
(6)消毒效率常以单位质量的消毒剂得到的电子数表示。ClO2的消毒效率是Cl2的__ 倍。
完成下列填空:
(1)将二氧化氯通入品红试液中,溶液褪色的理由是
(2)请配平下列反应的化学方程式(CH3OH中H为+1价,O为-2价):
(3)该反应中,被氧化的元素是
(4)根据上述反应可推知
a.氧化性:C1O2>NaClO3 b.氧化性:NaClO3>CH3OH
c.还原性:CH3OH>ClO2 d.还原性:CH3OH>Na2SO4
(5)若转移的电子数目为0.3NA(NA为阿伏加 德罗常数),则反应产生气体(标准状况)为
(6)消毒效率常以单位质量的消毒剂得到的电子数表示。ClO2的消毒效率是Cl2的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图是一些常见含氯产品,根据情况回答下列问题。

(1)下列有关氯单质和氯水的说法正确的是___________ (填序号)。
①液氯是纯净物,氯水是混合物
②氯气可使湿润的红色布条褪色,所以氯气具有漂白性
③过量的铁在少量的氯气中燃烧生成FeCl2
④新制氯水可使蓝色石蕊试纸先变红后褪色
⑤新制氯水放置数天后酸性将减弱
(2)漂白粉常用于对环境和饮用水进行杀菌,消毒,以抑制大规模传染病爆发。写出漂白粉在空气中杀菌消毒的原理___________ (用化学方程式表示)
(3)据报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分为稀盐酸)与“84”消毒液(有效成分NaClO),而发生氯气中毒事件,请从氧化还原的角度分析原因(用离子方程式表示)___________ 。
(4)某“84”消毒液部分标签如图所示,回答下列问题:
①计算该“84”消毒液的物质的量浓度___________ mol·L-1(保留小数点后一位)。
②某实验需用250ml上述消毒液,现用NaClO固体配制。在配制过程中,除需要烧杯、托盘天平外还必需的仪器有___________ (写三种),下列操作可能使配制溶液浓度偏低的是___________
A.移液时,未洗涤烧杯内壁和玻璃棒 B.溶解后未经冷却就移液 C.移液时,有少量液体溅出 D.定容时,俯视刻度线 E.容量瓶用蒸馏水洗净后,没烘干就直接使用 F.定容时,仰视刻度线

(1)下列有关氯单质和氯水的说法正确的是
①液氯是纯净物,氯水是混合物
②氯气可使湿润的红色布条褪色,所以氯气具有漂白性
③过量的铁在少量的氯气中燃烧生成FeCl2
④新制氯水可使蓝色石蕊试纸先变红后褪色
⑤新制氯水放置数天后酸性将减弱
(2)漂白粉常用于对环境和饮用水进行杀菌,消毒,以抑制大规模传染病爆发。写出漂白粉在空气中杀菌消毒的原理
(3)据报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分为稀盐酸)与“84”消毒液(有效成分NaClO),而发生氯气中毒事件,请从氧化还原的角度分析原因(用离子方程式表示)
(4)某“84”消毒液部分标签如图所示,回答下列问题:
| 净含量:500mL密度:1.19g·cm-3 主要成分:25% NaClO 注意事项:密封保存,易吸收空气中CO2变质 |
②某实验需用250ml上述消毒液,现用NaClO固体配制。在配制过程中,除需要烧杯、托盘天平外还必需的仪器有
A.移液时,未洗涤烧杯内壁和玻璃棒 B.溶解后未经冷却就移液 C.移液时,有少量液体溅出 D.定容时,俯视刻度线 E.容量瓶用蒸馏水洗净后,没烘干就直接使用 F.定容时,仰视刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素的“价—类二维图”是我们学习元素及其化合物相关知识的重要模型工具,也是发展“证据推理与模型认知”这一科学核心素养的重要途径。如图为氯元素的“价—类二维图”,回答下列问题:

(1)Y的化学式为___________ 。
(2)某同学利用以下试剂研究HClO4性质,进行了如下预测:从物质类别上看,HClO4像盐酸一样属于强酸,可能与HClO4反应的有(填序号)___________。
(3)NaClO是“84”消毒液的有效成分,在用“84”消毒液的稀溶液浸泡餐具过程中,因吸收空气中 ,使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:
,使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:___________ 。
(4)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①下列有关氯气的叙述不正确的是___________ (填序号)。
A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟
B.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸
C.纯净的 在
在 中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照
中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照 和
和 的混合气体时,因迅速化合而爆炸
的混合气体时,因迅速化合而爆炸
D.通常状况下氯气能和Fe反应,氯气的储存不能用铁质容器
②工业上利用氯气和石灰乳反应可制得漂白粉,漂白粉有效成分的化学式为___________ 。

(1)Y的化学式为
(2)某同学利用以下试剂研究HClO4性质,进行了如下预测:从物质类别上看,HClO4像盐酸一样属于强酸,可能与HClO4反应的有(填序号)___________。
A. | B.Fe | C.BaSO4 | D.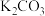 |
(3)NaClO是“84”消毒液的有效成分,在用“84”消毒液的稀溶液浸泡餐具过程中,因吸收空气中
 ,使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:
,使消毒杀菌能力增强,产物中有小苏打,请用离子方程式说明原因:(4)氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①下列有关氯气的叙述不正确的是
A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟
B.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸
C.纯净的
 在
在 中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照
中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照 和
和 的混合气体时,因迅速化合而爆炸
的混合气体时,因迅速化合而爆炸D.通常状况下氯气能和Fe反应,氯气的储存不能用铁质容器
②工业上利用氯气和石灰乳反应可制得漂白粉,漂白粉有效成分的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯气是一种重要的化工原料.
(1)氯气是一种黄绿色气体,化学性质上和氧气有许多相似之处,比如:氯气也能支持燃烧,写出铁丝在氯气中燃烧的方程式:______ ;氢气在氯气的燃烧观察的现象为: ______
(2)氯气和石灰乳反应可以制得漂白粉,漂白粉暴露在空气中因吸收了空气中的 和
和 而失效,漂白粉失效过程的化学反应方程式为:
而失效,漂白粉失效过程的化学反应方程式为: ______
(3)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空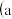 、b、c、d中重合部分代表物质间反应,且氯水足量
、b、c、d中重合部分代表物质间反应,且氯水足量 .
.

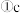 过程的反应方程式
过程的反应方程式 ______ , e过程中的化学方程式为 ______ .
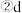 过程所观察到的现象为:
过程所观察到的现象为: ______
b过程证明了氯水的存在______ 微粒

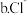
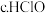
 .
.
(1)氯气是一种黄绿色气体,化学性质上和氧气有许多相似之处,比如:氯气也能支持燃烧,写出铁丝在氯气中燃烧的方程式:
(2)氯气和石灰乳反应可以制得漂白粉,漂白粉暴露在空气中因吸收了空气中的
 和
和 而失效,漂白粉失效过程的化学反应方程式为:
而失效,漂白粉失效过程的化学反应方程式为: (3)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空
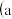 、b、c、d中重合部分代表物质间反应,且氯水足量
、b、c、d中重合部分代表物质间反应,且氯水足量 .
.
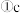 过程的反应方程式
过程的反应方程式 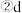 过程所观察到的现象为:
过程所观察到的现象为: b过程证明了氯水的存在

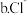
 .
.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求书写
(1)请写出2-甲基丁烷的结构简式___________ 葡萄糖分子式______________
(2)实验室制取氯气的离子反应方程式_______________
(3)呼吸面具中,过氧化钠与二氧化碳起反应的化学方程式______________
(1)请写出2-甲基丁烷的结构简式
(2)实验室制取氯气的离子反应方程式
(3)呼吸面具中,过氧化钠与二氧化碳起反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】X常温下是一种无色液体,极易水解,遇潮湿空气会产生白雾。实验室制备X可用A、C两种气体发生化合反应制得,物质转化过程如下:

为探究X的组成,取1.35 g X与足量水完全反应,在生成物中加入1.0 mol·L-1的NaOH溶液40.0 mL恰好显中性。继续加入过量BaCl2溶液,产生沉淀2.33 g。
请回答:
(1)由Na2SO3和B反应生成C的离子方程式:__________ 。
(2)X的分子式是________ 。在生成X的反应中,C表现了________ 性。

为探究X的组成,取1.35 g X与足量水完全反应,在生成物中加入1.0 mol·L-1的NaOH溶液40.0 mL恰好显中性。继续加入过量BaCl2溶液,产生沉淀2.33 g。
请回答:
(1)由Na2SO3和B反应生成C的离子方程式:
(2)X的分子式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】中国对新冠疫情的防控在世界上得到广泛的认同,其中消毒是重要的措施。84消毒液(有效成分NaClO)是一种高效、安全的杀菌消毒剂。可由氯气与NaOH溶液制得,回答下列问题。
(1)实验室配制0.5 mo/L的NaOH溶液,溶液转移时未对容量瓶干燥,其结果___________ 。(填“偏大”、“偏小”、或“不变”)
(2)实验室用下图所示装置制备、收集氯气。

完成下列填空:
①盛有MnO2的仪器名称是___________ 。
②写出装置A中发生反应的化学方程式为___________ 。
③若装置A、B之间增加一个盛有浓硫酸的洗气瓶,B中___________ (填“能”或“不能”)得到纯净的Cl2。
(3)高铁酸钾( )是一种高效低污染的水处理剂,其制备原理是将A中产生的
)是一种高效低污染的水处理剂,其制备原理是将A中产生的 通入D装置,产物有K2FeO4、KCl和H2O。若D装置中的反应共转移3mol电子,理论上生成的K2FeO4的质量为
通入D装置,产物有K2FeO4、KCl和H2O。若D装置中的反应共转移3mol电子,理论上生成的K2FeO4的质量为___________ 克。
(1)实验室配制0.5 mo/L的NaOH溶液,溶液转移时未对容量瓶干燥,其结果
(2)实验室用下图所示装置制备、收集氯气。

完成下列填空:
①盛有MnO2的仪器名称是
②写出装置A中发生反应的化学方程式为
③若装置A、B之间增加一个盛有浓硫酸的洗气瓶,B中
(3)高铁酸钾(
 )是一种高效低污染的水处理剂,其制备原理是将A中产生的
)是一种高效低污染的水处理剂,其制备原理是将A中产生的 通入D装置,产物有K2FeO4、KCl和H2O。若D装置中的反应共转移3mol电子,理论上生成的K2FeO4的质量为
通入D装置,产物有K2FeO4、KCl和H2O。若D装置中的反应共转移3mol电子,理论上生成的K2FeO4的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】新型冠状病毒蔓延期间,为做好自我保护,我们要减少外出,避免与表现出有呼吸道疾病症状的人密切接触,外出最重要的防护措施是佩戴符合要求的口罩。在生活中常见的口罩一般有棉布口罩、医用外科口罩、活性炭口罩和N95口罩。也可以在实验室进行制备84消毒液(有效成分是NaClO)。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的_______ (“溶液”、“胶体”、“悬浊液”)。
(2)佩戴口罩预防疾病的原理相当于化学实验中的_______ 操作。(“蒸发”、“过滤”“萃取”)
(3)生成N95口罩的主要原料是聚丙烯,它属于_________ (填“金属材料”或“合成材料”)
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:________ 。

(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为____ 。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的
(2)佩戴口罩预防疾病的原理相当于化学实验中的
(3)生成N95口罩的主要原料是聚丙烯,它属于
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:

(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)实验室需要用NaOH配制0.2mol/LNaOH溶液450mL。
①完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、胶头滴管、____ 。
②配制该溶液需称取NaOH____ g。
③称量完毕,将药品倒入烧杯中,溶解、冷却,转移、洗涤。
(2)取上述配制的NaOH溶液200mL制取消毒液:向该NaOH溶液通入Cl2,使得NaOH恰好完全反应。完成下列填空。
①该消毒液制备的化学方程式为____ ,该反应消耗的Cl2在标准状况下的体积为____ 。
②该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。若将二者混合,每产生1molCl2,转移电子个数约为____ 。
(1)实验室需要用NaOH配制0.2mol/LNaOH溶液450mL。
①完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、胶头滴管、
②配制该溶液需称取NaOH
③称量完毕,将药品倒入烧杯中,溶解、冷却,转移、洗涤。
(2)取上述配制的NaOH溶液200mL制取消毒液:向该NaOH溶液通入Cl2,使得NaOH恰好完全反应。完成下列填空。
①该消毒液制备的化学方程式为
②该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。若将二者混合,每产生1molCl2,转移电子个数约为
您最近一年使用:0次



