回答下列问题:
(1)实验室需要用NaOH配制0.2mol/LNaOH溶液450mL。
①完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、胶头滴管、____ 。
②配制该溶液需称取NaOH____ g。
③称量完毕,将药品倒入烧杯中,溶解、冷却,转移、洗涤。
(2)取上述配制的NaOH溶液200mL制取消毒液:向该NaOH溶液通入Cl2,使得NaOH恰好完全反应。完成下列填空。
①该消毒液制备的化学方程式为____ ,该反应消耗的Cl2在标准状况下的体积为____ 。
②该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。若将二者混合,每产生1molCl2,转移电子个数约为____ 。
(1)实验室需要用NaOH配制0.2mol/LNaOH溶液450mL。
①完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、胶头滴管、
②配制该溶液需称取NaOH
③称量完毕,将药品倒入烧杯中,溶解、冷却,转移、洗涤。
(2)取上述配制的NaOH溶液200mL制取消毒液:向该NaOH溶液通入Cl2,使得NaOH恰好完全反应。完成下列填空。
①该消毒液制备的化学方程式为
②该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。若将二者混合,每产生1molCl2,转移电子个数约为
更新时间:2022-09-29 09:06:13
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:
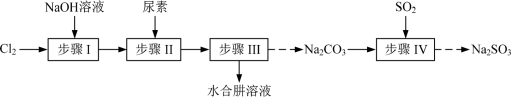
已知:①Cl2+2OH−=ClO−+Cl−+H2O是放热反应。
②N2H4·H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
步骤I制备NaClO溶液时,若温度超过40℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为_______ ;实验中控制温度除用冰水浴外,还需采取的措施是_______ 。

已知:①Cl2+2OH−=ClO−+Cl−+H2O是放热反应。
②N2H4·H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
步骤I制备NaClO溶液时,若温度超过40℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】小康同学用一定量的Na2O2与水反应,制取中学一种常见气体。
(1)相关反应的化学方程式是__________________________________ ,检验反应生成气体的方法是________________________________________________ 。
(2)利用本实验所得到的溶液(经检测为400 mL 1.0 mol/ L的碱溶液),小康又进行了两个自己感兴趣的实验。
①取100 mL 该溶液用于氯气的尾气吸收,则最多可吸收标准状况下的氯气多少升?(请写出相关反应的方程式或关系式,并列式计算,下同)
②取100 mL 该溶液恰好能与10 g某镁铝合金恰好完全反应,请计算该合金中铝的质量分数。
(1)相关反应的化学方程式是
(2)利用本实验所得到的溶液(经检测为400 mL 1.0 mol/ L的碱溶液),小康又进行了两个自己感兴趣的实验。
①取100 mL 该溶液用于氯气的尾气吸收,则最多可吸收标准状况下的氯气多少升?(请写出相关反应的方程式或关系式,并列式计算,下同)
②取100 mL 该溶液恰好能与10 g某镁铝合金恰好完全反应,请计算该合金中铝的质量分数。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯气极其相关产品在生产生活中应用广泛。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是__________ 。(用化学方程式表示)。
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是_________ (填字母)。
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。
①分析“对金属制品有腐蚀作用”的原因:_______________ 。
②需“密闭保存”的原因:______________ 。
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式_____________ 。
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是_______ 。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。

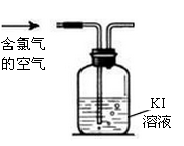
①分析“对金属制品有腐蚀作用”的原因:
②需“密闭保存”的原因:
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】实验室用固体烧碱配制500mL0.1000mol/L的NaOH溶液。
(1)需称量_______ g烧碱,应放在_______ (填仪器名称)中称量。
(2)配制过程中,不需要 的仪器(填写代号)_______ 。

a、烧杯 b、量筒 c、玻璃棒 d、1000mL容量瓶 e、漏斗 f、胶头滴管
(3)根据实验需要和(2)所列仪器判断,完成实验还缺少 的仪器有_______ 。
(4)将上述实验步骤A到F按实验过程先后次序排列_______ 。
(5)在容量瓶中确定溶液体积的过程中,最后加入少量水的操作(写过程)_______ 。
(1)需称量
(2)配制过程中,

a、烧杯 b、量筒 c、玻璃棒 d、1000mL容量瓶 e、漏斗 f、胶头滴管
(3)根据实验需要和(2)所列仪器判断,完成实验还
(4)将上述实验步骤A到F按实验过程先后次序排列
(5)在容量瓶中确定溶液体积的过程中,最后加入少量水的操作(写过程)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】实验室需要用烧碱固体配制1mol/L的NaOH溶液500mL。回答下列问题:
(1)如图所示的仪器中,配制溶液肯定不需要的是___________ (填序号)。

(2)下列操作中,题中所给容量瓶所不具备的功能有___________(填序号)。
(3)计算结果:需要称取NaOH固体___________ g;
(4)实验配置溶液操作过程中溶解、转移步骤均用到玻璃棒,其作用分别是:__________ 、___________ ;
(5)若出现如下情况,其中将引起所配溶液浓度偏低的是_______ ;(填下列编号)
①容量瓶实验前用水洗干净,但未烘干②定容观察液面时俯视
③配制过程中没有洗涤烧杯和玻璃棒④加蒸馏水时不慎超过刻度线
(1)如图所示的仪器中,配制溶液肯定不需要的是

(2)下列操作中,题中所给容量瓶所不具备的功能有___________(填序号)。
| A.配制一定体积准确浓度的标准溶液 | B.贮存溶液 |
| C.可以配制480ml的溶液 | D.用来加热溶解固体溶质 |
(4)实验配置溶液操作过程中溶解、转移步骤均用到玻璃棒,其作用分别是:
(5)若出现如下情况,其中将引起所配溶液浓度偏低的是
①容量瓶实验前用水洗干净,但未烘干②定容观察液面时俯视
③配制过程中没有洗涤烧杯和玻璃棒④加蒸馏水时不慎超过刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】物质的量浓度是一种常用的溶液浓度表示方法,利用其进行定量分析计算比较方便。
I.实验需要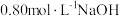 溶液475mL和
溶液475mL和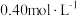 硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:
硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:
(1)下列操作中,能用容量瓶实现的有_____ (填序号)。
A.配制一定体积准确浓度的标准溶液
B.量取一定体积的液体
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.贮存溶液
F.用来加热溶解固体溶质
(2)根据计算用托盘天平称取所需的NaOH的质量。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度_____ (填“大于”“等于”或“小于”,下同)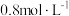 。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度
。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度_____ 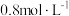 。
。
(3)若用质量分数为98%、密度为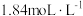 的浓硫酸来配制,需用量筒量取体积为
的浓硫酸来配制,需用量筒量取体积为_____ mL的浓硫酸来稀释。稀释浓硫酸的操作是_____ 。
II.在0.2L由NaCl、 、CaCl2组成的混合液中,部分离子浓度大小如图所示。请回答下列问题:
、CaCl2组成的混合液中,部分离子浓度大小如图所示。请回答下列问题:

(4)该混合液中 的物质的量为
的物质的量为_____ mol,将该混合液加水稀释至体积为1L,稀释后溶液中 的物质的量浓度为
的物质的量浓度为_____  。
。
I.实验需要
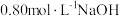 溶液475mL和
溶液475mL和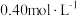 硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:
硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:(1)下列操作中,能用容量瓶实现的有
A.配制一定体积准确浓度的标准溶液
B.量取一定体积的液体
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.贮存溶液
F.用来加热溶解固体溶质
(2)根据计算用托盘天平称取所需的NaOH的质量。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度
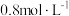 。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度
。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度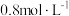 。
。(3)若用质量分数为98%、密度为
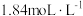 的浓硫酸来配制,需用量筒量取体积为
的浓硫酸来配制,需用量筒量取体积为II.在0.2L由NaCl、
 、CaCl2组成的混合液中,部分离子浓度大小如图所示。请回答下列问题:
、CaCl2组成的混合液中,部分离子浓度大小如图所示。请回答下列问题:
(4)该混合液中
 的物质的量为
的物质的量为 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次



