家用液化气的成分之一是丁烷。当10kg丁烷完全燃烧生成二氧化碳和液态水时,放出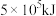 的热量。
的热量。
(1)写出1mol丁烷完全燃烧时热化学方程式___________ 。
(2)已知1mol液态水变为水蒸气时需要吸收44kJ的热量,计算1mol丁烷完全燃烧生成二氧化碳和水蒸气时放出的热量___________ 。
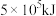 的热量。
的热量。(1)写出1mol丁烷完全燃烧时热化学方程式
(2)已知1mol液态水变为水蒸气时需要吸收44kJ的热量,计算1mol丁烷完全燃烧生成二氧化碳和水蒸气时放出的热量
更新时间:2021-12-01 23:29:05
|
相似题推荐
【推荐1】为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2,已知:2CO(g)+O2(g)==2CO2(g) △H=-566KJ/mol
2H2(g)+O2(g)==2H2O(g) △H=-483.6KJ/mol H2O(g)="=" H2O(l) △H=-44.0KJ/mol
(1)1mol氢气燃烧生成液态水时放出的热为____________
(2)写出CO和 H2O(g)作用生成CO2和H2的热化学方程式_________________________ 。
(3)往1L体积不变的容器中加入0.200molCO和1.00molH2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO的转化率为___________ ;反应达到平衡后,升高温度,此时平衡常数将___________ (填“变大”、“变小”或“不变”),平衡将向__________ (填“正”或“逆”)反应方向移动。
(4)H2是一种理想的绿色能源,可作燃料电池;若该氢氧燃料电池以KOH为电解质溶液,其负极的电极反应式是_______________________________________________ 。
2H2(g)+O2(g)==2H2O(g) △H=-483.6KJ/mol H2O(g)="=" H2O(l) △H=-44.0KJ/mol
(1)1mol氢气燃烧生成液态水时放出的热为
(2)写出CO和 H2O(g)作用生成CO2和H2的热化学方程式
(3)往1L体积不变的容器中加入0.200molCO和1.00molH2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO的转化率为
(4)H2是一种理想的绿色能源,可作燃料电池;若该氢氧燃料电池以KOH为电解质溶液,其负极的电极反应式是
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】盖斯定律的理解
(1)在一定条件下,化学反应的反应焓变只与反应体系的_______ 有关,而与反应的途径无关。
(2)某反应始态和终态相同,反应的途径有如下(Ⅰ)、(Ⅱ)、(Ⅲ)三种。
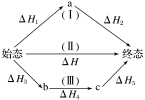
则ΔH=_______ =_______ 。
(1)在一定条件下,化学反应的反应焓变只与反应体系的
(2)某反应始态和终态相同,反应的途径有如下(Ⅰ)、(Ⅱ)、(Ⅲ)三种。

则ΔH=
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】①CaCO3(s)=CaO+CO2(g) ΔH=177.7kJ;
②C(g)+H2O(g)=CO(g)+H2(g) ΔH=-131.3kJ/mol;
③0.5H2SO4(l)+NaOH(l)=0.5Na2SO4(l)+H2O(l) ΔH=-57.3kJ/mol;
④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol;
⑤ CO(g)+ O2(g)=CO2(g) ΔH=-283kJ/mol;
O2(g)=CO2(g) ΔH=-283kJ/mol;
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3kJ/mol;
⑦2H2(g)+O2(g)=H2O(l);ΔH=-517.6kJ/mol;
(1)已知上述热化学方程式所给出的焓变绝对值没有错误,试从状态、反应放热或吸热等方面判断:在①—⑦中,不正确的有_________________ ,不正确的理由分别是:____________________________________________________________ 。
(2)根据上述信息,写出C转化为CO的热化学方程式:
______________________________________________________________ 。
(3)上述反应中,表示燃烧热的热化学方程式有_____ ,表示中和热的热化学方程式有_____ 。
(4)已知1mol气态H2与 mol气态O2反应生成1mol水蒸气,放出241.8kJ的热量;1mol气态H2与
mol气态O2反应生成1mol水蒸气,放出241.8kJ的热量;1mol气态H2与 mol气态O2反应生成1mol液态水,放出285.8kJ的热量。写出上述两个热化学方程式
mol气态O2反应生成1mol液态水,放出285.8kJ的热量。写出上述两个热化学方程式______________________________________________________________ 。
②C(g)+H2O(g)=CO(g)+H2(g) ΔH=-131.3kJ/mol;
③0.5H2SO4(l)+NaOH(l)=0.5Na2SO4(l)+H2O(l) ΔH=-57.3kJ/mol;
④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol;
⑤ CO(g)+
 O2(g)=CO2(g) ΔH=-283kJ/mol;
O2(g)=CO2(g) ΔH=-283kJ/mol;⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3kJ/mol;
⑦2H2(g)+O2(g)=H2O(l);ΔH=-517.6kJ/mol;
(1)已知上述热化学方程式所给出的焓变绝对值没有错误,试从状态、反应放热或吸热等方面判断:在①—⑦中,不正确的有
(2)根据上述信息,写出C转化为CO的热化学方程式:
(3)上述反应中,表示燃烧热的热化学方程式有
(4)已知1mol气态H2与
 mol气态O2反应生成1mol水蒸气,放出241.8kJ的热量;1mol气态H2与
mol气态O2反应生成1mol水蒸气,放出241.8kJ的热量;1mol气态H2与 mol气态O2反应生成1mol液态水,放出285.8kJ的热量。写出上述两个热化学方程式
mol气态O2反应生成1mol液态水,放出285.8kJ的热量。写出上述两个热化学方程式
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】根据盖斯定律计算
将两个或两个以上的热化学方程式包括其ΔH_____ ,得到一个新的热化学方程式及其ΔH。
将两个或两个以上的热化学方程式包括其ΔH
您最近一年使用:0次
【推荐3】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如图。
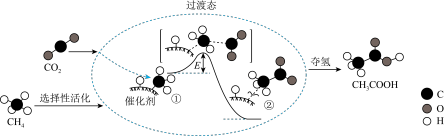
(1)①、②与过渡态三种物质中,最不稳定的是_______ ;①转化为②过程中_______ (选填“吸收”或“放出”)能量。
(2)25℃、101kPa下,CH4(g)、CH3COOH(l)的燃烧热分别-893kJ·mol-1、-870 kJ·mol-1,计算转化反应CO2(g) + CH4(g) = CH3COOH(l)的焓变ΔH=_______ kJ·mol-1

(1)①、②与过渡态三种物质中,最不稳定的是
(2)25℃、101kPa下,CH4(g)、CH3COOH(l)的燃烧热分别-893kJ·mol-1、-870 kJ·mol-1,计算转化反应CO2(g) + CH4(g) = CH3COOH(l)的焓变ΔH=
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】①CaCO3(s)=CaO+CO2(g) ΔH=177.7kJ;
②C(g)+H2O(g)=CO(g)+H2(g) ΔH=-131.3kJ/mol;
③0.5H2SO4(l)+NaOH(l)=0.5Na2SO4(l)+H2O(l) ΔH=-57.3kJ/mol;
④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol;
⑤ CO(g)+ O2(g)=CO2(g) ΔH=-283kJ/mol;
O2(g)=CO2(g) ΔH=-283kJ/mol;
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3kJ/mol;
⑦2H2(g)+O2(g)=H2O(l);ΔH=-517.6kJ/mol;
(1)已知上述热化学方程式所给出的焓变绝对值没有错误,试从状态、反应放热或吸热等方面判断:在①—⑦中,不正确的有_________________ ,不正确的理由分别是:____________________________________________________________ 。
(2)根据上述信息,写出C转化为CO的热化学方程式:
______________________________________________________________ 。
(3)上述反应中,表示燃烧热的热化学方程式有_____ ,表示中和热的热化学方程式有_____ 。
(4)已知1mol气态H2与 mol气态O2反应生成1mol水蒸气,放出241.8kJ的热量;1mol气态H2与
mol气态O2反应生成1mol水蒸气,放出241.8kJ的热量;1mol气态H2与 mol气态O2反应生成1mol液态水,放出285.8kJ的热量。写出上述两个热化学方程式
mol气态O2反应生成1mol液态水,放出285.8kJ的热量。写出上述两个热化学方程式______________________________________________________________ 。
②C(g)+H2O(g)=CO(g)+H2(g) ΔH=-131.3kJ/mol;
③0.5H2SO4(l)+NaOH(l)=0.5Na2SO4(l)+H2O(l) ΔH=-57.3kJ/mol;
④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol;
⑤ CO(g)+
 O2(g)=CO2(g) ΔH=-283kJ/mol;
O2(g)=CO2(g) ΔH=-283kJ/mol;⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3kJ/mol;
⑦2H2(g)+O2(g)=H2O(l);ΔH=-517.6kJ/mol;
(1)已知上述热化学方程式所给出的焓变绝对值没有错误,试从状态、反应放热或吸热等方面判断:在①—⑦中,不正确的有
(2)根据上述信息,写出C转化为CO的热化学方程式:
(3)上述反应中,表示燃烧热的热化学方程式有
(4)已知1mol气态H2与
 mol气态O2反应生成1mol水蒸气,放出241.8kJ的热量;1mol气态H2与
mol气态O2反应生成1mol水蒸气,放出241.8kJ的热量;1mol气态H2与 mol气态O2反应生成1mol液态水,放出285.8kJ的热量。写出上述两个热化学方程式
mol气态O2反应生成1mol液态水,放出285.8kJ的热量。写出上述两个热化学方程式
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ/mol
②C(s)+H2O(l)=CO(g)+H2(g) ΔH=-131.3 kJ/mol
③ H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)= Na2SO4(l)+H2O(l) ΔH=-57.3 kJ/mol
Na2SO4(l)+H2O(l) ΔH=-57.3 kJ/mol
④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
⑤CO(g)+ O2(g)=CO2(g) ΔH=-283 kJ/mol
O2(g)=CO2(g) ΔH=-283 kJ/mol
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ/mol
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-517.6 kJ/mol
(1)上述热化学方程式中,不正确的有________ 。
(2)根据上述信息,写出C转化为CO的热化学方程式________________ 。
②C(s)+H2O(l)=CO(g)+H2(g) ΔH=-131.3 kJ/mol
③
 H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)= Na2SO4(l)+H2O(l) ΔH=-57.3 kJ/mol
Na2SO4(l)+H2O(l) ΔH=-57.3 kJ/mol④C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
⑤CO(g)+
 O2(g)=CO2(g) ΔH=-283 kJ/mol
O2(g)=CO2(g) ΔH=-283 kJ/mol⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ/mol
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-517.6 kJ/mol
(1)上述热化学方程式中,不正确的有
(2)根据上述信息,写出C转化为CO的热化学方程式
您最近一年使用:0次



