盖斯定律的理解
(1)在一定条件下,化学反应的反应焓变只与反应体系的_______ 有关,而与反应的途径无关。
(2)某反应始态和终态相同,反应的途径有如下(Ⅰ)、(Ⅱ)、(Ⅲ)三种。
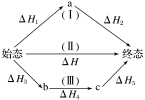
则ΔH=_______ =_______ 。
(1)在一定条件下,化学反应的反应焓变只与反应体系的
(2)某反应始态和终态相同,反应的途径有如下(Ⅰ)、(Ⅱ)、(Ⅲ)三种。

则ΔH=
22-23高二上·全国·课时练习 查看更多[1]
(已下线)化学反应的热效应——整体认知
更新时间:2022-08-16 11:41:24
|
相似题推荐
填空题
|
容易
(0.94)
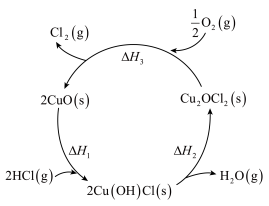
【推荐1】如图表示在CuO存在下HCl催化氧化的反应过程,则总反应的热化学方程为___________ 。

您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】根据盖斯定律计算
将两个或两个以上的热化学方程式包括其ΔH_____ ,得到一个新的热化学方程式及其ΔH。
将两个或两个以上的热化学方程式包括其ΔH
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】已知下列反应的反应热为:
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=−870.3 kJ∙mol−1
(2)C(s)+O2(g)=CO2(g) ΔH=−393.5 kJ∙mol−1
(3)H2(g)+ O2(g)=H2O(l) ΔH=−285.8 kJ∙mol−1试计算下列反应的反应热:
O2(g)=H2O(l) ΔH=−285.8 kJ∙mol−1试计算下列反应的反应热:
2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=_______ 。
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=−870.3 kJ∙mol−1
(2)C(s)+O2(g)=CO2(g) ΔH=−393.5 kJ∙mol−1
(3)H2(g)+
 O2(g)=H2O(l) ΔH=−285.8 kJ∙mol−1试计算下列反应的反应热:
O2(g)=H2O(l) ΔH=−285.8 kJ∙mol−1试计算下列反应的反应热:2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)=SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol−1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3(g) ΔH2=−30 kJ·mol−1
则反应4SiHCl3(g)=SiH4(g)+3SiCl4(g)的ΔH=__________ kJ·mol−1。
2SiHCl3(g)=SiH2Cl2(g)+ SiCl4(g) ΔH1=48 kJ·mol−1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3(g) ΔH2=−30 kJ·mol−1
则反应4SiHCl3(g)=SiH4(g)+3SiCl4(g)的ΔH=
您最近一年使用:0次

 2CO(g) ΔH1 K1
2CO(g) ΔH1 K1

