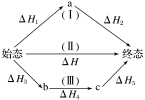
如图表示在CuO存在下HCl催化氧化的反应过程,则总反应的热化学方程为___________ 。

2023高三·全国·专题练习 查看更多[2]
更新时间:2023-02-01 21:36:33
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用做燃料。
已知:CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ΔH1 = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ΔH2 = -566.0 kJ·mol-1
(1)试写出CH3OH(1)在氧气中完全燃烧生成CO2和H2O(g)的热化学方程式:______
(2)甲醇作为燃料,优点是燃烧时排放的污染物少,从而不仅能缓解能源紧张和温室效应的问题,还能改善大气质量。试利用(1)中的热化学方程式计算,完全燃烧16g甲醇,生成二氧化碳和水蒸气时,放出的热量为___ kJ ,生成的CO2气体标准状况下体积是_____ L,转移电子____ mol
已知:CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ΔH1 = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ΔH2 = -566.0 kJ·mol-1
(1)试写出CH3OH(1)在氧气中完全燃烧生成CO2和H2O(g)的热化学方程式:
(2)甲醇作为燃料,优点是燃烧时排放的污染物少,从而不仅能缓解能源紧张和温室效应的问题,还能改善大气质量。试利用(1)中的热化学方程式计算,完全燃烧16g甲醇,生成二氧化碳和水蒸气时,放出的热量为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】由金红石(TiO2)制取单质Ti,涉及到的步骤为:
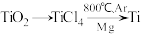
已知:①
②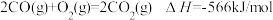
③
则:
(1)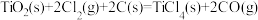 的
的 =
=________________ 。
(2)碳在氧气中不完全燃烧生成CO的热化学方程式为__________________________ 。
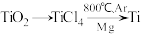
已知:①
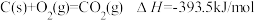
②
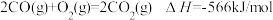
③

则:
(1)
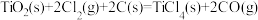 的
的 =
=(2)碳在氧气中不完全燃烧生成CO的热化学方程式为
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】根据盖斯定律计算
将两个或两个以上的热化学方程式包括其ΔH_____ ,得到一个新的热化学方程式及其ΔH。
将两个或两个以上的热化学方程式包括其ΔH
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
(1)已知: (g)=
(g)= (g)+H2(g) ΔH1=100.3kJ·mol−1 ①
(g)+H2(g) ΔH1=100.3kJ·mol−1 ①
H2(g)+I2(g)=2HI(g) ΔH2=﹣11.0kJ·mol−1 ②
对于反应: (g)+I2(g)=
(g)+I2(g)= (g)+2HI(g) ③ ΔH3=
(g)+2HI(g) ③ ΔH3=_______ kJ·mol−1。
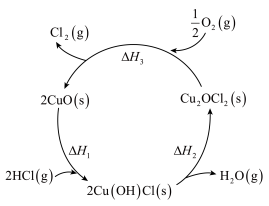
7近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
(2)Deacon直接氧化法可按下列催化过程进行:
CuCl2(s)=CuCl(s)+ Cl2(g) ΔH1=83kJ·mol-1
Cl2(g) ΔH1=83kJ·mol-1
CuCl(s)+ O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) ΔH2=-20kJ·mol-1
Cl2(g) ΔH2=-20kJ·mol-1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=-121kJ·mol-1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH=_______ kJ·mol-1。
 )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:(1)已知:
 (g)=
(g)= (g)+H2(g) ΔH1=100.3kJ·mol−1 ①
(g)+H2(g) ΔH1=100.3kJ·mol−1 ①H2(g)+I2(g)=2HI(g) ΔH2=﹣11.0kJ·mol−1 ②
对于反应:
 (g)+I2(g)=
(g)+I2(g)= (g)+2HI(g) ③ ΔH3=
(g)+2HI(g) ③ ΔH3=7近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
(2)Deacon直接氧化法可按下列催化过程进行:
CuCl2(s)=CuCl(s)+
 Cl2(g) ΔH1=83kJ·mol-1
Cl2(g) ΔH1=83kJ·mol-1CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+ Cl2(g) ΔH2=-20kJ·mol-1
Cl2(g) ΔH2=-20kJ·mol-1CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=-121kJ·mol-1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH=
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】利用盖斯定律回答下列问题:
已知热化学方程式
C(s、金刚石)+O2(g) → CO2(g) △H=-395.4kJ·mol—1
C(s、石墨)+O2(g) → CO2(g) △H = -393.5kJ·mol—1
由金刚石转化为石墨的热化学方程式为______________ ,由热化学反应方程式看来,更稳定的碳的同素异形体是__________ 。
已知热化学方程式
C(s、金刚石)+O2(g) → CO2(g) △H=-395.4kJ·mol—1
C(s、石墨)+O2(g) → CO2(g) △H = -393.5kJ·mol—1
由金刚石转化为石墨的热化学方程式为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】2SO2(g)+ O2(g) 2SO3(g)反应过程的能虽变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的△H= -99kJ / mol.
2SO3(g)反应过程的能虽变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的△H= -99kJ / mol.
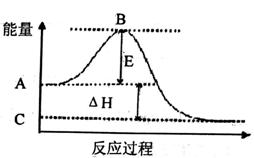
请回答下列问题:
①E的大小对该反应的反应热_______ (填“有”或“无”)影响。
②图中△H =_____ kJ/mol。
 2SO3(g)反应过程的能虽变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的△H= -99kJ / mol.
2SO3(g)反应过程的能虽变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的△H= -99kJ / mol.
请回答下列问题:
①E的大小对该反应的反应热
②图中△H =
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】二甲醚(CH3OCH。)和甲醇(CH3OH)被称为21世纪的新型燃料,具有清洁、高效等优良的性能。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
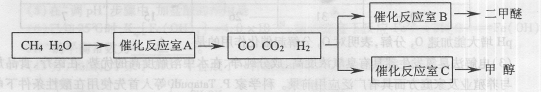
(1)催化反应室B中CO与H2合成二甲醚的化学方程式为____ 。
(2)催化反应室A中发生的反应为:
CH4(g)+H2O(g)⇌CO(g)+3H2(g)……(I)
CO(g)+H2O(g)⇌CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO(g)+2H2(g)⇌CH3OH(g)……(Ⅲ)
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)……(Ⅳ)
①已知:原子利用率=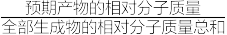 ×100%,试求反应(Ⅳ)的原子利用率为
×100%,试求反应(Ⅳ)的原子利用率为____ 。
②反应(Ⅳ)的△S____ 0(填“>”、“=”或“<”)。
③在压强为5MPa,体积为VL的反应室c中,amol CO与20mol H2在催化剂作用下发生反应(Ⅲ)生成甲醇,CO的转化率与温度的关系如图。则该反应的△H____ 0(填“>”、“=”或“<”)。300℃时该反应的平衡常数K=____ (用含字母的代数式表示)。

(3)我国某科研所提供一种碱性“直接二甲醚燃料电池”。
该燃料电池负极的电极反应式为:CH3OCH3-12e-+16OH-=2CO +11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
+11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
①将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液;
②将电解饱和食盐水所得气体反应后制得盐酸;
③将盐酸加入NaHSO3溶液中得SO2气体回收。
用上述碱性“直接二甲醚燃料电池”电解食盐水来处理标准状况下VL的废气,计算消耗二甲醚的质量____ 。
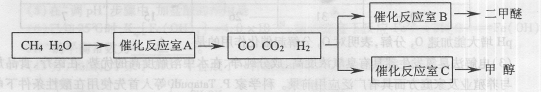
(1)催化反应室B中CO与H2合成二甲醚的化学方程式为
(2)催化反应室A中发生的反应为:
CH4(g)+H2O(g)⇌CO(g)+3H2(g)……(I)
CO(g)+H2O(g)⇌CO2(g)+H2(g)……(Ⅱ)催化反应室C中发生的反应为:
CO(g)+2H2(g)⇌CH3OH(g)……(Ⅲ)
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)……(Ⅳ)
①已知:原子利用率=
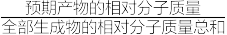 ×100%,试求反应(Ⅳ)的原子利用率为
×100%,试求反应(Ⅳ)的原子利用率为②反应(Ⅳ)的△S
③在压强为5MPa,体积为VL的反应室c中,amol CO与20mol H2在催化剂作用下发生反应(Ⅲ)生成甲醇,CO的转化率与温度的关系如图。则该反应的△H

(3)我国某科研所提供一种碱性“直接二甲醚燃料电池”。
该燃料电池负极的电极反应式为:CH3OCH3-12e-+16OH-=2CO
 +11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:
+11H2O。有人提出了一种利用氯碱工业产品治理含二氧化硫(体积分数为x)废气的方法如下:①将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液;
②将电解饱和食盐水所得气体反应后制得盐酸;
③将盐酸加入NaHSO3溶液中得SO2气体回收。
用上述碱性“直接二甲醚燃料电池”电解食盐水来处理标准状况下VL的废气,计算消耗二甲醚的质量
您最近一年使用:0次

 2CO(g) ΔH1 K1
2CO(g) ΔH1 K1