单质碘(I2)在医药。分析等方面应用广泛,回答下列问题
(1)碘酊又称碘酒,常用于皮肤消毒。它是由I2、KI分散于乙醇后形成的分散系。碘酊中分散剂为___________ ,该分散系属于___________ (选填“胶体”“浊液”“溶液”)。
(2)I2加热易升华,升华时下列物理量增大的是___________(选填编号)
(3)用CCl4提取碘水中I2,萃取后单质碘主要在___________ 层(选填“上”“下”),理由是___________ 。碘量法测定氧化铜样品中CuO含量步骤如下:取2.00g氧化铜样品溶于足量稀硫酸(假设杂质不参与反应),充分反应后过滤。再向滤液中加入过量KI溶液反应,最后当加入90mL 0.20mol/LNa2S2O3溶液恰好完全反应。主要反应原理为:
2CuSO4+4KI=2CuI↓+I2+2K2SO4
2Na2S2O3+I2=2NaI+Na2S4O6
(4)配置上述Na2S2O3溶液所需的定量仪器有___________ 。
(5)上述氧化铜样品中CuO的质量分数为___________ 。若配制Na2S2O3溶液时俯视读数,则测量结果___________ (选填“偏小”“偏大”“不变”)
(1)碘酊又称碘酒,常用于皮肤消毒。它是由I2、KI分散于乙醇后形成的分散系。碘酊中分散剂为
(2)I2加热易升华,升华时下列物理量增大的是___________(选填编号)
| A.分子间作用力 | B.分子间的平均距离 | C.分子的数目 | D.分子的质量 |
2CuSO4+4KI=2CuI↓+I2+2K2SO4
2Na2S2O3+I2=2NaI+Na2S4O6
(4)配置上述Na2S2O3溶液所需的定量仪器有
(5)上述氧化铜样品中CuO的质量分数为
更新时间:2021-12-02 08:19:39
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】将少量FeCl3的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③
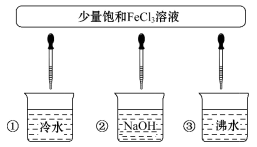
(1)将③继续加热煮沸至液体呈红褐色,反应的化学方程式为_______ 。
(2)如何用最简单的方法判断③中是否成功制备胶体?_______ 。

(1)将③继续加热煮沸至液体呈红褐色,反应的化学方程式为
(2)如何用最简单的方法判断③中是否成功制备胶体?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】胶体和溶液、浊液都是我们生活中常见的分散系,具有特殊性质,生活中常利用其性质。
(1)新冠病毒可以通过气溶胶传播,气溶胶属于胶体的一种,下列叙述错误的是________。
实验室可制备 胶体供学生探究胶体的性质,具体操作方法为:沸腾的蒸馏水中逐滴加入饱和
胶体供学生探究胶体的性质,具体操作方法为:沸腾的蒸馏水中逐滴加入饱和 溶液,继续煮沸至烧杯内液体呈均匀红褐色后停止加热。
溶液,继续煮沸至烧杯内液体呈均匀红褐色后停止加热。
(2)以上反应的化学方程式为:___________ 。
(3)某同学在制备过程中未使用洁净的烧杯(残留少量 固体),加水煮沸并滴入饱和
固体),加水煮沸并滴入饱和 后,观察到产生红褐色沉淀,因为
后,观察到产生红褐色沉淀,因为___________ 。
在一篇关于“生活中的胶体”文章中,介绍了如何利用牛奶或淀粉等生活中常见物质制备胶体,如将少量淀粉分散在水中可得无色澄清透明的淀粉溶液。某同学对“淀粉溶液”这种说法产生了疑惑,为探究“淀粉溶液”到底是溶液还是胶体,同学取材于生活常见材料设计了如下实验:
甲同学预先将少量碘酒溶于水,配置成碘水,并准备如图搭建实验装置。

(4)实验前,甲同学设计了如下表格以记录现象并分析结论:
(5)实际实验过程中,同学不仅观察到了如编号2所预测的实验现象,还观察到了半透膜内的淀粉溶液变蓝,从分散质粒径角度分析产生这两个现象的原因:___________ 。
(1)新冠病毒可以通过气溶胶传播,气溶胶属于胶体的一种,下列叙述错误的是________。
| A.胶体金抗原检测试纸保质期较长,体现了胶体的稳定性 |
| B.在电压作用下,带电胶体微粒可以发生电泳 |
| C.溶液呈电中性,而胶体带电,不呈电中性 |
| D.雾是气溶胶,在阳光下可以观察到丁达尔现象 |
实验室可制备
 胶体供学生探究胶体的性质,具体操作方法为:沸腾的蒸馏水中逐滴加入饱和
胶体供学生探究胶体的性质,具体操作方法为:沸腾的蒸馏水中逐滴加入饱和 溶液,继续煮沸至烧杯内液体呈均匀红褐色后停止加热。
溶液,继续煮沸至烧杯内液体呈均匀红褐色后停止加热。(2)以上反应的化学方程式为:
(3)某同学在制备过程中未使用洁净的烧杯(残留少量
 固体),加水煮沸并滴入饱和
固体),加水煮沸并滴入饱和 后,观察到产生红褐色沉淀,因为
后,观察到产生红褐色沉淀,因为在一篇关于“生活中的胶体”文章中,介绍了如何利用牛奶或淀粉等生活中常见物质制备胶体,如将少量淀粉分散在水中可得无色澄清透明的淀粉溶液。某同学对“淀粉溶液”这种说法产生了疑惑,为探究“淀粉溶液”到底是溶液还是胶体,同学取材于生活常见材料设计了如下实验:
甲同学预先将少量碘酒溶于水,配置成碘水,并准备如图搭建实验装置。

(4)实验前,甲同学设计了如下表格以记录现象并分析结论:
| 编号 | 实验现象 | 实验结论 |
| 1 | 烧杯中溶液呈 | “淀粉溶液”是溶液 |
| 2 | 烧杯中溶液呈 | “淀粉溶液”是胶体 |
(5)实际实验过程中,同学不仅观察到了如编号2所预测的实验现象,还观察到了半透膜内的淀粉溶液变蓝,从分散质粒径角度分析产生这两个现象的原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)证明明胶溶于水形成的分散系是胶体的最简单的方法是_______ 。
(2)现有10 mL明胶溶于水形成的分散系与5 mL NaCl溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明NaCl中Cl-能够透过半透膜:_______ 。
(3)取少量Fe2O3粉末(红棕色)加入适量盐酸,反应后得到饱和的FeCl3溶液呈棕黄色。用此溶液进行以下实验:
①取少量FeCl3溶液置于试管中,滴入氨水,可观察到有红褐色沉淀生成,反应的离子方程式为_______ 。
②在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至液体呈红褐色,停止加热。写出该制备过程的化学方程式:_______ 。
③以上①、②实验制备的分散系最本质的区别为_______ 。
(1)证明明胶溶于水形成的分散系是胶体的最简单的方法是
(2)现有10 mL明胶溶于水形成的分散系与5 mL NaCl溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明NaCl中Cl-能够透过半透膜:
(3)取少量Fe2O3粉末(红棕色)加入适量盐酸,反应后得到饱和的FeCl3溶液呈棕黄色。用此溶液进行以下实验:
①取少量FeCl3溶液置于试管中,滴入氨水,可观察到有红褐色沉淀生成,反应的离子方程式为
②在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至液体呈红褐色,停止加热。写出该制备过程的化学方程式:
③以上①、②实验制备的分散系最本质的区别为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有六种原子序数依次增大的短周期主族元素A、B、C、D、E、F。
已知信息如下:
①A是原子半径最小的元素,B是空气中含量最多的元素
②D是短周期元素中金属性最强的元素;
③部分元素在周期表中的相对位置如图所示;
请回答下列问题:
(1)A与F形成的化合物的结构式为___________ ;仅由A、C形成的18e-的化合物的分子式为___________ ;写出 E离子的结构示意图_______
(2)B、C、D、E 的原子半径由大到小的顺序为___________ (填元素符号),简单离子半径由大到小的顺序为___________ (填离子符号)。
(3)上述元素对应的最高价含氧酸中酸性最强的是___________ (填化学式,下同)。C、E形成的最简单氢化物中沸点由高到低的顺序为___________ 。
已知信息如下:
①A是原子半径最小的元素,B是空气中含量最多的元素
②D是短周期元素中金属性最强的元素;
③部分元素在周期表中的相对位置如图所示;
| B | C |
| E |
(1)A与F形成的化合物的结构式为
(2)B、C、D、E 的原子半径由大到小的顺序为
(3)上述元素对应的最高价含氧酸中酸性最强的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铂(Pt)的单质又称白金,是常用的催化剂和电极材料,顺二氨环丁羧酸铂(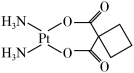 )又名卡铂,是一种低毒性抗癌药,遇光易分解。请回答下列问题:
)又名卡铂,是一种低毒性抗癌药,遇光易分解。请回答下列问题:
(1)用酒精把铂丝润湿点燃,酒精剧烈燃烧,使铂丝温度达到炽热程度,同时伴有很亮的光。产生上述现象可能的原因是___________ 。
(2)卡铂分子中非金属元素的电负性由大到小的顺序为___________ ,碳原子的杂化轨道类型有___________ 。
(3)卡铂静脉注射时需要注意的事项是___________ 。
(4)卡铂分子中存在的作用力有___________(填标号)。
(5)合成卡铂的中间体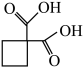 沸点比图1中化合物沸点低,原因是
沸点比图1中化合物沸点低,原因是___________ 。
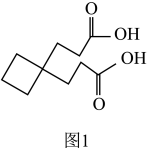
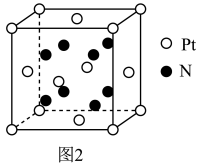
(6)超硬材料(仅次于金刚石)氮化铂的一种晶胞如图2所示,N的配位数是___________ 。
 )又名卡铂,是一种低毒性抗癌药,遇光易分解。请回答下列问题:
)又名卡铂,是一种低毒性抗癌药,遇光易分解。请回答下列问题:(1)用酒精把铂丝润湿点燃,酒精剧烈燃烧,使铂丝温度达到炽热程度,同时伴有很亮的光。产生上述现象可能的原因是
(2)卡铂分子中非金属元素的电负性由大到小的顺序为
(3)卡铂静脉注射时需要注意的事项是
(4)卡铂分子中存在的作用力有___________(填标号)。
| A.离子键 | B.配位键 | C.金属键 | D.非极性键 |
 沸点比图1中化合物沸点低,原因是
沸点比图1中化合物沸点低,原因是
(6)超硬材料(仅次于金刚石)氮化铂的一种晶胞如图2所示,N的配位数是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】依据物质结构与性质回答下列问题:
(1)在① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 六种分子中,碳原子采取
六种分子中,碳原子采取 杂化的分子有
杂化的分子有_______ (填序号), 分子的空间结构是
分子的空间结构是_______ 。 与
与 相比,
相比,_______ 的熔点较高。
(2)碘的相关化合物在化工、医药、材料等领域有着广泛的应用。X射线衍射测定等发现,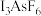 中存在
中存在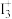 ,
,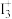 的空间结构为
的空间结构为_______ ,中心原子的杂化轨道类型为_______ 。
(3) 有机合成中常用的还原剂,
有机合成中常用的还原剂, 中的阴离子空间结构是
中的阴离子空间结构是_______ ,中心原子的杂化轨道类型为_______ 。
(1)在①
 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 六种分子中,碳原子采取
六种分子中,碳原子采取 杂化的分子有
杂化的分子有 分子的空间结构是
分子的空间结构是 与
与 相比,
相比,(2)碘的相关化合物在化工、医药、材料等领域有着广泛的应用。X射线衍射测定等发现,
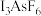 中存在
中存在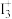 ,
,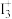 的空间结构为
的空间结构为(3)
 有机合成中常用的还原剂,
有机合成中常用的还原剂, 中的阴离子空间结构是
中的阴离子空间结构是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室要配制480mL 0.2 mol·L-1 NaCl溶液,实验室只有含有少量硫酸钠的氯化钠样品,设计如下方案,请回答下列问题:

Ⅰ.粗盐提纯
(1)固体A的成分为________________ (填化学式)。
(2)试剂2的化学式为_____________ ,判断试剂2是否过量的方法_______________ ,操作2的名称__________________ 。
Ⅱ.配制溶液
(1)用托盘天平称取氯化钠,其质量为________ g。
(2)配制过程中需要使用的实验仪器除了托盘天平、药匙、量筒、玻璃棒、烧杯、胶头滴管外,还需要___________ 。
(3)下列主要操作步骤的正确顺序是①—____ —_____ — ____ —④(填序号)。
①称取一定质量的氯化钠,放入烧杯中,用适量蒸馏水溶解
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
③将溶液转移到容量瓶中
④盖好瓶塞,反复上下颠倒,摇匀
⑤用少量的蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中
(4)下列情况对所配制的NaCl溶液浓度有何影响?(选填“偏大”、“偏小”或“无影响”)
①容量瓶用蒸馏洗涤后残留有少量的水________________ ;
②定容时,仰视容量瓶的刻度线________________ ;
③转移溶液时,玻璃棒的下端靠在容量瓶的刻度线以上的内壁________________ 。

Ⅰ.粗盐提纯
(1)固体A的成分为
(2)试剂2的化学式为
Ⅱ.配制溶液
(1)用托盘天平称取氯化钠,其质量为
(2)配制过程中需要使用的实验仪器除了托盘天平、药匙、量筒、玻璃棒、烧杯、胶头滴管外,还需要
(3)下列主要操作步骤的正确顺序是①—
①称取一定质量的氯化钠,放入烧杯中,用适量蒸馏水溶解
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
③将溶液转移到容量瓶中
④盖好瓶塞,反复上下颠倒,摇匀
⑤用少量的蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中
(4)下列情况对所配制的NaCl溶液浓度有何影响?(选填“偏大”、“偏小”或“无影响”)
①容量瓶用蒸馏洗涤后残留有少量的水
②定容时,仰视容量瓶的刻度线
③转移溶液时,玻璃棒的下端靠在容量瓶的刻度线以上的内壁
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】(I)化学是一门以实验为基础的学科,化学所取得的丰硕成果与实验的重要作用分不开。结合下列实验装置图回答问题:
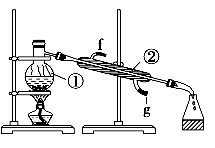
(1)写出上图中所示仪器的名称:①___ ;②___ 。
(2)若利用该装置分离乙酸(沸点118 ℃)和乙酸乙酯(沸点77.1 ℃)的混合物,还缺少的仪器有___ ,将仪器补充完整后进行的实验操作的名称为___ ;实验时仪器②中冷却水的进口为________ (填“f”或“g”)。
(3)应用上述分离操作,首先得到的物质是________ 。
(4)蒸馏烧瓶内碎瓷片的作用是________________ 。
(Ⅱ)硫酸试剂瓶标签上的内容:

(1)该硫酸的物质的量浓度是________ mol·L-1。
(2)某化学兴趣小组进行硫酸性质的实验探究时,需要240 mL 4.6 mol·L-1的稀硫酸,则配制稀硫酸时需要取________ mL的该硫酸;配制时需选用的仪器主要有量筒、烧杯、玻璃棒、___ 、___ (在横线上填写所缺仪器的名称)。
(3)配制过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是___ (填序号)。
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液并定容
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线

(1)写出上图中所示仪器的名称:①
(2)若利用该装置分离乙酸(沸点118 ℃)和乙酸乙酯(沸点77.1 ℃)的混合物,还缺少的仪器有
(3)应用上述分离操作,首先得到的物质是
(4)蒸馏烧瓶内碎瓷片的作用是
(Ⅱ)硫酸试剂瓶标签上的内容:

(1)该硫酸的物质的量浓度是
(2)某化学兴趣小组进行硫酸性质的实验探究时,需要240 mL 4.6 mol·L-1的稀硫酸,则配制稀硫酸时需要取
(3)配制过程中,下列操作会使配制的稀硫酸溶液浓度偏高的是
①量取浓硫酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液并定容
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验:某学生欲用18 mol/L的硫酸配制6.0 mol/L的H2SO4 1 000 mL,实验室有三种规格的容量瓶:250 mL、500 mL、1 000 mL。请回答下列问题:
(1)配制该硫酸溶液应选用容量瓶的规格为________ mL
(2)配制时,该同学的操作顺序如下,请将操作步骤A、C补充完整。
a.用量筒准确量取所需的18 mol/L的浓硫酸________ mL,沿玻璃棒倒入烧杯中,并用玻璃棒搅拌,使其混合均匀;
b.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
c.___________________ ;
d.振荡,继续向容量瓶中加水,直到液面接近刻度线1 cm~2 cm处;
e.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
f.将容量瓶盖紧,振荡,摇匀。
(3)如果省略操作c,对所配溶液浓度有何影响?______ (填“偏大”、“偏小”或“无影响”)。
(4)进行操作b前还需注意__________________ 。
(1)配制该硫酸溶液应选用容量瓶的规格为
(2)配制时,该同学的操作顺序如下,请将操作步骤A、C补充完整。
a.用量筒准确量取所需的18 mol/L的浓硫酸
b.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
c.
d.振荡,继续向容量瓶中加水,直到液面接近刻度线1 cm~2 cm处;
e.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
f.将容量瓶盖紧,振荡,摇匀。
(3)如果省略操作c,对所配溶液浓度有何影响?
(4)进行操作b前还需注意
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某小组同学探究久置FeSO4固体变质的情况,并测定其中铁元素的质量分数。将0.6gFeSO4固体用蒸馏水溶解,配成20mL待测液,进行实验。
资料:KSCN中S元素的化合价为﹣2价;酸性条件下,MnO 的还原产物为Mn2+。
的还原产物为Mn2+。
(1)实验一:
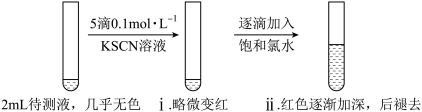
①i中溶液略微变红,说明待测液中存在_______ 。
②ii中溶液颜色逐渐加深的原因是_______ (用离子方程式表示)。
③由实验一推测FeSO4固体变质的情况是_______ (填字母序号)。
a.未变质 b.部分变质 c.完全变质
(2)实验二:探究ii中“红色褪去”的原因。
针对“红色褪去”的现象,小组同学猜想可能的原因是_______ ,并通过如下实验证实了猜想。将褪色后的溶液分两份分别进行实验:
请补全②中的现象:_______ 。
(3)实验三:测定久置FeSO4固体中铁元素的含量,设计实验方案如图:

①可选作A的物质是_______ (填字母序号)。
a.Zn b.Cu c.Fe d.KI
②若消耗0.1mol/LKMnO4溶液3.6mL,则久置FeSO4固体中铁元素的质量分数是_______ 。
资料:KSCN中S元素的化合价为﹣2价;酸性条件下,MnO
 的还原产物为Mn2+。
的还原产物为Mn2+。(1)实验一:

①i中溶液略微变红,说明待测液中存在
②ii中溶液颜色逐渐加深的原因是
③由实验一推测FeSO4固体变质的情况是
a.未变质 b.部分变质 c.完全变质
(2)实验二:探究ii中“红色褪去”的原因。
针对“红色褪去”的现象,小组同学猜想可能的原因是
| 序号 | 操作 | 现象 |
| ① | 滴加NaOH溶液 | 产生红褐色沉淀 |
| ② | 滴加FeCl3溶液 | _______ |
(3)实验三:测定久置FeSO4固体中铁元素的含量,设计实验方案如图:

①可选作A的物质是
a.Zn b.Cu c.Fe d.KI
②若消耗0.1mol/LKMnO4溶液3.6mL,则久置FeSO4固体中铁元素的质量分数是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】二茂铁可用作燃料的节能消烟剂,熔点173℃,沸点249℃,在100℃以上能升华。二茂铁的实验室制备原理是: ,制备装置如图一所示,实验操作步骤如下:
,制备装置如图一所示,实验操作步骤如下:

①在三颈烧瓶中加入28g粉末状的KOH,并从仪器a中加入60mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a滴入6.6mL新蒸馏的环戊二烯(C5H6,密度为0.95g·cm3),搅拌;
③将6.35g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25mL装入仪器a中,慢慢滴入仪器c中,45min滴完,继续搅拌45min;
④再从仪器a加入25mL无水乙醚搅拌;
⑤将c中的液体转入分液漏斗中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品;
⑦…。
回答下列问题:
(1)仪器c的名称是___________ ,仪器b的作用___________ 。
(2)步骤①中通入氮气的目的是___________ 。
(3)仪器c的适宜容积为___________ (填序号)。
A.100mL B.250mL C.500mL
(4)步骤⑤用盐酸洗涤的目的是___________ 。
(5)步骤⑦是二茂铁粗产品的提纯,该过程在图二装置中进行,其操作名称为___________ ;该操作中棉花的作用是___________ 。
(6)若最终制得纯净的二茂铁4.65g,则该实验的产率为___________ 。
 ,制备装置如图一所示,实验操作步骤如下:
,制备装置如图一所示,实验操作步骤如下:
①在三颈烧瓶中加入28g粉末状的KOH,并从仪器a中加入60mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a滴入6.6mL新蒸馏的环戊二烯(C5H6,密度为0.95g·cm3),搅拌;
③将6.35g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25mL装入仪器a中,慢慢滴入仪器c中,45min滴完,继续搅拌45min;
④再从仪器a加入25mL无水乙醚搅拌;
⑤将c中的液体转入分液漏斗中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品;
⑦…。
回答下列问题:
(1)仪器c的名称是
(2)步骤①中通入氮气的目的是
(3)仪器c的适宜容积为
A.100mL B.250mL C.500mL
(4)步骤⑤用盐酸洗涤的目的是
(5)步骤⑦是二茂铁粗产品的提纯,该过程在图二装置中进行,其操作名称为
(6)若最终制得纯净的二茂铁4.65g,则该实验的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】草酸亚铁晶体(FeC2O4·2H2O,M=180g/mol)呈淡黄色,可用作晒制蓝图。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如下装置可重复选用)进行实验:
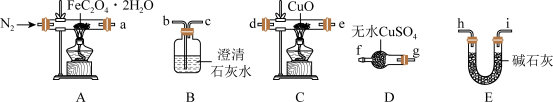
①E中盛装碱石灰的仪器名称为_________ 。
②按照气流从左到右的方向,上述装置的接口顺序为a→g→f→_____ →尾气处理装置(仪器可重复使用)。
③实验前先通入一段时间N2,其目的为__________________ 。
④实验证明了气体产物中含有CO,依据的实验现象为_____________ 。
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为____________________ 。
(3)晒制蓝图时,以K3[Fe(CN)6]溶液为显色剂,该反应的化学方程式为______________ 。
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀HSO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用 cmol/L KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用 cmol/L KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为______________ ;步骤3中加入锌粉的目的为_______ 。
(5)草酸亚铁晶体样品的纯度为________ ;若步骤1配制溶液时部分Fe2+被氧化变质,则测定结果将____ (填“偏高”、“偏低”或“不变”)。
I.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如下装置可重复选用)进行实验:

①E中盛装碱石灰的仪器名称为
②按照气流从左到右的方向,上述装置的接口顺序为a→g→f→
③实验前先通入一段时间N2,其目的为
④实验证明了气体产物中含有CO,依据的实验现象为
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(3)晒制蓝图时,以K3[Fe(CN)6]溶液为显色剂,该反应的化学方程式为
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀HSO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用 cmol/L KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用 cmol/L KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为
(5)草酸亚铁晶体样品的纯度为
您最近一年使用:0次



