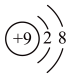
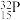对于第VIIA族元素,从上到下,下列关于其性质变化的叙述中,错误的是
| A.原子半径逐渐增大 | B.电负性逐渐减小 |
| C.第一电离能逐渐减小 | D.氢化物水溶液的酸性逐渐减弱 |
更新时间:2021-12-03 09:07:47
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】锂(Li)是世界上最轻的金属,它属于碱金属的一种。下列关于碱金属的说法正确的是
| A.和锂在同一主族的都是金属元素 |
| B.Na+比Li多一个电子层 |
| C.Li、Na、K、Rb+的最外层都只有一个电子 |
| D.Li是碱金属原子中半径最小的原子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列有关叙述错误的是
| A.碱性:NaOH>KOH | B.原子半径:r(C)>r(O) |
| C.稳定性:HF>PH3 | D.氧化性:Al3+>Ca2+ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知短周期元素的离子:aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A.原子半径 A>B>D>C | B.原子序数 d>c>b>a |
| C.离子半径 C>D>B>A | D.阴离子的还原性C2-< D- |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】短周期主族元素A、C、D、E、F和G原子序数依次递增,其中A的原子半径最小,C是空气中含量最多的元素,D是地壳中含量最多的元素,E、F和G同周期,E在该周期中原子半径最大,F的单质中有一种是淡黄色的固体。下列说法错误的是
| A.原子半径:E>F>G>C>D>A |
| B.氧化物对应的水化物酸性:F<G |
| C.D与E、E与G均可形成离子化合物 |
D.A与E形成的化合物电子式为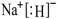 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列关于元素的说法正确的是
| A.基态原子失去一个电子转化为基态正离子所需要的能量叫做第一电离能 |
| B.钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠 |
| C.金属的电负性小于1.8,而非金属的电负性大于1.8 |
| D.元素的电负性越大,非金属性就越强,元素原子的第一电离就越大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】元素周期表是学习物质结构与性质的重要工具,如图所示是元素周期表前三周期的一部分。关于下列五种元素的叙述正确的是
| X | |||
| W | Y | Z | R |
| A.Z的基态原子最外层p轨道上有2个未成对电子 |
| B.WZ3的空间结构为平面三角形 |
| C.H2Y键角小于YX3 |
| D.第一电离能:R> Y> W |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】磷化铜(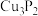 )用于制造磷青铜,磷青铜是含少量金属锡、磷的铜合金,主要用作耐磨零件和弹性原件,磷化铜与水作用产生有毒的
)用于制造磷青铜,磷青铜是含少量金属锡、磷的铜合金,主要用作耐磨零件和弹性原件,磷化铜与水作用产生有毒的 ,下列判断错误的是
,下列判断错误的是
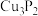 )用于制造磷青铜,磷青铜是含少量金属锡、磷的铜合金,主要用作耐磨零件和弹性原件,磷化铜与水作用产生有毒的
)用于制造磷青铜,磷青铜是含少量金属锡、磷的铜合金,主要用作耐磨零件和弹性原件,磷化铜与水作用产生有毒的 ,下列判断错误的是
,下列判断错误的是A. 中心原子的杂化方式为 中心原子的杂化方式为 |
| B.电负性:Cu<P |
C.熔沸点: > > |
D.基态Cu原子的价电子轨道表示式为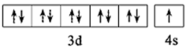 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法中正确的是 ( )
①第一电离能:S>P>Si②电负性:C<N<O<F
③因为CaO的晶格能比KCl的高,所以KCl的熔点比CaO的低
④SO2与CO2的化学性质类似,分子结构也呈直线形,相同条件下SO2的溶解度更大
⑤分子晶体中,共价键键能越大,该分子晶体的熔、沸点越高
①第一电离能:S>P>Si②电负性:C<N<O<F
③因为CaO的晶格能比KCl的高,所以KCl的熔点比CaO的低
④SO2与CO2的化学性质类似,分子结构也呈直线形,相同条件下SO2的溶解度更大
⑤分子晶体中,共价键键能越大,该分子晶体的熔、沸点越高
| A.①②③ | B.②③ | C.②④⑤ | D.①②③④⑤ |
您最近一年使用:0次

 原子最高能级电子云轮廓图:
原子最高能级电子云轮廓图:
 的结构示意图:
的结构示意图: