在下图所示的物质转化关系中,A是常见的气态氢化物,B是能使带火星的木条复燃的无色、无味气体,E的相对分子质量比D的大17,G是一种紫红色金属单质(反应条件和部分生成物未列出)。
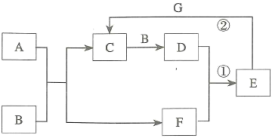
(1)A的电子式为___________ ,B的化学式为___________ 。
(2)请写出:
反应①的化学方程式_________
反应②的离子方程式____________ 。

(1)A的电子式为
(2)请写出:
反应①的化学方程式
反应②的离子方程式
更新时间:2021-12-02 21:30:50
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】图示表示物质X、Y、Z、W在一定条件下可以按照箭头一步转化。
(1)X是金属单质,焰色反应呈黄色;Y的纯净物易潮解;Z可用于治疗胃酸过多;X在黄绿色的气体中燃烧可以产生白烟W(已知:电解熔融态的W可以得到X)。
X是:___________ Y是:___________ Z是:__________ W是:__________ (填写化学式)
(2)Z具有漂白性,但是不稳定,易分解产生含氯化合物。Z是:________ (填写化学式)
(3)鉴别X、Y可以滴加___________ 溶液,前者出现血红色。(填写名称)
| 序号 | X | Y | Z | W | 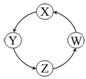 |
| (1) | |||||
| (2) |  | 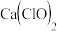 | |||
| (3) |  |  |
X是:
(2)Z具有漂白性,但是不稳定,易分解产生含氯化合物。Z是:
(3)鉴别X、Y可以滴加
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知:A、C均为常见的单质,B、D为常见的化合物,它们在一定条件下有
如下转化关系:A + B→C + D。
⑴ 若A、C均为生活中常见金属,B 为红棕色固体,D既能与盐酸,又能与氢氧化钠溶液反应,则组成A单质的元素在周期表中的位置为_______________ ;请写出该反应的化学方程式:_____________________________ ;A和B所具有的总能量_____ (填“大于”、“小于”或“等于”)C和D所具有的总能量。
⑵ 若A、C分别是由原子序数相差8的非金属元素组成的固体单质,B是一种不溶于水的酸性氧化物。请写出该反应的化学方程式:______________________ ,则该反应中氧化剂和还原剂的物质的量之比为__________ 。
⑶ 若组成A单质的元素可形成带两个单位正电荷的阳离子,且具有与氖原子相同的电子层结构, C为黑色固态单质,该反应的化学方程式是____________________ ,B为__________ 分子(填“极性”或“非极性”),D存在化学键的类型为____________ 。
如下转化关系:A + B→C + D。
⑴ 若A、C均为生活中常见金属,B 为红棕色固体,D既能与盐酸,又能与氢氧化钠溶液反应,则组成A单质的元素在周期表中的位置为
⑵ 若A、C分别是由原子序数相差8的非金属元素组成的固体单质,B是一种不溶于水的酸性氧化物。请写出该反应的化学方程式:
⑶ 若组成A单质的元素可形成带两个单位正电荷的阳离子,且具有与氖原子相同的电子层结构, C为黑色固态单质,该反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知:溶液E焰色反应为黄色。
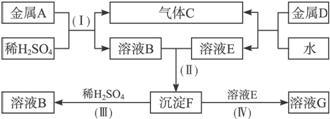
根据以上转化关系,回答下列问题:
(1)写出下面物质的化学式:
A______________ ,B____________ ,C_______________ ,D_____________ 。
(2)写出下列离子方程式:
(Ⅰ)___________________________ ;
(Ⅱ)___________________________ ;
(Ⅲ)___________________________ ;
(Ⅳ)_______________________________ 。

根据以上转化关系,回答下列问题:
(1)写出下面物质的化学式:
A
(2)写出下列离子方程式:
(Ⅰ)
(Ⅱ)
(Ⅲ)
(Ⅳ)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】甲、乙、丙三种物质之间有如下转化关系:
甲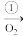 乙
乙 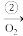 丙
丙  丁
丁
(1)若甲是一种黄色固体物质,丁是一种常见的酸,则丁是_______________ ,写出 ②的化学方程式:________________ 。
(2)若甲是一种极易溶于水的气体,丙是一种红棕色气体,则丙物质是____________ 。写出 ①的化学方程式_______________ 。
甲
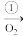 乙
乙 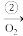 丙
丙  丁
丁(1)若甲是一种黄色固体物质,丁是一种常见的酸,则丁是
(2)若甲是一种极易溶于水的气体,丙是一种红棕色气体,则丙物质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】化合物X由四种常见元素组成,某实验小组为探究其组成进行了如图实验:
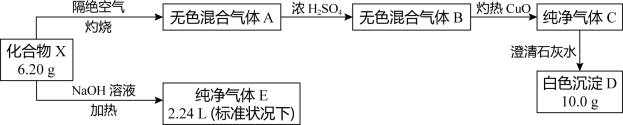
已知:①纯净气体E能使湿润的红色石蕊试纸变蓝色;②流程中所用转化试剂均过量。
请回答下列问题:
(1)化合物X中所含的元素有H、O和_______ , X的化学式为_______ 。
(2)写出化台物X隔绝空气灼烧生成混合气体A的化学方程式_______ 。
(3)在实验室,X常用作沉淀剂。写出化合物X与CaCl2溶液反应的离子方程式_______ 。
(4)气体E也能与灼热CuO发生氧化还原反应,只生成一种固体产物。 请推测固体产物的组成(假设CuO完全反应)_______ ,并设计实验方案验证之_______ 。
(5)某同学认为可以用点燃的方法将混合气体B转变为纯净气体C,你认为是否可行,并说明理由_______ 。

已知:①纯净气体E能使湿润的红色石蕊试纸变蓝色;②流程中所用转化试剂均过量。
请回答下列问题:
(1)化合物X中所含的元素有H、O和
(2)写出化台物X隔绝空气灼烧生成混合气体A的化学方程式
(3)在实验室,X常用作沉淀剂。写出化合物X与CaCl2溶液反应的离子方程式
(4)气体E也能与灼热CuO发生氧化还原反应,只生成一种固体产物。 请推测固体产物的组成(假设CuO完全反应)
(5)某同学认为可以用点燃的方法将混合气体B转变为纯净气体C,你认为是否可行,并说明理由
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氮元素形成的化合物种类十分丰富。
⑴请回答下列有关NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:________________
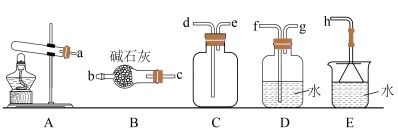
②欲收集一瓶干燥的氨气,选择下图中的装置,其连接顺序为:a →___________ (按气流方向,用小写字母表示)。
③ 氨气的催化氧化的化学方程式为___________________________________________
⑵ 工业生产中利用氨水吸收SO2和NO2,原理如下图所示
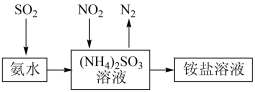
写出 NO2被吸收过程的离子方程式:__________________________________ 。
⑴请回答下列有关NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:
②欲收集一瓶干燥的氨气,选择下图中的装置,其连接顺序为:a →

③ 氨气的催化氧化的化学方程式为
⑵ 工业生产中利用氨水吸收SO2和NO2,原理如下图所示

写出 NO2被吸收过程的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铜银合金在现代工业中有广泛应用。从铜银合金切割废料(不含其它金属)中回收银并制备铜化工产品的工艺如图。
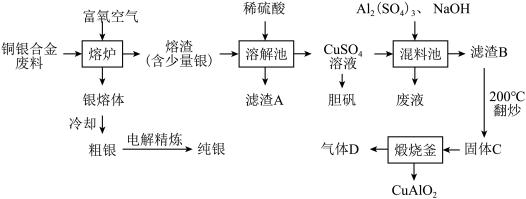
(1)向熔炉中通入适量富氧空气的目的是:___________ 。
(2)滤渣A溶于稀硝酸时产生无色气体,该反应的离子方程式为___________ 。
(3)在混料池中,将三种原料按一定的物质的量之比混合均匀,煮沸,过滤。将滤渣B在200℃下翻炒至质量不再变化,得到固体C.C只含CuO、Al2O3,物质的量之比为2:1。在惰性气体保护下,将C在煅烧釜中高温灼烧,得到CuAlO2.该反应的方程式为___________ 。
(4)若溶解所得溶液中含有1molCuSO4,则混料时应加入___________ molNaOH。
(5)冷却银熔体得到的粗银可使用电解法精炼,精炼池中阳极的电极反应为___________ 。
(6)该工艺中,可循环利用的物质为___________ 。

(1)向熔炉中通入适量富氧空气的目的是:
(2)滤渣A溶于稀硝酸时产生无色气体,该反应的离子方程式为
(3)在混料池中,将三种原料按一定的物质的量之比混合均匀,煮沸,过滤。将滤渣B在200℃下翻炒至质量不再变化,得到固体C.C只含CuO、Al2O3,物质的量之比为2:1。在惰性气体保护下,将C在煅烧釜中高温灼烧,得到CuAlO2.该反应的方程式为
(4)若溶解所得溶液中含有1molCuSO4,则混料时应加入
(5)冷却银熔体得到的粗银可使用电解法精炼,精炼池中阳极的电极反应为
(6)该工艺中,可循环利用的物质为
您最近一年使用:0次
【推荐2】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2。某同学在实验室中对NH3与NO2反应进行了探究。回答下列问题:
I.氨气的制备
某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。___________ ;B中圆底烧瓶收集氨气时,请你选择氨气的进气口___________ (填“a”或“b”)。
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是___________ ;你认为引发喷泉的操作应是___________ 。
(3)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是___________ (填序号)。
(4)铜和浓硝酸产生NO2的化学方程式是___________ 。
(5)将I中收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入(4)中产生的NO2(两端用夹子K1、K2夹好)。___________ ;反应的化学方程式___________ 。
(6)若有NO2和NH3的混合物1mol,充分反应。反应后所得到产物中,经氧化得到的N2比经还原得到的N2多1.4g,则反应混合物中NO2与NH3的体积比是___________
I.氨气的制备
某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。
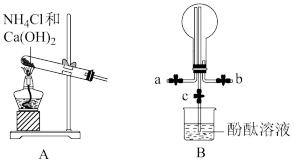
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(3)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是
①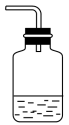 ②
②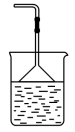 ③
③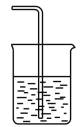 ④
④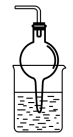
(4)铜和浓硝酸产生NO2的化学方程式是
(5)将I中收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入(4)中产生的NO2(两端用夹子K1、K2夹好)。
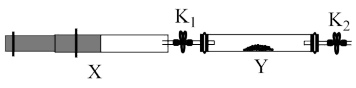
(6)若有NO2和NH3的混合物1mol,充分反应。反应后所得到产物中,经氧化得到的N2比经还原得到的N2多1.4g,则反应混合物中NO2与NH3的体积比是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硝酸铁是一种工业和医药行业常用的原料,用作媒染剂、铜着色剂等。Fe(NO3)3∙9H2O是浅紫色晶体,易溶于水、乙醇和丙酮。
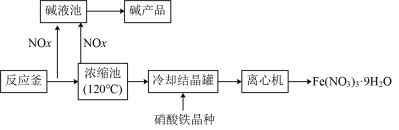
Ⅰ. 利用稀硝酸和铁屑制备硝酸铁。目前常见的生产流程如图所示。
(1)反应釜中原料是稀硝酸和细铁屑,反应的离子方程式是_______ 。硝酸需要过量,原因是_______ 。
(2) 会污染空气,不能随意排放,浓缩池中也会产生
会污染空气,不能随意排放,浓缩池中也会产生 ,请用化学用语解释产生
,请用化学用语解释产生 的原因
的原因_______ 。
(3)冷却结晶后的硝酸铁晶体,最适宜用下列哪种试剂进行洗涤_______。
Ⅱ. 利用工业废水制备硝酸铁。不锈钢酸洗废液中含有大量 、
、 、
、 等金属离子,可对不锈钢酸洗废液中的各金属元素进行分离,并利用分离的含铁物质制备硝酸铁,同时回收其他金属。
等金属离子,可对不锈钢酸洗废液中的各金属元素进行分离,并利用分离的含铁物质制备硝酸铁,同时回收其他金属。
已知:①Cr(OH)3是两性氢氧化物。
②各金属离子沉淀的范围如下表所示:
(4)分离出 适宜的
适宜的 范围是
范围是_______ 。
(5)请设计实验,继续从废液中分别分离出Cr元素和Ni元素_______ 。
Ⅰ. 利用稀硝酸和铁屑制备硝酸铁。目前常见的生产流程如图所示。

(1)反应釜中原料是稀硝酸和细铁屑,反应的离子方程式是
(2)
 会污染空气,不能随意排放,浓缩池中也会产生
会污染空气,不能随意排放,浓缩池中也会产生 ,请用化学用语解释产生
,请用化学用语解释产生 的原因
的原因(3)冷却结晶后的硝酸铁晶体,最适宜用下列哪种试剂进行洗涤_______。
| A.水 | B.四氯化碳 | C.20%稀硝酸 | D.乙醇 |
Ⅱ. 利用工业废水制备硝酸铁。不锈钢酸洗废液中含有大量
 、
、 、
、 等金属离子,可对不锈钢酸洗废液中的各金属元素进行分离,并利用分离的含铁物质制备硝酸铁,同时回收其他金属。
等金属离子,可对不锈钢酸洗废液中的各金属元素进行分离,并利用分离的含铁物质制备硝酸铁,同时回收其他金属。已知:①Cr(OH)3是两性氢氧化物。
②各金属离子沉淀的范围如下表所示:
 |  |  | |
开始沉淀 | 1.5 | 4.6 | 6.7 |
完全沉淀 | 3.2 | 6.9 | 9.5 |
 适宜的
适宜的 范围是
范围是(5)请设计实验,继续从废液中分别分离出Cr元素和Ni元素
您最近一年使用:0次



