为测定空气中 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的200mL0.100mol/L的酸性
的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的200mL0.100mol/L的酸性 溶液。已知
溶液。已知 与该溶液反应的离子方程式为:
与该溶液反应的离子方程式为: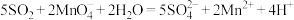 ,若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的
,若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的 可被溶液充分吸收,则该空气样品中
可被溶液充分吸收,则该空气样品中 的含量(单位为g/L)是
的含量(单位为g/L)是__________ 。
 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的200mL0.100mol/L的酸性
的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的200mL0.100mol/L的酸性 溶液。已知
溶液。已知 与该溶液反应的离子方程式为:
与该溶液反应的离子方程式为: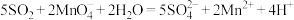 ,若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的
,若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的 可被溶液充分吸收,则该空气样品中
可被溶液充分吸收,则该空气样品中 的含量(单位为g/L)是
的含量(单位为g/L)是
更新时间:2021-12-02 21:30:50
|
【知识点】 二氧化硫的化学性质
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题。

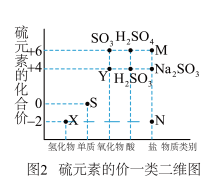
(1)图1中与图2中M、N对应的物质分别是___________ 、___________ 。(各写一个)
(2)写出物质X的电子式___________ 。
(3)SO2的排放是造成酸雨的主要因素,同时SO2在生活中也有多种用途。请回答下列问题:
①从环境保护的角度看,人们通常把pH<5.6的降水称为酸雨。已知pH=-lgc(H+)。经测定某次雨水中只含硫酸。且浓度为5×10-5mol/L,这次降雨___________ (填“是”或“不是”)酸雨。
②石灰石——石膏(CaSO4·2H2O)法是处理含SO2烟气脱硫的常见方法,该工艺原理是,将石灰石粉末加水制成浆液作为吸收剂与烟气充分混合并接触氧化。最终生成石膏。写出该过程发生反应的化学方程式___________ 。
③在酸酒时人工添加SO2有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入SO2,请用离子方程式表示该反应原理___________ 。
④发酵酒卫生标准中对葡萄酒中的二氧化硫含量有要求:总SO2小于250mg/L,若在室温下。每升溶液中最多通入___________ mLSO2.(室温下Vm=24L/mol)
(4)向BaCl2溶液中通入SO2至饱和,此过程看不到现象,再向溶液中加入一种物质。溶液变浑浊。加入的这种物质不可能是___________。


(1)图1中与图2中M、N对应的物质分别是
(2)写出物质X的电子式
(3)SO2的排放是造成酸雨的主要因素,同时SO2在生活中也有多种用途。请回答下列问题:
①从环境保护的角度看,人们通常把pH<5.6的降水称为酸雨。已知pH=-lgc(H+)。经测定某次雨水中只含硫酸。且浓度为5×10-5mol/L,这次降雨
②石灰石——石膏(CaSO4·2H2O)法是处理含SO2烟气脱硫的常见方法,该工艺原理是,将石灰石粉末加水制成浆液作为吸收剂与烟气充分混合并接触氧化。最终生成石膏。写出该过程发生反应的化学方程式
③在酸酒时人工添加SO2有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入SO2,请用离子方程式表示该反应原理
④发酵酒卫生标准中对葡萄酒中的二氧化硫含量有要求:总SO2小于250mg/L,若在室温下。每升溶液中最多通入
(4)向BaCl2溶液中通入SO2至饱和,此过程看不到现象,再向溶液中加入一种物质。溶液变浑浊。加入的这种物质不可能是___________。
| A.Cl2 | B.NH3 | C.CO2 | D.H2S |
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】碳酸锰(MnCO3) 是理想的高性能强磁性材料,也是制备Mn2O3、MnO2等锰的氧化物的重要原料,广泛用于电子、化工、医药等行业。
(1) 工业上制备方程式为:MnSO4+2NH4HCO3=MnCO3 ↓+ (NH4)2 SO4+CO2 ↑+H2O。反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4。加入稍过量的NH4HCO3的目的是_____ 。
(2) 实验室模拟工业二氧化锰制备硫酸锰装置如图4所示。
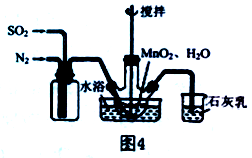
①石灰乳的作用是________ 。
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有________ 。
(3) MnCO3 在空气中加热易转化为不同价态的锰的氧化物,且其固体残留率随温度的变化如图5 中A、B、C、D 点所示。则300℃时,剩余固体中锰元素与氧元素的物质的量之比即n(Mn) :n(O)为_______ ; 图中点D 对应固体的成分为______ (填化学式)。

(1) 工业上制备方程式为:MnSO4+2NH4HCO3=MnCO3 ↓+ (NH4)2 SO4+CO2 ↑+H2O。反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4。加入稍过量的NH4HCO3的目的是
(2) 实验室模拟工业二氧化锰制备硫酸锰装置如图4所示。

①石灰乳的作用是
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有
(3) MnCO3 在空气中加热易转化为不同价态的锰的氧化物,且其固体残留率随温度的变化如图5 中A、B、C、D 点所示。则300℃时,剩余固体中锰元素与氧元素的物质的量之比即n(Mn) :n(O)为

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】硫的化合物在生产、生活中应用广泛。
(1)某兴趣小组探究SO2气体还原Fe3+、I2。
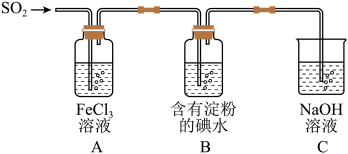
通入足量SO2后,装置B中的现象是___________ ,装置C的作用是___________ 。
(2)该小组同学认为SO2与FeCl3溶液发生的是氧化还原反应。写出为SO2与FeCl3溶液反应的离子方程式:___________ 。
(3)铬是环境中的一种主要污染物,可以用焦亚硫酸钠(Na2S2O5)处理含铬酸性废水(含有 ),利用氧化还原反应,将六价铬还原为三价铬,
),利用氧化还原反应,将六价铬还原为三价铬,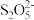 被氧化为
被氧化为 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)已知:Na2S2O5溶于水会生成NaHSO3。取Na2S2O5晶体于试管中,加入适量水溶解,滴入足量盐酸,再滴入氯化钡溶液,有白色沉淀。请推断可能的原因___________ 。
(1)某兴趣小组探究SO2气体还原Fe3+、I2。

通入足量SO2后,装置B中的现象是
(2)该小组同学认为SO2与FeCl3溶液发生的是氧化还原反应。写出为SO2与FeCl3溶液反应的离子方程式:
(3)铬是环境中的一种主要污染物,可以用焦亚硫酸钠(Na2S2O5)处理含铬酸性废水(含有
 ),利用氧化还原反应,将六价铬还原为三价铬,
),利用氧化还原反应,将六价铬还原为三价铬,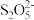 被氧化为
被氧化为 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为(4)已知:Na2S2O5溶于水会生成NaHSO3。取Na2S2O5晶体于试管中,加入适量水溶解,滴入足量盐酸,再滴入氯化钡溶液,有白色沉淀。请推断可能的原因
您最近一年使用:0次



