已知H与O可以形成 和
和 两种化合物。请完成下列空白:
两种化合物。请完成下列空白:
(1) 内的O—H、水分子间的范德华力和氢键,从强到弱依次为
内的O—H、水分子间的范德华力和氢键,从强到弱依次为___________ 。 可与
可与 形成
形成 ,
, 中O采用
中O采用___________ 杂化。 中
中 键角比
键角比 中的
中的___________ ,原因为___________ 。
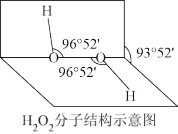
(2) 是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。
是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。 的电子式是
的电子式是___________ ,结构式是___________ 。 是含有
是含有___________ 键和___________ 键的分子(填“极性”或“非极性”)。 能与水混溶,却不溶于
能与水混溶,却不溶于 。请予以解释:
。请予以解释:___________ 。
 和
和 两种化合物。请完成下列空白:
两种化合物。请完成下列空白:(1)
 内的O—H、水分子间的范德华力和氢键,从强到弱依次为
内的O—H、水分子间的范德华力和氢键,从强到弱依次为 可与
可与 形成
形成 ,
, 中O采用
中O采用 中
中 键角比
键角比 中的
中的(2)
 是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。
是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。 的电子式是
的电子式是 是含有
是含有 能与水混溶,却不溶于
能与水混溶,却不溶于 。请予以解释:
。请予以解释:
更新时间:2021-12-03 09:25:19
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)用电子式表示H2O和MgBr2的形成过程:
H2O_________
MgBr2__________
(2)写出CO2、Na2O2、H2O2的电子式:
CO2___________ Na2O2________ H2O2________
(3)A+、B+、C-、D、E 5种离子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:
A.A++ C- → D + E b.B++ C- → 2D 。据此回答下列问题:
①写出A反应的离子方程式________ ;
②写出A+、C-离子的电子式:A+________ C-__________ 。
H2O
MgBr2
(2)写出CO2、Na2O2、H2O2的电子式:
CO2
(3)A+、B+、C-、D、E 5种离子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:
A.A++ C- → D + E b.B++ C- → 2D 。据此回答下列问题:
①写出A反应的离子方程式
②写出A+、C-离子的电子式:A+
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请回答下列问题:
(1)①磁性氧化铁的化学式是___________ ;② 的电子式是
的电子式是___________ 。
(2) 分子的空间结构为
分子的空间结构为___________ 。
(3)除去 粉末中混有的少量
粉末中混有的少量 ,所涉及的反应的化学方程式为
,所涉及的反应的化学方程式为___________ 。
(1)①磁性氧化铁的化学式是
 的电子式是
的电子式是(2)
 分子的空间结构为
分子的空间结构为(3)除去
 粉末中混有的少量
粉末中混有的少量 ,所涉及的反应的化学方程式为
,所涉及的反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工业上用焦炭与石英在高温下氮气流中发生如下反应,3SiO2(s)+6C(s)+2N2(g)⇌Si3N4(s)+6CO(g) +Q(Q>0),可制得一种新型陶瓷材料氮化硅(Si3N4),该材料熔点高,硬度大 ,广泛应用于光伏、轴承、冶金、化工、能源、环保等行业。回答下列问题:
(1)N2的电子式为____________ ,Si在元素周期表中的位置是_______________ ,氮化硅晶体属于__________ 晶体。
(2)该反应中,还原产物是______________ 。若测得反应生成22.4 L CO气体(标准状况下),则转移的电子的物质的量为_____________ 。
(3)该反应的平衡常数表达式K=__________________ ;若其他条件不变,降低温度,达到新的平衡时,K值____________ (填“增大”、“减小”或“不变”,以下同)。CO的浓度_________ ,SiO2的质量______________ 。
(4)已知在一定条件下的2L密闭容器中制备氮化硅,SiO2(纯度98.5%,所含杂质不与参与反应)剩余质量和反应时间的关系如右图所示。CO在0~10min的平均反应速率为_______ 。

(5)现用四氯化硅、氮气和氢气在高温下发生反应,可得较高纯度的氮化硅。反应的化学方程式为______________ 。
(1)N2的电子式为
(2)该反应中,还原产物是
(3)该反应的平衡常数表达式K=
(4)已知在一定条件下的2L密闭容器中制备氮化硅,SiO2(纯度98.5%,所含杂质不与参与反应)剩余质量和反应时间的关系如右图所示。CO在0~10min的平均反应速率为

(5)现用四氯化硅、氮气和氢气在高温下发生反应,可得较高纯度的氮化硅。反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】黄铜矿(主要成分是CuFeS2)是一种重要的化工原料,通过化学工艺可获得二氨基丙酸合铜[Cu(NH2CH2CH2COO)2]等产品。
(1)Cu2+基态核外电子排布式为_____ 。
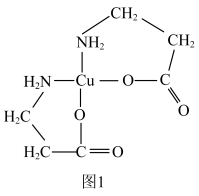
(2)[Cu(NH2CH2CH2COO)2]的结构简式如图1所示。1mol[Cu(NH2CH2CH2COO)2]中含σ键的数目为_____ 。
(3)黄铜矿在空气中灼烧得到废气和固体混合物。废气中SO2经催化氧化生成SO3,SO2分子中S原子轨道的杂化类型为_____ ,SO3分子的空间构型为_____ ;固体混合物中含有一种化合物X,其晶胞如图2所示,化合物X的化学式为_____ 。

(1)Cu2+基态核外电子排布式为
(2)[Cu(NH2CH2CH2COO)2]的结构简式如图1所示。1mol[Cu(NH2CH2CH2COO)2]中含σ键的数目为

(3)黄铜矿在空气中灼烧得到废气和固体混合物。废气中SO2经催化氧化生成SO3,SO2分子中S原子轨道的杂化类型为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知N—N、N=N和N≡N键能之比为1.00∶2.17∶4.90,而C—C、C=C和C≡C键能之比为1.00∶1.77∶2.34,下列说法正确的是___________ 。
A.σ键一定比π键稳定
B.N2较易发生加成反应
C.乙烯、乙炔较易发生加成反应
D.乙烯、乙炔中的π键比σ键稳定
E.σ键可以旋转,π键不能旋转
A.σ键一定比π键稳定
B.N2较易发生加成反应
C.乙烯、乙炔较易发生加成反应
D.乙烯、乙炔中的π键比σ键稳定
E.σ键可以旋转,π键不能旋转
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在H2O、NH3、CS2、CH4、BF3分子中:
(1)存在π键的共价化合物分子是_______ (填分子式,下同)。
(2)具有直线形结构的分子是_______ 。
(3)具有正四面体形结构的分子是_______ 。
(4)具有三角锥形结构的分子是_______ 。
(5)具有sp2杂化轨道类型的分子是_______ 。
(6)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ 。OF2分子的空间构型为_______ 。
(1)存在π键的共价化合物分子是
(2)具有直线形结构的分子是
(3)具有正四面体形结构的分子是
(4)具有三角锥形结构的分子是
(5)具有sp2杂化轨道类型的分子是
(6)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】20世纪初,科学家们才发现原子其实具有复杂的内部结构。而丰富的原子种类也造就了自然界中丰富的物质。
(1)下列化学用语表达正确的是___________(单选)。
(2)硫的化合物很多,如 、
、 、
、 、
、 等,其中三聚的
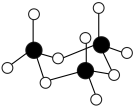
等,其中三聚的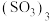 的结构如图所示(白球为O,黑球为S,黑线表示单键)。下列说法正确的是___________。
的结构如图所示(白球为O,黑球为S,黑线表示单键)。下列说法正确的是___________。
(3)乙炔分子中 键和
键和 键数目之比为
键数目之比为___________ 。
(4)下列说法正确的是___________(不定项)。
(5) 、
、 、
、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为___________ 。
(6)与 元素同主族的基态
元素同主族的基态 原子的最外层电子排布式为
原子的最外层电子排布式为___________ 。
(1)下列化学用语表达正确的是___________(单选)。
A. 的球棍模型为 的球棍模型为 |
B.乙烯分子中形成 键所用的轨道如右图所示 键所用的轨道如右图所示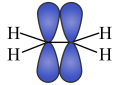 |
C.基态 的简化电子排布式为 的简化电子排布式为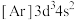 |
D.氯离子的结构示意图为 |
(2)硫的化合物很多,如
 、
、 、
、 、
、 等,其中三聚的
等,其中三聚的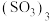 的结构如图所示(白球为O,黑球为S,黑线表示单键)。下列说法正确的是___________。
的结构如图所示(白球为O,黑球为S,黑线表示单键)。下列说法正确的是___________。
A.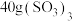 分子中含有2.5mol 分子中含有2.5mol 键 键 |
B. 中中心原子S的杂化方式是 中中心原子S的杂化方式是 |
C. 、 、 分子的VSEPR模型不一样 分子的VSEPR模型不一样 |
D. 和 和 的电负性大小比较: 的电负性大小比较: |
(3)乙炔分子中
 键和
键和 键数目之比为
键数目之比为(4)下列说法正确的是___________(不定项)。
A. 中的键角大于 中的键角大于 中的键角 中的键角 |
B. 、 、 、 、 、 、 的第一电离能逐渐减小 的第一电离能逐渐减小 |
C.N原子的最外层电子轨道表示式如图 |
D. 的球棍模型如图 的球棍模型如图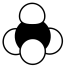 |
(5)
 、
、 、
、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为(6)与
 元素同主族的基态
元素同主族的基态 原子的最外层电子排布式为
原子的最外层电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】我国“奋斗者”号潜水器载人舱球壳“钛”厉害,球壳材料 是一种Ti和Al、
是一种Ti和Al、 、Si等形成的合金。回答下列问题:
、Si等形成的合金。回答下列问题:
(1)钛元素位于元素周期表的_______ 区,其基态原子核外有_______ 种运动状态不同的电子,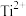 的电子排布式为
的电子排布式为_______ 。
(2)已知钛和铝的相对原子半径分别是1.45和1.43,钛的硬度比铝大的原因是_______ 。
(3)TiCl4可以与胺形成配合物,如[TiCl4(CH3NH2)2]、[TiCl4(H2NCH2CH2NH2)]等。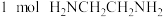 中含有的
中含有的 键物质的量为
键物质的量为_______ 。
(4)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为_______ ,阳离子中O的杂化方式为_______ ,阴离子的空间构型为_______ 。

 是一种Ti和Al、
是一种Ti和Al、 、Si等形成的合金。回答下列问题:
、Si等形成的合金。回答下列问题:(1)钛元素位于元素周期表的
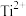 的电子排布式为
的电子排布式为(2)已知钛和铝的相对原子半径分别是1.45和1.43,钛的硬度比铝大的原因是
(3)TiCl4可以与胺形成配合物,如[TiCl4(CH3NH2)2]、[TiCl4(H2NCH2CH2NH2)]等。
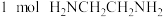 中含有的
中含有的 键物质的量为
键物质的量为(4)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知H元素和O元素可以形成 和
和 两种化合物,试根据有关信息回答下列问题。
两种化合物,试根据有关信息回答下列问题。
(1)水是维持生命活动所必需的一种物质,用球棍模型表示的水分子结构是_______ (填序号)。

(2)已知 分子的结构如图所示,
分子的结构如图所示, 分子结构不是直线形,两个氢原子犹如在半展开的书的两个面上,两个氧原子在书脊位置上,书页夹角为
分子结构不是直线形,两个氢原子犹如在半展开的书的两个面上,两个氧原子在书脊位置上,书页夹角为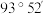 ,而两个
,而两个 键与
键与 键的夹角均为
键的夹角均为 。
。

试回答下列问题:
① 分子结构式为
分子结构式为_______ 。
② 分子是含有
分子是含有_______ 键和_______ 键的_______ 分子(填“极性”或“非极性”)。
 和
和 两种化合物,试根据有关信息回答下列问题。
两种化合物,试根据有关信息回答下列问题。(1)水是维持生命活动所必需的一种物质,用球棍模型表示的水分子结构是

(2)已知
 分子的结构如图所示,
分子的结构如图所示, 分子结构不是直线形,两个氢原子犹如在半展开的书的两个面上,两个氧原子在书脊位置上,书页夹角为
分子结构不是直线形,两个氢原子犹如在半展开的书的两个面上,两个氧原子在书脊位置上,书页夹角为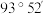 ,而两个
,而两个 键与
键与 键的夹角均为
键的夹角均为 。
。
试回答下列问题:
①
 分子结构式为
分子结构式为②
 分子是含有
分子是含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在HF、H2S、NH3、CO2、CCl4、N2、C60、SO2分子中:
(1)以非极性键结合的非极性分子是___________
(2)以极性键相结合,具有直线型结构的非极性分子是___________
(3)以极性键相结合,具有正四面体结构的非极性分子是___________
(4)以极性键相结合,具有三角锥型结构的极性分子是___________
(5)以极性键相结合,具有V型结构的极性分子是___________
(6)以极性键相结合,而且分子极性最大的是___________
(1)以非极性键结合的非极性分子是
(2)以极性键相结合,具有直线型结构的非极性分子是
(3)以极性键相结合,具有正四面体结构的非极性分子是
(4)以极性键相结合,具有三角锥型结构的极性分子是
(5)以极性键相结合,具有V型结构的极性分子是
(6)以极性键相结合,而且分子极性最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知:A、B、C、D是四种短周期非金属元素,它们的原子序数依次增大,A元素的原子形成的阳离子就是一个质子,B原子的最外层上s电子数等于p电子数,B、C、D在元素周期表中处于相邻的位置,C、D的单质在常温下均为无色气体。试回答:
(1)写出C的原子结构示意图____________ ,D原子的电子排布式_______ 。
有同学将B原子最外层电子排布的轨道表示式写成: ,你认为
,你认为_______ (填“正确”或“不正确”),若不正确,请写出正确的轨道表示式__________
(2)A、B两种元素组成的化合物很多,其中只含有一种类型共价键的化合物名称为_______ 。BD2是_______ 分子(填“极性”或“非极性”)。
(3)A单质和C单质在一定条件下反应生成化合物E,E分子的空间结构为_________ ,电子式为_______________ 。
(1)写出C的原子结构示意图
有同学将B原子最外层电子排布的轨道表示式写成:
 ,你认为
,你认为(2)A、B两种元素组成的化合物很多,其中只含有一种类型共价键的化合物名称为
(3)A单质和C单质在一定条件下反应生成化合物E,E分子的空间结构为
您最近一年使用:0次

 的键角大于
的键角大于 的键角,解释其原因:
的键角,解释其原因: 中含有的化学键类型包括
中含有的化学键类型包括 中
中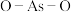 键角
键角 中
中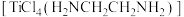 与游离的
与游离的 分子相比,其
分子相比,其 键角
键角

