回答下列问题:
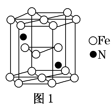
(1)氮化铁晶体的晶胞结构如图1所示。该晶体中Fe、N的个数之比为__ 。
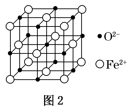
(2)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为__ ;Fe2+与O2-的最短核间距为__ pm。
(1)氮化铁晶体的晶胞结构如图1所示。该晶体中Fe、N的个数之比为

(2)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为

2021高三·全国·专题练习 查看更多[1]
(已下线)专题讲座(十一)晶胞参数、坐标参数的分析与应用(练) — 2022年高考化学一轮复习讲练测(新教材新高考)
更新时间:2021-12-05 12:44:17
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】按要求回答下列问题:
(1)在周期表中,与Li的化学性质最相似的邻族元素是_______ ,该元素基态原子核外M层电子的自旋状态_______ (填“相同”或“相反”)。
(2)符号“3px”没有给出的信息是_______
(3)某元素基态原子4s轨道上有1个电子,则该元素基态原子价电子排布不可能是_______
(4)X元素的原子最外层电子排布式为(n+1)sn(n+1)pn+1,则X的氢化物的化学式是_______
(5)下列比较正确的是_______
(6)下列实验事实不能用氢键来解释的是_______
(7)用电子式表示MgCl2的形成过程_______ 。
(8)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有_______ 种。
(9)下列图象是NaCl、CsCl、ZnS等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于NaCl的晶体结构的图是 。
(10)键能的大小可以衡量化学键的强弱。下列说法中错误的是_______
(1)在周期表中,与Li的化学性质最相似的邻族元素是
(2)符号“3px”没有给出的信息是_______
| A.能层 | B.能级 | C.电子云在空间的伸展方向 | D.电子的自旋方向 |
| A.4s1 | B.3p64s1 | C.3d54s1 | D.3d104s1 |
| A.HX | B.H2X | C.XH3 | D.XH4 |
| A.酸性:H3PO4<H3AsO4 | B.熔点:MgO>CaO |
| C.离子半径:r(Al3+)>r(O2−) | D.键角:H2O>NH3 |
| A.CH4比SiH4稳定 |
| B.乙醇能与水以任意比互溶 |
| C.邻羟基苯甲醛的沸点低于对羟基苯甲醛 |
| D.接近沸点的水蒸气的相对分子质量测量值大于18 |
(8)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有
(9)下列图象是NaCl、CsCl、ZnS等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于NaCl的晶体结构的图是 。
A.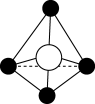 | B.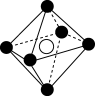 | C.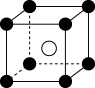 | D.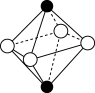 |
| 化学键 | Si−O | Si−Cl | H−H | H−Cl | Si−Si | Si−C |
| 键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
| A.SiCl4的熔点比SiC熔点低 |
| B.HCl的稳定性比HI稳定性高 |
| C.C−C的键能大于Si−Si |
| D.拆开1mol晶体硅中的化学键所吸收的能量为176kJ |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】铝广泛应用于航空、建筑、汽车等行业,目前工业上采用电解氧化铝和冰晶石混合物的方法制取铝。回答下列问题:
(1)某同学写出了铝原子的4种不同状态的电子排布图:
A.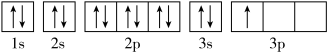
B.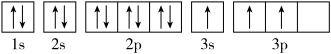
C.
D.
其中能量最低的是____ (填字母),电子由状态C到状态B所得原子光谱为____ 光谱(填“发射”或“吸收”) ,状态D是铝的某种激发态,但该电子排布图有错误,主要是不符合_____ 。
(2)熔融态氯化铝可挥发出二聚分子Al2Cl6,其结构如图所示。
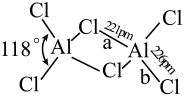
①a键的键能_____ b键的键能(填“>”“<”或“=”),其理由是_______ 。
②Al2Cl6中铝原子的杂化方式为___ ;AlCl3的空间结构为______ 。
(3)冰晶石属于离子化合物,由Na+和AlF63−组成,在冰晶石的晶胞中,AlF63−占据的位置相当于氯化钠晶胞中Cl−的位置。
①冰晶石的化学式为_____ ,一个冰晶石晶胞中Na+的个数为_____ 。
②已知冰晶石的密度为2.95 g/cm3,则冰晶石晶胞的边长a=____ pm(列出算式即可,阿伏伽德罗常数值为6.02×1023)。
(1)某同学写出了铝原子的4种不同状态的电子排布图:
A.

B.

C.

D.

其中能量最低的是
(2)熔融态氯化铝可挥发出二聚分子Al2Cl6,其结构如图所示。

①a键的键能
②Al2Cl6中铝原子的杂化方式为
(3)冰晶石属于离子化合物,由Na+和AlF63−组成,在冰晶石的晶胞中,AlF63−占据的位置相当于氯化钠晶胞中Cl−的位置。
①冰晶石的化学式为
②已知冰晶石的密度为2.95 g/cm3,则冰晶石晶胞的边长a=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】m、n、x、y四种主族元素在周期表里的相对位置如下图所示。已知它们的原子序数总和为46,则:
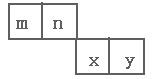
(1)写出n元素基态原子电子排布图:________________________ 。
(2)元素x气态氢化物的分子式为___________ ,空间构型为____________ 。
(3)m与y所形成的化合物含______________ 键,属_____________ 分子。(填“极性”或“非极性”)
(4)x位于周期表的第_____ 周期,第_____ 族;其原子结构示意图为____________ 。
(5)由n、y的氢化物相互作用所生成的物质的电子式为______________________ ,此物质属于_______________ 化合物。(填“离子”或“共价”)

(1)写出n元素基态原子电子排布图:
(2)元素x气态氢化物的分子式为
(3)m与y所形成的化合物含
(4)x位于周期表的第
(5)由n、y的氢化物相互作用所生成的物质的电子式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】汞钡铜氧晶体的晶胞如图A所示,通过掺杂Ca2+获得的具有更高临界温度的超导材料如图B所示。图A晶胞中钡离子的分数坐标为( ,
, ,
,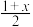 )和
)和________
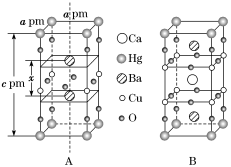
 ,
, ,
,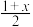 )和
)和
您最近一年使用:0次
【推荐2】I.碳元素的单质有多种形式,下图依次是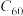 、石墨和金刚石的结构图:
、石墨和金刚石的结构图:
(1)C60属于___________ 晶体,石墨属于___________ 晶体。
(2)在金刚石晶体中,碳原子数与化学键数之比为___________ 。
(3)石墨晶体中,层内C—C键的键长为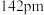 ,而金刚石中C—C键的键长为
,而金刚石中C—C键的键长为 。推测金刚石的熔点
。推测金刚石的熔点___________  填“
填“ ”“
”“ ”或“
”或“ ”
” 石墨的熔点。
石墨的熔点。
Ⅱ.回答下列问题
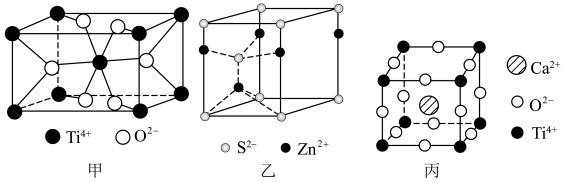
(4)如图甲所示的是金红石的晶胞,则每个晶胞拥有___________ 个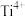 、
、___________ 个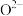 。
。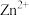 、
、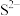 的数目之比是
的数目之比是___________ 。
(6)如图丙所示的是钙钛矿的晶胞,则其化学式是___________ 。
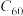 、石墨和金刚石的结构图:
、石墨和金刚石的结构图: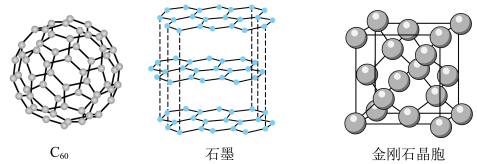
(1)C60属于
(2)在金刚石晶体中,碳原子数与化学键数之比为
(3)石墨晶体中,层内C—C键的键长为
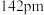 ,而金刚石中C—C键的键长为
,而金刚石中C—C键的键长为 。推测金刚石的熔点
。推测金刚石的熔点 填“
填“ ”“
”“ ”或“
”或“ ”
” 石墨的熔点。
石墨的熔点。Ⅱ.回答下列问题
(4)如图甲所示的是金红石的晶胞,则每个晶胞拥有
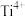 、
、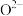 。
。
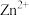 、
、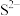 的数目之比是
的数目之比是(6)如图丙所示的是钙钛矿的晶胞,则其化学式是
您最近一年使用:0次
【推荐3】为降低成本,某些复合型物质也常用作催化剂。某复合型物质的晶胞结构如图所示。
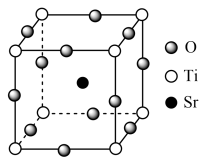
(1)该复合型物质的化学式为___________ 。每个Ti原子周围距离最近的O原子的个数为___________ 。
(2)Ti的四卤化物熔点如下表所示。
TiF4熔点高于其他三种卤化物,而自TiCl4至TiI4熔点依次升高,原因是___________ 。

(1)该复合型物质的化学式为
(2)Ti的四卤化物熔点如下表所示。
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据如表所示:
(1)Mn元素原子的电子排布式为___________ 。比较两元素的I2、I3可知:气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是___________ 。
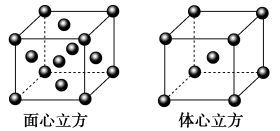
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是___________ 。
(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为___________ 。
| 元素 | Mn | Fe | |
| 电离能(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是
(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】汞钡铜氧晶体的晶胞如图A所示,通过掺杂Ca2+获得的具有更高临界温度的超导材料如图B所示。图A晶胞中钡离子的分数坐标为( ,
, ,
,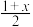 )和
)和________

 ,
, ,
,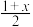 )和
)和
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】已知:离子晶体中与一个离子紧邻的异电性离子的数目称为配位数。
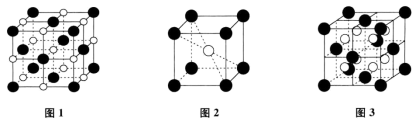
(1)图1是NaCl晶体的晶胞, 表示
表示 表示
表示 。该晶胞中实际含有的
。该晶胞中实际含有的 数为
数为_______ , 的配位数是
的配位数是_______ 。
(2)图2是CsCl晶体的晶胞, 表示
表示 表示
表示 。该晶胞中实际含有的
。该晶胞中实际含有的 数为
数为_______ , 的配位数是
的配位数是_______ 。
(3)图3是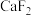 的晶胞,
的晶胞, 位于顶角和面心,
位于顶角和面心, 位于大立方体对角线
位于大立方体对角线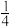 处。
处。 表示的离子是
表示的离子是_______ ,它的配位数是_______ ; 表示的离子是
表示的离子是_______ ,它的配位数是_______ 。

(1)图1是NaCl晶体的晶胞,
 表示
表示 表示
表示 。该晶胞中实际含有的
。该晶胞中实际含有的 数为
数为 的配位数是
的配位数是(2)图2是CsCl晶体的晶胞,
 表示
表示 表示
表示 。该晶胞中实际含有的
。该晶胞中实际含有的 数为
数为 的配位数是
的配位数是(3)图3是
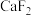 的晶胞,
的晶胞, 位于顶角和面心,
位于顶角和面心, 位于大立方体对角线
位于大立方体对角线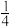 处。
处。 表示的离子是
表示的离子是 表示的离子是
表示的离子是
您最近一年使用:0次



