室温下,取50mL H+浓度为0.20 mol/L的盐酸和硫酸的混合溶液,加入50mL Ba(OH)2溶液充分反应,得到沉淀0.233g,反应后溶液的pH值为12(假设反应后溶液的总体积为100mL)。请计算:
(1)原混合酸溶液中H+的物质的量为___________ mol。
(2)原混合酸溶液中HCl的物质的量浓度为___________ mol/L。
(3)加入的Ba(OH)2溶液的物质的量浓度为___________ mol/L。
(1)原混合酸溶液中H+的物质的量为
(2)原混合酸溶液中HCl的物质的量浓度为
(3)加入的Ba(OH)2溶液的物质的量浓度为
更新时间:2021-11-05 09:08:31
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】有Na2SO4和Na2CO3混合溶液10.0mL,加入足量BaCl2溶液,充分反应后,经过滤、洗涤、烘干,得到白色沉淀1.45g,将沉淀与过量的盐酸反应,得到112mLCO2气体(标况)。求原混合溶液中Na2SO4物质的量浓度为_________________ 、Na2CO3的物质的量浓度为_______________ ?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】填空
(1)从1L 溶液中取出100mL,向其中加入200mL
溶液中取出100mL,向其中加入200mL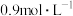 的
的 溶液恰好使
溶液恰好使 完全沉淀,则原溶液中
完全沉淀,则原溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是_______ 。
(3)标况下,1体积水中溶解了V体积HCl气体,所得溶液的密度为 ,所得溶液的物质的量浓度为
,所得溶液的物质的量浓度为_______ 。
(1)从1L
 溶液中取出100mL,向其中加入200mL
溶液中取出100mL,向其中加入200mL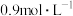 的
的 溶液恰好使
溶液恰好使 完全沉淀,则原溶液中
完全沉淀,则原溶液中 的物质的量浓度为
的物质的量浓度为(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是
(3)标况下,1体积水中溶解了V体积HCl气体,所得溶液的密度为
 ,所得溶液的物质的量浓度为
,所得溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】完成下列填空:
(1)某市售的浓氨水, 的质量分数为
的质量分数为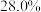 ,密度为
,密度为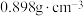 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为___________ 。
(2)已知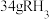 气体中含有
气体中含有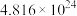 个原子,则该气体的摩尔质量为
个原子,则该气体的摩尔质量为___________ 。
(3)质量为___________  的
的 所含的电子的物质的量为
所含的电子的物质的量为 。
。
(4)质量比为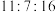 的
的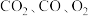 ,其物质的量之比为
,其物质的量之比为___________ 。
(5)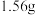 某金属与足量盐酸完全反应,生成
某金属与足量盐酸完全反应,生成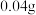 氢气,生成氯化物中金属显
氢气,生成氯化物中金属显 价,则该金属的摩尔质量为
价,则该金属的摩尔质量为___________ 。(写出计算过程)
(1)某市售的浓氨水,
 的质量分数为
的质量分数为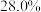 ,密度为
,密度为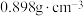 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为(2)已知
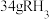 气体中含有
气体中含有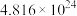 个原子,则该气体的摩尔质量为
个原子,则该气体的摩尔质量为(3)质量为
 的
的 所含的电子的物质的量为
所含的电子的物质的量为 。
。(4)质量比为
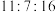 的
的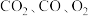 ,其物质的量之比为
,其物质的量之比为(5)
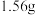 某金属与足量盐酸完全反应,生成
某金属与足量盐酸完全反应,生成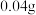 氢气,生成氯化物中金属显
氢气,生成氯化物中金属显 价,则该金属的摩尔质量为
价,则该金属的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】甲、乙、丙、丁四位同学用锌与稀硫酸反应,所得相关数据记录如下(实验中的误差忽略不计)。
计算:
(1)甲同学加入金属锌的质量x___ ;
(2)稀硫酸中溶质的质量分数___ 。
| 甲 | 乙 | 丙 | 丁 | |
| 取用稀硫酸质量/克 | 100 | 100 | 100 | 200 |
| 加入金属的质量/克 | x | 1.25x | 2x | 2x |
| 生成氢气的质量/克 | 0.4 | 0.5 | 0.6 | 0.8 |
计算:
(1)甲同学加入金属锌的质量x
(2)稀硫酸中溶质的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某温度下的溶液中c (H+)=1.0×10xmol/L,c (OH-)=1.0×10ymol/L。x与y的关系如图所示:

(1)求该温度下,中性溶液的pH___ ;
(2)求该温度下0.01mol/LNaOH溶液的pH___ ;
(3)该温度下,pH=a的醋酸溶液与pH=b的NaOH溶液等体积混合,恰好完全反应,求此醋酸溶液中醋酸的电离度____ 。

(1)求该温度下,中性溶液的pH
(2)求该温度下0.01mol/LNaOH溶液的pH
(3)该温度下,pH=a的醋酸溶液与pH=b的NaOH溶液等体积混合,恰好完全反应,求此醋酸溶液中醋酸的电离度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某温度(t°C)时,测得0.01mol·L-1的NaOH溶液的pH为11,则该温度下水的Kw=_______ ;在此温度下,将pH=a的H2SO4溶液VaL与pH=b的NaOH溶液VbL混合.
(1)若所得混合液为中性,且a=2,b=12,则Va∶Vb=_______ ;
(2)若所得混合液的pH=10,且a=2,b=12,则Va∶Vb=_______ 。
(1)若所得混合液为中性,且a=2,b=12,则Va∶Vb=
(2)若所得混合液的pH=10,且a=2,b=12,则Va∶Vb=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)常温下,0.05 mol/L Ba(OH)2溶液中c(OH-)= _____ ,pH=______ 。
(2)某温度下,纯水中的c(H+)= 2×10-7mol/L,则此时溶液中的c(OH-)=____ ;若温度不变,滴入稀盐酸,使c(H+)= 5×10-4 mol/L,则溶液中c(OH-)=____ ,此时溶液中由水电离产生的c(H+)= _____ 。
(3)已知:lg2=0.3,lg3=0.5,lg5=0.7。常温时,将pH为5的HCl溶液与pH为2的H2SO4溶液等体积混合,混合后溶液的pH约为___________ 。
(4)常温下,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈______ (填“酸性”,“中性”或“碱性”)。
(5)25℃时,已知 HF 的电离常数为3.6×10-4,H3PO4的电离常数K1 =7.5×10-3,K2=6.2×10-8,K3 =4.4×10-13。则足量NaF溶液和H3PO4溶液反应的离子方程式为_______________________________ 。
(2)某温度下,纯水中的c(H+)= 2×10-7mol/L,则此时溶液中的c(OH-)=
(3)已知:lg2=0.3,lg3=0.5,lg5=0.7。常温时,将pH为5的HCl溶液与pH为2的H2SO4溶液等体积混合,混合后溶液的pH约为
(4)常温下,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
(5)25℃时,已知 HF 的电离常数为3.6×10-4,H3PO4的电离常数K1 =7.5×10-3,K2=6.2×10-8,K3 =4.4×10-13。则足量NaF溶液和H3PO4溶液反应的离子方程式为
您最近一年使用:0次



