下列表示对应化学反应的离子方程式正确的是
| A.用石墨电极电解饱和食盐水:2Cl-+2H2O=2OH-+H2↑+Cl2↑ |
B.向稀NaHCO3中加入过量Ca(OH)2溶液:2 +Ca2++2OH-=CaCO 3↓+2H2O+ +Ca2++2OH-=CaCO 3↓+2H2O+ |
C.用Na2CO3溶液预处理水垢中的CaSO4: +CaSO4=CaCO3+ +CaSO4=CaCO3+ |
D.向稀HNO3中滴加Na2SO3溶液: +2H+=SO2↑+H2O +2H+=SO2↑+H2O |
21-22高三上·北京西城·期中 查看更多[3]
(已下线)卷03 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)第四单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)北京师范大学附属中学2021-2022学年高三上学期期中考试化学试题
更新时间:2021-11-13 11:09:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式中,正确的是( )
| A.铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B.氯气与氯化亚铁溶液反应:2FeCl2+Cl2=2FeCl3 |
| C.氯化铁溶液与铁反应:Fe3++Fe=2Fe2+ |
| D.氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH- = Fe(OH)3↓ |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列指定反应的离子方程式正确的是
A.向Ba(OH) 2溶液中加入过量NH4HSO4溶液:Ba2++2OH- + +H++ +H++ =BaSO4↓+NH3·H2O+H2O =BaSO4↓+NH3·H2O+H2O |
B.向PbS固体中滴加硫酸铜溶液:Cu2++ +PbS=CuS+PbSO4 +PbS=CuS+PbSO4 |
| C.将Fe(OH)3固体溶于氢碘酸:Fe (OH) 3+3H+=Fe3+ +3H2O |
D.过量CO2通入饱和碳酸钠溶液: 2Na++ +CO2+H2O=2 +CO2+H2O=2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列过程中的化学反应,相应的离子方程式正确的是
A.将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:Ba2++2OH-+2H++SO =BaSO4↓+2H2O =BaSO4↓+2H2O |
B.过量铁粉加入稀硝酸中:Fe+4H++NO =Fe3++NO↑ +2H2O =Fe3++NO↑ +2H2O |
C.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-=AlO +2H2O +2H2O |
| D.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子方程式书写正确的是
A. 溶液中通入过量 溶液中通入过量 : :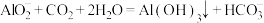 |
B.向 溶液中通入 溶液中通入 : :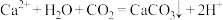 |
C.向NaClO溶液中通入少量 : :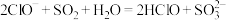 |
D.氧化亚铁溶于稀硝酸: |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加德罗常数的值。下列说法正确的是
A.0.02g H与0.03g H与0.03g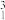 H合成 H合成 He时释放 He时释放 的数目为0.1NA 的数目为0.1NA |
B.1mol甲基碳正离子(CH )所含质子总数为8NA )所含质子总数为8NA |
| C.加热条件下,56gFe与足量浓硝酸充分反应,转移的电子数为3NA |
| D.在一定条件下,2molSO2和1molO2充分反应后,容器中的分子总数小于2NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】从下列实验事实所得出的相应结论正确的是
| 选项 | 实验事实 | 结论 |
| A | Na2S2O3溶液与稀硫酸反应,其他条件相同时,Na2S2O3溶液浓度越大,析出硫沉淀所需时间越短 | 当其他条件不变时,增大反应物浓度,化学反应速率加快 |
| B | 向0.1mol·L−1的HCOOH中加水稀释,溶液pH增大 | HCOOH是弱酸 |
| C | 向盛有2mL浓度为0.1mol·L−1的AgNO3溶液中滴加2滴0.1mol·L−1NaCl溶液,然后再滴加4滴0.1mol·L−1NaI溶液,白色沉淀转化为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 向NaAlO2溶液中滴加NaHCO3溶液,产生白色沉淀 |  和 和 发生了双水解 发生了双水解 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验中,由实验现象得到的结论正确的是
| 实验操作 | 现象 | 结论 | |
| A | 大小相同的铝片分别加入同温同体积且 都为 都为 的盐酸、硫酸中 的盐酸、硫酸中 | 铝与盐酸反应产生气泡速率较快 | 可能是 对该反应起到促进作用 对该反应起到促进作用 |
| B | 往 溶液中滴加 溶液中滴加 溶液,再加入少量 溶液,再加入少量 固体 固体 | 溶液先变成红色,后无明显变化 |  与 与 的反应不可逆 的反应不可逆 |
| C | 室温下,用pH试纸测浓度均为 的 的 和 和 溶液的pH 溶液的pH |  溶液的pH约为9, 溶液的pH约为9, 溶液的pH约为3 溶液的pH约为3 |  结合 结合 的能力比 的能力比 的强 的强 |
| D | 向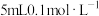 的 的 溶液中先滴加5滴 溶液中先滴加5滴 溶液,再滴加5滴 溶液,再滴加5滴 溶液 溶液 | 先产生白色沉淀,后白色沉淀变为黄色沉淀 |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
【推荐3】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色 | X溶液中一定含有Fe2+ |
| B | 向含酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向含有ZnS和Na2S的悬浊液中滴加CuSO4溶液,生成黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| D | 用pH试纸测得:Na2CO3溶液的pH约为9,NaNO2溶液的pH约为8 | HNO2电离出H+的能力比H2CO3的强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述中,正确的是( )
①电解池是将化学能转变成电能的装置 ②原电池是将电能转变成化学能的装置 ③金属和石墨导电均为物理变化,电解质溶液导电是化学变化 ④不能自发进行的氧化还原反应,通过电解的原理有可能实现 ⑤Cu+2Ag+===Cu2++2Ag,反应既可以在原电池中实现,也可以在电解池中实现,其他条件相同时,二种装置中反应速率相同
①电解池是将化学能转变成电能的装置 ②原电池是将电能转变成化学能的装置 ③金属和石墨导电均为物理变化,电解质溶液导电是化学变化 ④不能自发进行的氧化还原反应,通过电解的原理有可能实现 ⑤Cu+2Ag+===Cu2++2Ag,反应既可以在原电池中实现,也可以在电解池中实现,其他条件相同时,二种装置中反应速率相同
| A.①②③④ | B.③④ | C.③④⑤ | D.④ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】磷氰酸根负离子对构建新型含磷化合物的研究有着重要的意义。以惰性材料为电极,将白磷转化为二氰基磷负离子的锂盐,工作原理如图所示。下列说法错误的是
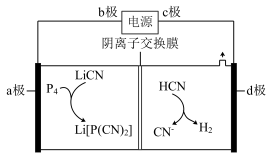
| A.Li[P(CN)2]中 P元素的化合价为+1 |
| B.装置工作时,b极电势高于c极电势 |
| C.阴极反应为2HCN+2e- =2CN- +H2↑ |
| D.外电路中通过0.2 mol电子时,阴极室质量减少0.2g |
您最近半年使用:0次

 ===Cu2++2NO2↑+2H2O
===Cu2++2NO2↑+2H2O


