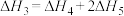选择性催化还原法( )烟气脱硝技术是一种成熟的
)烟气脱硝技术是一种成熟的 控制处理方法,主要反应如下:
控制处理方法,主要反应如下:
①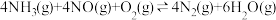 △H1=a kJ·mol-1
△H1=a kJ·mol-1
②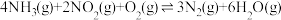 △H2=b kJ·mol-1
△H2=b kJ·mol-1
副反应③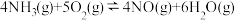 △H3=d kJ·mol-1
△H3=d kJ·mol-1
可以计算出反应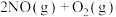

 的△H为
的△H为
 )烟气脱硝技术是一种成熟的
)烟气脱硝技术是一种成熟的 控制处理方法,主要反应如下:
控制处理方法,主要反应如下:①
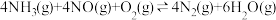 △H1=a kJ·mol-1
△H1=a kJ·mol-1②
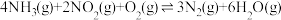 △H2=b kJ·mol-1
△H2=b kJ·mol-1副反应③
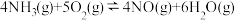 △H3=d kJ·mol-1
△H3=d kJ·mol-1可以计算出反应
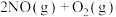

 的△H为
的△H为A.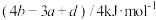 | B.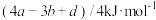 |
C.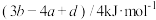 | D.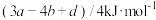 |
2018·新疆·一模 查看更多[8]
更新时间:2021-11-10 15:49:33
|
相似题推荐
单选题
|
容易
(0.94)
【推荐2】一定条件下,废水中的NO 可被氧化为NO
可被氧化为NO 。已知反应2NO
。已知反应2NO (aq)+O2(g)=2NO
(aq)+O2(g)=2NO (aq) ΔH1=-146.0kJ·mol-1,NO
(aq) ΔH1=-146.0kJ·mol-1,NO (aq)+O2(g)=NO
(aq)+O2(g)=NO (aq)+O(g) ΔH2=xkJ·mol-1,O=O键断裂需要的能量为499.0kJ·mol-1。则x的值为
(aq)+O(g) ΔH2=xkJ·mol-1,O=O键断裂需要的能量为499.0kJ·mol-1。则x的值为
 可被氧化为NO
可被氧化为NO 。已知反应2NO
。已知反应2NO (aq)+O2(g)=2NO
(aq)+O2(g)=2NO (aq) ΔH1=-146.0kJ·mol-1,NO
(aq) ΔH1=-146.0kJ·mol-1,NO (aq)+O2(g)=NO
(aq)+O2(g)=NO (aq)+O(g) ΔH2=xkJ·mol-1,O=O键断裂需要的能量为499.0kJ·mol-1。则x的值为
(aq)+O(g) ΔH2=xkJ·mol-1,O=O键断裂需要的能量为499.0kJ·mol-1。则x的值为| A.+176.5 | B.-176.5 | C.+322.5 | D.-322.5 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】在25℃、101kPa条件下,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5kJ·mol-1、285.8kJ·mol-1、870.3kJ·mol-1,则2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为( )
| A.-488.3kJ·mol-1 | B.+488.3kJ·mol-1 |
| C.-191kJ·mol-1 | D.+191kJ·mol-1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐2】已知下列热化学方程式:
H2O(g)=H2O(l) △H=Q1kJ·mol-1;
C2H5OH(g)=C2H5OH(l) △H=Q2kJ·mol-1;
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H=Q3kJ·mol-1。
若46g液体酒精完全燃烧,最后恢复到室温,放出的热量为(单位:kJ)
H2O(g)=H2O(l) △H=Q1kJ·mol-1;
C2H5OH(g)=C2H5OH(l) △H=Q2kJ·mol-1;
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H=Q3kJ·mol-1。
若46g液体酒精完全燃烧,最后恢复到室温,放出的热量为(单位:kJ)
| A.3Q1+Q2+Q3 | B.-(3Q1+Q2+Q3) | C.-3Q1+Q2-Q3 | D.3Q1-Q2+Q3 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐3】煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaSO4(s)+4CO(g) CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
下列有关说法正确的是
CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)CaSO4(s)+4CO(g)
 CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)下列有关说法正确的是
| A.反应I在较低的温度下可自发进行 |
| B.反应II在较低的温度下可自发进行 |
C.用生石灰固硫的反应为:4CaO(s)+4SO2(g)  3CaSO4(s)+CaS(s) △H3,则△H3>△H2 3CaSO4(s)+CaS(s) △H3,则△H3>△H2 |
D.由反应I和反应II可计算出反应CaSO4(s)  CaO(s)+SO3(g)的焓变 CaO(s)+SO3(g)的焓变 |
您最近一年使用:0次

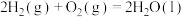
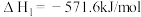

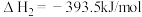
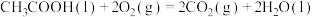
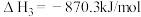
 的反应热
的反应热 为
为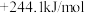
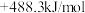




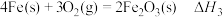
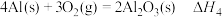
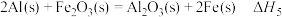
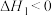 ,
,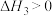
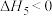 ,
,