下列条件的改变对反应 的影响说法不正确的是
的影响说法不正确的是
 的影响说法不正确的是
的影响说法不正确的是| A.升高温度能加快化学反应速率 |
| B.增大H2的浓度能加快化学反应速率 |
| C.达到化学平衡状态时,N2能全部转化为NH3 |
| D.增大压强可加快该反应的化学反应速率 |
2021高二上·江苏·学业考试 查看更多[12]
江苏省2021-2022学年高二上学期学业水平合格性调研考试化学试题江苏省扬州市红桥高级中学2022-2023学年高一下学期3月阶段性测试化学试题江苏省淮安市高中校协作体2022~2023学年高一下学期期中考试化学试题江苏省无锡市太湖高级中学2022-2023学年高一下学期期中考试化学试题江苏省扬州市广陵区红桥高级中学2022-2023学年高一下学期期中考试化学试题江苏省无锡市名校2022-2023学年高一下学期期中考试化学试题新疆维吾尔自治区喀什地区疏附县2022-2023学年高三上学期11月期中考试化学试题2024届江苏省苏州市南京航空航天大学苏州附属中学高三上学期二模化学试题江苏省淮安市涟水县第一中学2023-2024学年高二上学期第二次月考化学试卷江苏省徐州市丰县中学2023-2024学年高一下学期3月学情调研(一)化学试题(必修)江苏省扬州市广陵区红桥高级中学2023-2024学年高一下学期4月期中考试化学试题江苏省盐城市五校联考2023-2024学年高一下学期3月月考化学试题
更新时间:2021-12-14 21:28:45
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知丙酮的碘代反应CH3COCH3+ I2→CH3COCH2I + HI的速率方程为v=kcm(CH3COCH3)cn(I2),其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为0.7/k,改变反应物浓度时,反应的瞬时速率如表所示。
下列说法正确的是
| c(CH3COCH3)/ mol·L -1 | c(I2)/ mol·L-1 | v/10-3 mol· L-1·min-1 |
| 0.25 | 0.050 | 1.4 |
| 0.50 | 0.050 | 2.8 |
| 1.00 | 0.050 | 5.6 |
| 0.50 | 0.100 | 2.8 |
| A.速率方程中的m=1、n=1 |
| B.该反应的速率常数k=2.8 ×10-3 min-1 |
| C.增大I2的浓度,反应的瞬时速率不变 |
| D.在过量的I2存在时,反应掉75%的CH3COCH3所需的时间是375 min |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向绝热恒容密闭容器中通入 和
和 ,一定条件下使反应
,一定条件下使反应 达到平衡,正反应速率随时间变化如图所示。以下说法正确的是
达到平衡,正反应速率随时间变化如图所示。以下说法正确的是
 和
和 ,一定条件下使反应
,一定条件下使反应 达到平衡,正反应速率随时间变化如图所示。以下说法正确的是
达到平衡,正反应速率随时间变化如图所示。以下说法正确的是
| A.c点达到平衡状态 |
| B.反应物浓度:a点<b点 |
| C.反应物的总能量>生成物的总能量 |
| D.若起始投料相同,改用起始温度和体积均相同的恒温恒容容器,平衡时反应物的转化率下降 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】甲和乙两同学在同样的实验条件下,用同样的实验仪器和方法步骤进行中和热测定实验,实验试剂及用量如表所示。下列关于该实验的说法错误的是
| 实验者 | 反应物 | 起始温度t1/℃ | 终止温度t2/℃ | 中和热/kJ·mol-1 |
| 甲 | 1.0mol·L-1 HCl溶液50mL、1.1mol·L-1NaOH溶液50 mL | 18.0 | 25.8 | △H1 |
| 乙 | 1.0mol·L-1 HCl溶液50mL、1.1mol·L-1氨水50 mL | 18.0 | 25.3 | △H2 |
| A.两组实验的离子方程式均为H++OH-=H2O |
| B.中和热测定实验成功的关键是减少实验过程中热量的损失 |
| C.正常情况下,甲同学实验中中和反应起始速率大于乙同学 |
| D.两组实验中碱均过量,其目的是让酸反应完全 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向四个相同容积的密闭容器中分别充入一定量的CO、H2,发生反应:CO(g)+2H2(g) CH3OH(g)。开始反应时,按正反应速率由大到小的顺序排列,正确的是
CH3OH(g)。开始反应时,按正反应速率由大到小的顺序排列,正确的是
①在500℃时,5 mol CO和10 mol H2反应
②在500℃时,加入催化剂,10 mol H2与5 mol CO反应
③在450℃时,6 mol H2和3 mol CO反应
④在500℃时,6 mol H2和3 mol CO反应
⑤在450℃时,4 mol H2和2 mol CO反应
 CH3OH(g)。开始反应时,按正反应速率由大到小的顺序排列,正确的是
CH3OH(g)。开始反应时,按正反应速率由大到小的顺序排列,正确的是①在500℃时,5 mol CO和10 mol H2反应
②在500℃时,加入催化剂,10 mol H2与5 mol CO反应
③在450℃时,6 mol H2和3 mol CO反应
④在500℃时,6 mol H2和3 mol CO反应
⑤在450℃时,4 mol H2和2 mol CO反应
| A.②①③④⑤ | B.②①④③⑤ | C.⑤②①③④ | D.②④⑤③① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】恒温时,在体积为V的密闭容器内,可逆反应:N2 + 3H2 2NH 3 达平衡时,测得容器内气体的压强为p1 。将容器的体积压缩 V/2 至达到新的平衡时,气体的压强为 p2。则 p1和p 2的关系为
2NH 3 达平衡时,测得容器内气体的压强为p1 。将容器的体积压缩 V/2 至达到新的平衡时,气体的压强为 p2。则 p1和p 2的关系为
 2NH 3 达平衡时,测得容器内气体的压强为p1 。将容器的体积压缩 V/2 至达到新的平衡时,气体的压强为 p2。则 p1和p 2的关系为
2NH 3 达平衡时,测得容器内气体的压强为p1 。将容器的体积压缩 V/2 至达到新的平衡时,气体的压强为 p2。则 p1和p 2的关系为| A.p2 < p 1 | B.p1 < p2 < 2p1 | C.p1 > 2p2 | D.2p1 = p2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
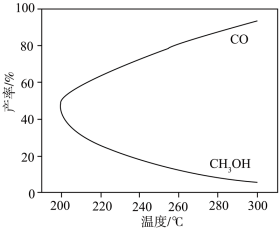
【推荐3】在一定条件下,利用CO2合成CH3OH的反应如下:CO2(g) + 3H2(g) CH3OH(g) + H2O(g) △H1,研究发现,反应过程中会有副反应:CO2(g) + H2(g)
CH3OH(g) + H2O(g) △H1,研究发现,反应过程中会有副反应:CO2(g) + H2(g)  CO(g)+ H2O(g) △H2,温度对CH3OH、CO的平衡产率影响如图所示。下列说法中,不正确的是
CO(g)+ H2O(g) △H2,温度对CH3OH、CO的平衡产率影响如图所示。下列说法中,不正确的是
 CH3OH(g) + H2O(g) △H1,研究发现,反应过程中会有副反应:CO2(g) + H2(g)
CH3OH(g) + H2O(g) △H1,研究发现,反应过程中会有副反应:CO2(g) + H2(g)  CO(g)+ H2O(g) △H2,温度对CH3OH、CO的平衡产率影响如图所示。下列说法中,不正确的是
CO(g)+ H2O(g) △H2,温度对CH3OH、CO的平衡产率影响如图所示。下列说法中,不正确的是
| A.△H1<0,△H2>0 |
| B.增大压强有利于加快合成反应的速率 |
| C.实际生产过程中,升高温度一定降低CH3OH的产率 |
| D.实际生产过程中,可以通过使用合适的催化剂提高CH3OH的选择性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】2SO2+O2 2SO3是制造硫酸的重要反应。下列关于该反应的说法正确的是
2SO3是制造硫酸的重要反应。下列关于该反应的说法正确的是
 2SO3是制造硫酸的重要反应。下列关于该反应的说法正确的是
2SO3是制造硫酸的重要反应。下列关于该反应的说法正确的是| A.使用催化剂不影响反应速率 |
| B.降低体系温度能加快反应速率 |
| C.增加O2的浓度能加快反应速率 |
| D.一定条件下达到反应限度时SO2全部转化为SO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2021年10月16日,长征二号F火箭将神舟十三号载人飞船送入太空。其火箭使用的推进剂为偏二甲肼(C2H8N2)和四氧化二氮(N2O4),发生反应的化学方程式为C2H8N2+2N2O4=2CO2↑+4H2O↑+3N2↑;已知偏二甲肼中C、N元素的化合价相等。反应2NO2(g)  N2O4(g)在一定体积的密闭容器中进行。下列说法正确的是
N2O4(g)在一定体积的密闭容器中进行。下列说法正确的是
 N2O4(g)在一定体积的密闭容器中进行。下列说法正确的是
N2O4(g)在一定体积的密闭容器中进行。下列说法正确的是| A.升高温度能减慢反应速率 |
| B.减小N2O4浓度能加快反应速率 |
| C.缩小反应容器的体积能加快反应速率 |
| D.达到化学平衡时,NO2能100%转化为N2O4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】由实验操作和现象,可得出相应正确结论是
| 实验操作 | 实验现象 | 解释或结论 | |
| A | 将铁锈溶于浓盐酸中,滴入高锰酸钾溶液 | 紫色褪去 | 铁锈中含有二价铁 |
| B | 石蜡油加强热,将产生的气体通入Br2的 CCl4溶液 | 溶液红棕色变无色 | 产生的气体中含有烯烃 |
| C | 向蔗糖溶液中滴加稀硫酸,水浴加热, 加入新制Cu(OH)2悬浊液 | 无砖红色沉淀 | 蔗糖未发生水解 |
| D | 加热试管中的聚氯乙烯薄膜碎片 | 试管口润湿的蓝色石 蕊试纸变红 | 氯乙烯加聚是可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在密闭容器中进行X2(g)+Y2(g) 2Z(g)的反应,已知起始时其中X2、Y2、Z各物质浓度分别为0.1mol∙L-1、0.3mol∙L-1、0.2mol∙L-1,反应达到平衡时,各物质浓度可能是
2Z(g)的反应,已知起始时其中X2、Y2、Z各物质浓度分别为0.1mol∙L-1、0.3mol∙L-1、0.2mol∙L-1,反应达到平衡时,各物质浓度可能是
 2Z(g)的反应,已知起始时其中X2、Y2、Z各物质浓度分别为0.1mol∙L-1、0.3mol∙L-1、0.2mol∙L-1,反应达到平衡时,各物质浓度可能是
2Z(g)的反应,已知起始时其中X2、Y2、Z各物质浓度分别为0.1mol∙L-1、0.3mol∙L-1、0.2mol∙L-1,反应达到平衡时,各物质浓度可能是| A.c(X)=0.2mol∙L-1 | B.c(Y2)=0.35mol∙L-1 |
| C.c(Y2)=0.2mol∙L-1 | D.c(Z)=0.4mol∙L-1 |
您最近一年使用:0次

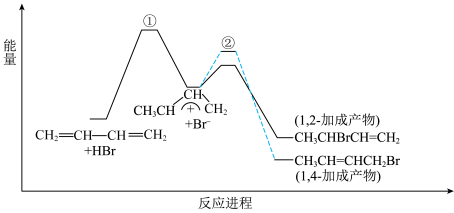
 加成机理如下,在
加成机理如下,在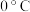 和
和 时,1,2-加成与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是
时,1,2-加成与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是