现有A、B、C三种气体,常温下,A是密度最小的气体,B是黄绿色单质气体,纯净的A可以在B中安静地燃烧,生成C。
(1)写出A在B中燃烧的化学方程式_______ 。
(2)把A、B、C三种气体分别通入硝酸酸化的硝酸银溶液中,出现白色沉淀的气体是_______ (用字母表示)。
(3)气体B通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合液,经测定Cl-与 的个数比为11:2,则所得溶液中ClO-与
的个数比为11:2,则所得溶液中ClO-与 的个数比为
的个数比为_______ 。
(4)金属Fe在B中燃烧的产物溶于水可以得到棕黄色溶液,某同学想利用该溶液来制备Fe(OH)3胶体:
①制备该胶体的离子方程式:_______ ;判断胶体制备成功的方法是_______ 。
②向制得的Fe(OH)3胶体中逐滴滴加稀盐酸,开始产生红褐色沉淀,这是因为_______ ,继续滴加,沉淀减少最终消失,写出离子反应方程式_______ 。
(1)写出A在B中燃烧的化学方程式
(2)把A、B、C三种气体分别通入硝酸酸化的硝酸银溶液中,出现白色沉淀的气体是
(3)气体B通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合液,经测定Cl-与
 的个数比为11:2,则所得溶液中ClO-与
的个数比为11:2,则所得溶液中ClO-与 的个数比为
的个数比为(4)金属Fe在B中燃烧的产物溶于水可以得到棕黄色溶液,某同学想利用该溶液来制备Fe(OH)3胶体:
①制备该胶体的离子方程式:
②向制得的Fe(OH)3胶体中逐滴滴加稀盐酸,开始产生红褐色沉淀,这是因为
更新时间:2021-12-16 14:42:31
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】随着科学技术的发展,许多新材料、新技术广泛应用于各个领域。
I.图1是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:
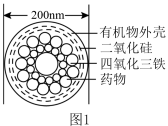
(1)“纳米药物分子车”分散于水中所得的分散系__________ (填“属于”或“不属于”)胶体。
(2)“纳米药物分子车”的外壳属于有机物。①酒精②蔗糖③冰醋酸中这三种有机物中,属于电解质的是__________ (填序号)。
(3)从元素组成的角度分析, 和
和 可归为同一类物质,其类别属于化合物中的
可归为同一类物质,其类别属于化合物中的__________ 。
Ⅱ.无土栽培技术的成功推广,营养液的准确配制是重要环节。某 营养液中含有
营养液中含有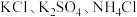 三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中
三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中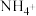 的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
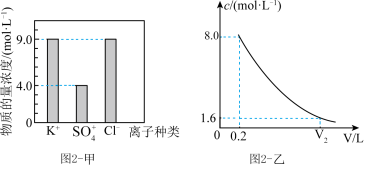
(4)该营养液中 的物质的量浓度为
的物质的量浓度为__________ 。
(5)写出一种与 含相同电子数的分子的化学式
含相同电子数的分子的化学式______________ ;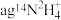 含有的中子的物质的量为
含有的中子的物质的量为__________ 。
Ⅲ.近年来,我国储氢材料的研制取得重大发展。其中电弧法合成储氢碳纳米管时,常伴有大量碳纳米颗粒杂质,这种碳纳米颗粒可用氧化气化法提纯,其反应原理如下:
_____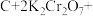 _____
_____ (稀)
(稀) ____
____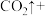 _____
_____ _____
_____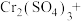 _____
_____
回答下列问题:
(6)完成上述反应的配平_________ 。
(7)某学生欲配制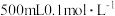 的稀硫酸,用量筒量取需要的浓硫酸,则需量取
的稀硫酸,用量筒量取需要的浓硫酸,则需量取 的浓硫酸
的浓硫酸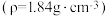 的体积为
的体积为__________ 。
(8)标准状况下,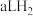 和
和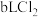 的混合气体,经强光充分照射后,所得气体恰好使含
的混合气体,经强光充分照射后,所得气体恰好使含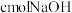 的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是
的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是____________________ 。
I.图1是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:

(1)“纳米药物分子车”分散于水中所得的分散系
(2)“纳米药物分子车”的外壳属于有机物。①酒精②蔗糖③冰醋酸中这三种有机物中,属于电解质的是
(3)从元素组成的角度分析,
 和
和 可归为同一类物质,其类别属于化合物中的
可归为同一类物质,其类别属于化合物中的Ⅱ.无土栽培技术的成功推广,营养液的准确配制是重要环节。某
 营养液中含有
营养液中含有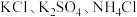 三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中
三种溶质,测得该营养液中部分离子的浓度柱状图如图2-甲所示,稀释过程中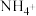 的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
的浓度(c)随溶液体积(V)变化的曲线如图2-乙所示。
(4)该营养液中
 的物质的量浓度为
的物质的量浓度为(5)写出一种与
 含相同电子数的分子的化学式
含相同电子数的分子的化学式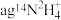 含有的中子的物质的量为
含有的中子的物质的量为Ⅲ.近年来,我国储氢材料的研制取得重大发展。其中电弧法合成储氢碳纳米管时,常伴有大量碳纳米颗粒杂质,这种碳纳米颗粒可用氧化气化法提纯,其反应原理如下:
_____
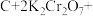 _____
_____ (稀)
(稀) ____
____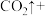 _____
_____ _____
_____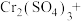 _____
_____
回答下列问题:
(6)完成上述反应的配平
(7)某学生欲配制
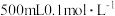 的稀硫酸,用量筒量取需要的浓硫酸,则需量取
的稀硫酸,用量筒量取需要的浓硫酸,则需量取 的浓硫酸
的浓硫酸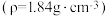 的体积为
的体积为(8)标准状况下,
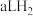 和
和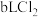 的混合气体,经强光充分照射后,所得气体恰好使含
的混合气体,经强光充分照射后,所得气体恰好使含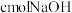 的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是
的氢氧化钠溶液完全转变为盐,则a、b、c应满足的关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将饱和的Fe Cl3溶液逐滴滴入沸水中,液体变为红褐色 :
(1)写出反应的化学方程式_____ 。
(2)将其装入U形管内,用石墨棒做电极,接通直流电源,通电一段时间后发现阴极附近颜色_____ ,这表明__________ ,这种现象称为_____ 。
(3)向其中逐滴加入过量稀硫酸,现象是______ ;原因是__________ 。
(1)写出反应的化学方程式
(2)将其装入U形管内,用石墨棒做电极,接通直流电源,通电一段时间后发现阴极附近颜色
(3)向其中逐滴加入过量稀硫酸,现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是___________。
(2)现有甲、乙两名同学进行Fe(OH)3胶体的制备实验正确的是___________ (填序号)。
①甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
②乙同学向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟。
(3)Fe(OH)3胶体制备的化学方程式为______________________ 。
(4)证明有Fe(OH)3胶体生成的实验操作是______________________ 。利用的胶体性质是___________ 。
(5)Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是___________ (填序号)。
A.胶粒直径大小不同 B.颜色不同 C.后者不稳定
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是___________。
| A.冷水 | B.沸水 |
| C.NaOH浓溶液 | D.NaCl浓溶液 |
①甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
②乙同学向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟。
(3)Fe(OH)3胶体制备的化学方程式为
(4)证明有Fe(OH)3胶体生成的实验操作是
(5)Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是
A.胶粒直径大小不同 B.颜色不同 C.后者不稳定
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硝酸是重要的化工原料,在工农业生产和国防上有重要用途。
(1)实验室利用硝石(NaNO3)和浓硫酸共热制取硝酸。
①该反应利用了浓硫酸的_______ 性;
②该反应的温度不宜太高,原因是(用化学方程式表示)______ ;
(2)工业上用氨气的催化氧化法制取硝酸,再利用硝酸和氨气反应生产NH4NO3。
①写出氨气的电子式_____ ;
②写出氨气催化氧化的化学方程式_______ ;
③在生产过程中,氨催化氧化生成氮氧化物的利用率是80%,氮氧化物被吸收得到硝酸的利用率是85%,则制取80 t的NH4NO3需要氨气______ t;
(3)某混合酸1L中含1mol的硝酸和2mol的硫酸。取该混合酸100mL,加入5.6g铁粉充分反应。
①反应中可以生成NO____ L(标准状况);
②向反应后的溶液再加入铁粉,能继续溶解铁粉____ g。
(1)实验室利用硝石(NaNO3)和浓硫酸共热制取硝酸。
①该反应利用了浓硫酸的
②该反应的温度不宜太高,原因是(用化学方程式表示)
(2)工业上用氨气的催化氧化法制取硝酸,再利用硝酸和氨气反应生产NH4NO3。
①写出氨气的电子式
②写出氨气催化氧化的化学方程式
③在生产过程中,氨催化氧化生成氮氧化物的利用率是80%,氮氧化物被吸收得到硝酸的利用率是85%,则制取80 t的NH4NO3需要氨气
(3)某混合酸1L中含1mol的硝酸和2mol的硫酸。取该混合酸100mL,加入5.6g铁粉充分反应。
①反应中可以生成NO
②向反应后的溶液再加入铁粉,能继续溶解铁粉
您最近一年使用:0次
【推荐2】铁是人体含量最多的微量元素,这些铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是_____ 。
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,以前有许多起因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有_____ 性。下列不能实现这种转化的物质是_____ (填字母)。
A.Cl2 B.O2 C.FeCl3 D.浓硫酸
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有___________ 性。
(4)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,每有1个Fe参加反应,被还原的HNO3为_____ 个。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,以前有许多起因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3 D.浓硫酸
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,每有1个Fe参加反应,被还原的HNO3为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据已经学过的化学知识,回答下列问题。
Ⅰ、金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________ 性;___________ (填“能”或“不能”)用氢氧化钠溶液代替。
(2)将Cu与稀硫酸混合,二者不能反应,滴入H2O2后,溶液很快变成蓝色,该反应的化学方程式为___________ 。
(3)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式:___________ 。
Ⅱ、物质的量是学习化学的基础。
(4)14.4gCO和CO2的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为___________ 。
(5)19g某二价金属的氯化物ACl2中含有0.4molCl-,金属A的相对原子质量是___________ 。
(6)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,被氧化的硫的物质的量为___________ mol。
Ⅰ、金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现
(2)将Cu与稀硫酸混合,二者不能反应,滴入H2O2后,溶液很快变成蓝色,该反应的化学方程式为
(3)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式:
Ⅱ、物质的量是学习化学的基础。
(4)14.4gCO和CO2的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为
(5)19g某二价金属的氯化物ACl2中含有0.4molCl-,金属A的相对原子质量是
(6)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,被氧化的硫的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】光卤石是生产钾盐和镁盐的原料,易溶于水。某课外小组通过下列实验测定某光卤石试样(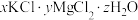 )的组成。
)的组成。
(1)取样品6.170g,加热至全部失去结晶水(杂质不分解),称得剩余固体的质量为4.010g,则样品中H2O的物质的量为___________ 。
(2)另取样品6.170g溶于水,加入过量氢氧化钠溶液,过滤、洗涤、干燥,得固体1.160g,试样中 的物质的量为
的物质的量为___________ 。
(3)另取样品6.170g溶于水,加入过量硝酸银溶液,过滤、洗涤、干燥,得固体8.610g,试样中 KCl的物质的量为___________ 。
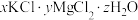 )的组成。
)的组成。(1)取样品6.170g,加热至全部失去结晶水(杂质不分解),称得剩余固体的质量为4.010g,则样品中H2O的物质的量为
(2)另取样品6.170g溶于水,加入过量氢氧化钠溶液,过滤、洗涤、干燥,得固体1.160g,试样中
 的物质的量为
的物质的量为(3)另取样品6.170g溶于水,加入过量硝酸银溶液,过滤、洗涤、干燥,得固体8.610g,试样中 KCl的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图为氯及其化合物的“价—类”二维图。
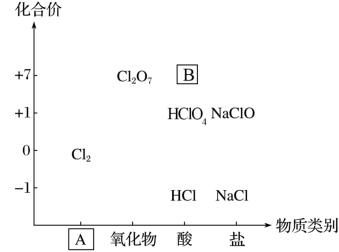
(1)根据二维图填写:A物质所属类别___ ;B物质的化学式__ 。
(2)某同学利用以下试剂研究HCl的性质,进行了如下预测:
从二维图上看,HCl的物质类别属于___ ;从化合价角度看,Cl-具有___ 性(填氧化性、还原性或既有氧化性又有还原性),下列物质在一定条件下可能与HCl发生反应的是__ (填字母)。
a.NaClO b.Fe c.NaOH d.KMnO4 e.AgNO3

(1)根据二维图填写:A物质所属类别
(2)某同学利用以下试剂研究HCl的性质,进行了如下预测:
从二维图上看,HCl的物质类别属于
a.NaClO b.Fe c.NaOH d.KMnO4 e.AgNO3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】二氧化氯消毒剂是国际公认的高效消毒灭菌剂。
(1)制备 的一种反应为:
的一种反应为: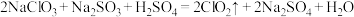 ,用单线桥法标出其电子转移的方向和数目
,用单线桥法标出其电子转移的方向和数目_____ 。
(2)实验室可用亚氯酸钠( )溶液与氯气反应制
)溶液与氯气反应制 ,此反应的化学方程式为
,此反应的化学方程式为_____ 。
(3) 可将废水中的
可将废水中的 转化为
转化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应中氧化剂与还原剂的物质的量之比是
,该反应中氧化剂与还原剂的物质的量之比是_____ 。
(4) 可经过题图所示的转化制取
可经过题图所示的转化制取 。已知“反应Ⅱ”为复分解反应。
。已知“反应Ⅱ”为复分解反应。

①“反应Ⅰ”的离子方程式为_____ 。
②过滤之后是洗涤,判断 沉淀是否洗涤干净的方法是
沉淀是否洗涤干净的方法是_____ 。
(5)一种“二氧化氯泡腾片”有效成分为 、
、 、
、 ,该泡腾片能快速溶于水,产生大量气泡,得到
,该泡腾片能快速溶于水,产生大量气泡,得到 溶液。取某品牌泡腾片1片溶于水配成
溶液。取某品牌泡腾片1片溶于水配成 溶液,为测定溶液中
溶液,为测定溶液中 的含量,进行了下列实验:
的含量,进行了下列实验:
①取该溶液 ,加入锥形瓶中,用稀硫酸调节溶液
,加入锥形瓶中,用稀硫酸调节溶液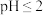 ,再加入足量
,再加入足量 晶体,发生反应:
晶体,发生反应: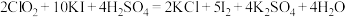
②用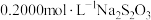 溶液和生成的碘单质反应,化学方程式如下:
溶液和生成的碘单质反应,化学方程式如下: ,恰好完全反应时消耗
,恰好完全反应时消耗 溶液
溶液 。则配成的
。则配成的 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为_____ 。
(1)制备
 的一种反应为:
的一种反应为: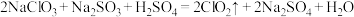 ,用单线桥法标出其电子转移的方向和数目
,用单线桥法标出其电子转移的方向和数目(2)实验室可用亚氯酸钠(
 )溶液与氯气反应制
)溶液与氯气反应制 ,此反应的化学方程式为
,此反应的化学方程式为(3)
 可将废水中的
可将废水中的 转化为
转化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应中氧化剂与还原剂的物质的量之比是
,该反应中氧化剂与还原剂的物质的量之比是(4)
 可经过题图所示的转化制取
可经过题图所示的转化制取 。已知“反应Ⅱ”为复分解反应。
。已知“反应Ⅱ”为复分解反应。
①“反应Ⅰ”的离子方程式为
②过滤之后是洗涤,判断
 沉淀是否洗涤干净的方法是
沉淀是否洗涤干净的方法是(5)一种“二氧化氯泡腾片”有效成分为
 、
、 、
、 ,该泡腾片能快速溶于水,产生大量气泡,得到
,该泡腾片能快速溶于水,产生大量气泡,得到 溶液。取某品牌泡腾片1片溶于水配成
溶液。取某品牌泡腾片1片溶于水配成 溶液,为测定溶液中
溶液,为测定溶液中 的含量,进行了下列实验:
的含量,进行了下列实验:①取该溶液
 ,加入锥形瓶中,用稀硫酸调节溶液
,加入锥形瓶中,用稀硫酸调节溶液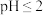 ,再加入足量
,再加入足量 晶体,发生反应:
晶体,发生反应: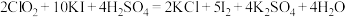
②用
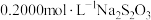 溶液和生成的碘单质反应,化学方程式如下:
溶液和生成的碘单质反应,化学方程式如下: ,恰好完全反应时消耗
,恰好完全反应时消耗 溶液
溶液 。则配成的
。则配成的 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】NaCl是一种化工原料,可以制备多种物质,如图所示。
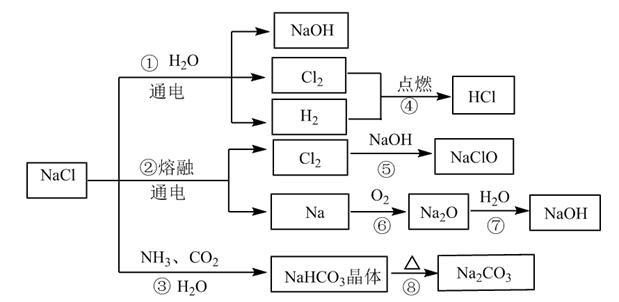
请回答下列问题:
(1)图所列物质中属于电解质的有___________ 种,转化反应中属于氧化还原反应的有___________ (填图中序号)
(2)工业上制取NaOH主要采用反应①,而不采用反应⑦的方法,主要原因是___________ 。
(3)反应④的现象是___________ ;反应⑤的化学方程式为___________ 。
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。某同学购买了一瓶某品牌的“84消毒液”,查看相关资料及包装说明可获得以下信息:原液净含量为600g、密度约为1.1g/cm3、有效成分NaClO的质量分数约为1.9%(通过有效氯含量折算而得)。该同学从中取出100mL原液,按包装说明稀释30倍(体积之比)后用于家庭一般物体表面消毒,稀释后的溶液中c(NaClO)=___________ mol/L(结果保留两位小数);“84消毒液”不能与“洁厕灵(主要成分是HCl)”混合使用,否则会产生黄绿色的有毒气体引起安全事故,其反应的离子方程式是___________ 。

请回答下列问题:
(1)图所列物质中属于电解质的有
(2)工业上制取NaOH主要采用反应①,而不采用反应⑦的方法,主要原因是
(3)反应④的现象是
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。某同学购买了一瓶某品牌的“84消毒液”,查看相关资料及包装说明可获得以下信息:原液净含量为600g、密度约为1.1g/cm3、有效成分NaClO的质量分数约为1.9%(通过有效氯含量折算而得)。该同学从中取出100mL原液,按包装说明稀释30倍(体积之比)后用于家庭一般物体表面消毒,稀释后的溶液中c(NaClO)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I磷酸氯喹是治疗新型肺炎的潜力药。磷酸是合成该药的初级原料之一,沸点高,难挥发。化学兴趣小组设计了合成磷酸的流程如图。
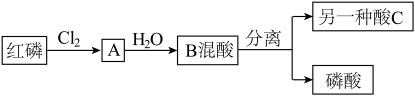
回答下列问题
(1)将一定了的红磷与氯气置于容积为2L的恒温恒容(温度,体积均不变)反应器中制取A,各物质的物质的量与时间关系如图

①前10s消耗的氯气为________ mol,该反应的化学方程式为_________ (A用化学式表示)
②前10s的平均反应速率v(Cl2)=________
(2)将A加入热水中,生成两种酸。一种为磷酸,反应过程各元素化合价不变。
①另一种是酸C是________ (写名称)
②A与热水反应的化学方程式为________
II(1)将反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,完成该原电池的装置示意图,并作相应标注(标明正负极材料及电解质溶液的名称,电子移动方向、离子移动方向)________

(2)该装置中负极的电极方程式为________ 。
(3)若在反应过程中电极减轻3.2g,则在导线中通过电子_____________ mol。

回答下列问题
(1)将一定了的红磷与氯气置于容积为2L的恒温恒容(温度,体积均不变)反应器中制取A,各物质的物质的量与时间关系如图

①前10s消耗的氯气为
②前10s的平均反应速率v(Cl2)=
(2)将A加入热水中,生成两种酸。一种为磷酸,反应过程各元素化合价不变。
①另一种是酸C是
②A与热水反应的化学方程式为
II(1)将反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,完成该原电池的装置示意图,并作相应标注(标明正负极材料及电解质溶液的名称,电子移动方向、离子移动方向)

(2)该装置中负极的电极方程式为
(3)若在反应过程中电极减轻3.2g,则在导线中通过电子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某同学在复习元素化合物的性质时,做了如下学习笔记,请你一起完成。
氯气的颜色为__________ ;由氯的原子结构示意图推测,氯气具有很强的______ 性。为了证明推测是否正确,进行如下实验:
I:将红热的铁丝伸入盛满氯气的集气瓶,观察铁丝在氯气中燃烧,有大量棕黄色烟。该反应的化学方程式是___________ 。
II:在空气中点燃H2,然后将导管缓缓伸入盛满氯气的集气瓶,可观察到H2在氯气中安静燃烧,产生______ 色的火焰,瓶口有白雾的现象。
由实验I、II可知,上述推测_____ (填“正确”或“不正确”)。
III:将氯气溶于水,制得氯水。下列物质不能与新制氯水反应的是_____ 。
A.Na2CO3溶液 B.FeCl2溶液 C.AgNO3 溶液 D.CuCl2溶液
氯气的颜色为
I:将红热的铁丝伸入盛满氯气的集气瓶,观察铁丝在氯气中燃烧,有大量棕黄色烟。该反应的化学方程式是
II:在空气中点燃H2,然后将导管缓缓伸入盛满氯气的集气瓶,可观察到H2在氯气中安静燃烧,产生
由实验I、II可知,上述推测
III:将氯气溶于水,制得氯水。下列物质不能与新制氯水反应的是
A.Na2CO3溶液 B.FeCl2溶液 C.AgNO3 溶液 D.CuCl2溶液
您最近一年使用:0次



