按要求填空
(1)我国化学家侯德榜改进国外的纯碱生产工艺,生产流程可简要表示如图
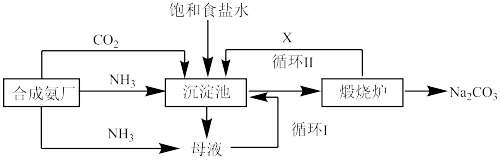
①生产时应往沉淀池中先后通入两种气体,先通入的气体为_______ 上述流程中X物质的化学式_______ 。
②请写出煅烧炉中发生反应的化学反应方程式:_______ 。上述流程中母液中最主要的成分是_______ (填化学式),检验这一组分的阴离子的具体方法是:_______ 。
(2)已知氨气具有还原性,能够和CuO发生氧化还原反应,反应后观察到黑色粉末逐渐变成红色,同时产生了使无水硫酸铜变蓝的物质,还有 一种无污染的气体单质生成,写出该反应的化学方程式:_______
(3)有两瓶无色溶液,分别是K2CO3和NaHCO3,请写出一种能鉴别这两种试剂的方法_______ 。(写出简要操作、现象和结论)
(1)我国化学家侯德榜改进国外的纯碱生产工艺,生产流程可简要表示如图

①生产时应往沉淀池中先后通入两种气体,先通入的气体为
②请写出煅烧炉中发生反应的化学反应方程式:
(2)已知氨气具有还原性,能够和CuO发生氧化还原反应,反应后观察到黑色粉末逐渐变成红色,同时产生了使无水硫酸铜变蓝的物质,还有 一种无污染的气体单质生成,写出该反应的化学方程式:
(3)有两瓶无色溶液,分别是K2CO3和NaHCO3,请写出一种能鉴别这两种试剂的方法
更新时间:2021-12-02 08:28:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】离子反应和氧化还原反应在生产、生活中应用广泛,用所学知识回答问题:
(1)新制氢氧化亚铁被氧气氧化,其化学方程式为______________ 。
(2)氯化铝溶液中滴加四羟基合铝酸钠溶液的离子方程式________ 。
(3)向硫酸铜溶液中逐滴滴加氨水至过量的离子方程式是____ 、______ 。
(4)向硫酸铝钾溶液中逐滴加入Ba(OH)2溶液至SO42-全部沉淀时的离子方程式_______ ;
(1)新制氢氧化亚铁被氧气氧化,其化学方程式为
(2)氯化铝溶液中滴加四羟基合铝酸钠溶液的离子方程式
(3)向硫酸铜溶液中逐滴滴加氨水至过量的离子方程式是
(4)向硫酸铝钾溶液中逐滴加入Ba(OH)2溶液至SO42-全部沉淀时的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】过氧化钠、过氧化镁、过氧化氢都是重要的过氧化物。回答下列问题:
(1)过氧化镁不溶于水,但易溶于稀酸.广泛用作胃药,治疗胃酸过多.试写出过氧化镁与胃酸反应的离子方程式:_____________________ 。
(2)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,工业上利用NaClO 和NaOH的混合溶液将Fe(OH)3氧化性制备高铁酸钠,反应的化学方程式为___________________ ;高铁酸钠能用作新型净水剂的原理是_________________ ;
(3)取少量含Fe2+、H+溶液于试管中,滴加几滴硫氰化钾溶液,无明显现象;再滴加H2O2,发现溶液变红色,其中包括的反应有_______________ 、______________ (写离子方程式);继续加H2O2,红色逐渐褪去且有气泡产生,反应原理如下:(已知SCN-中S为-2价,配平方程式)
___ H2O2+____ SCN--→____ SO42-+____ CO2↑+____ N2↑+____ H2O+____ H+
(1)过氧化镁不溶于水,但易溶于稀酸.广泛用作胃药,治疗胃酸过多.试写出过氧化镁与胃酸反应的离子方程式:
(2)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,工业上利用NaClO 和NaOH的混合溶液将Fe(OH)3氧化性制备高铁酸钠,反应的化学方程式为
(3)取少量含Fe2+、H+溶液于试管中,滴加几滴硫氰化钾溶液,无明显现象;再滴加H2O2,发现溶液变红色,其中包括的反应有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一些行业的废水中氨氮含量严重超标,废水脱氮已成为主要污染物减排和水体富营养化防治的研究热点,有多种方法可以去除。
I.电镀行业废水处理流程如图:
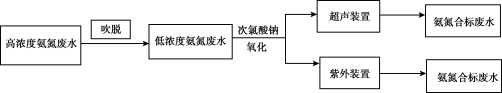
(1)吹脱法除氨氮:水中的氨氮大多数以NH4+和游离态的NH3保持平衡状态而存在。将空气直接通入水中,使气相和液相充分接触。水中溶解的游离氨穿过气液界面,向气相转移。从而达到脱除氨的目的。氨氮废水中NH3和NH4+平衡态的平衡关系有___ 。
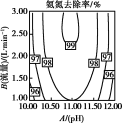
(2)温度、pH值、空气流量对脱除氨有很大的影响。pH值、空气流量对脱除氨影响如图所示。由图可以看出,空气流量一定时,10<pH<11时,吹脱率随着pH增加而增加,请用化学平衡移动原理解释原因___ 。
(3)次氯酸钠氧化法:利用次氯酸钠氧化废水中氨氮的离子方程式是___ 。
II.对于含有H2PO4-的氨氮废水还可以用电化学沉淀与阴极氧化协同去除水中的氨氮,装置如图所示。电解过程中,石墨毡电极产生OH-,在通入O2的情况,又产生H2O2,以氧化水中的NH4+,同时NH4+还可以通过生成MgNH4PO4•6H2O沉淀而持续被除去。
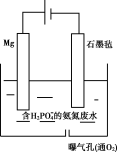
(1)阳极的电极反应式是___ 。
(2)废水中的NH4+'转化为MgNH4PO4•6H2O的离子方程式是___ 。
(3)pH大于10.5不利于MgNH4PO4•6H2O的生成,原因是___ 。
I.电镀行业废水处理流程如图:

(1)吹脱法除氨氮:水中的氨氮大多数以NH4+和游离态的NH3保持平衡状态而存在。将空气直接通入水中,使气相和液相充分接触。水中溶解的游离氨穿过气液界面,向气相转移。从而达到脱除氨的目的。氨氮废水中NH3和NH4+平衡态的平衡关系有
(2)温度、pH值、空气流量对脱除氨有很大的影响。pH值、空气流量对脱除氨影响如图所示。由图可以看出,空气流量一定时,10<pH<11时,吹脱率随着pH增加而增加,请用化学平衡移动原理解释原因

(3)次氯酸钠氧化法:利用次氯酸钠氧化废水中氨氮的离子方程式是
II.对于含有H2PO4-的氨氮废水还可以用电化学沉淀与阴极氧化协同去除水中的氨氮,装置如图所示。电解过程中,石墨毡电极产生OH-,在通入O2的情况,又产生H2O2,以氧化水中的NH4+,同时NH4+还可以通过生成MgNH4PO4•6H2O沉淀而持续被除去。

(1)阳极的电极反应式是
(2)废水中的NH4+'转化为MgNH4PO4•6H2O的离子方程式是
(3)pH大于10.5不利于MgNH4PO4•6H2O的生成,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
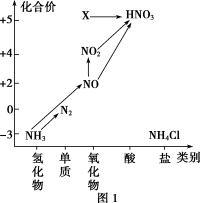
【推荐2】依据下图中氮元素及其化合物的转化关系,回答下列问题:_______ 。
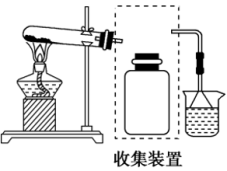
(2)若要收集一瓶氨,请将下列装置补充完整,在虚框内画出连接图_______ 。_______ 。
A.浓硫酸 B.碱石灰 C.NaOH固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO:化学方程式为_______ 。
②NO→NO2:实验现象是_______ 。
③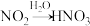 :氧化剂与还原剂的物质的量之比为
:氧化剂与还原剂的物质的量之比为_______ 。
(5)图1中,只用一种物质将NO直接转化为硝酸且绿色环保,则该物质的化学式为_______ 。
(6)图1中,X的化学式为_______ ,从物质性质上看,X属于_______ 氧化物。
(2)若要收集一瓶氨,请将下列装置补充完整,在虚框内画出连接图
A.浓硫酸 B.碱石灰 C.NaOH固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO:化学方程式为
②NO→NO2:实验现象是
③
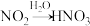 :氧化剂与还原剂的物质的量之比为
:氧化剂与还原剂的物质的量之比为(5)图1中,只用一种物质将NO直接转化为硝酸且绿色环保,则该物质的化学式为
(6)图1中,X的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】NH3和HNO3是重要的工业产品,如图是合成氨和氨氧化制硝酸的工艺流程。

(1)合成塔中发生反应的化学方程式是______ 。
(2)氨分离器中压强约为15MPa,温度约为-20℃,分离氨时应用了氨_____ 的性质,从氨分离器中又回到合成塔中的物质是______ 。
(3)氧化炉中反生反应的化学方程式是______ 。
(4)尾气中的少量NO、NO2可以用NH3来处理,在催化剂作用下生成无污染的气体,写出NO2和NH3反应的化学方程式______ 。当有5.6LNO2(标准状况)被还原时,转移电子的物质的量为______ mol。
(5)取一定量制取的硝酸加水稀释,加入过量的铜充分反应,用烧瓶共收集到6.72L(标况)NO、NO2的混合气体(不考虑N2O4),然后充入0.125molO2并倒扣于水槽中,水刚好充满整个烧瓶,则NO和NO2体积比是_____ 。

(1)合成塔中发生反应的化学方程式是
(2)氨分离器中压强约为15MPa,温度约为-20℃,分离氨时应用了氨
(3)氧化炉中反生反应的化学方程式是
(4)尾气中的少量NO、NO2可以用NH3来处理,在催化剂作用下生成无污染的气体,写出NO2和NH3反应的化学方程式
(5)取一定量制取的硝酸加水稀释,加入过量的铜充分反应,用烧瓶共收集到6.72L(标况)NO、NO2的混合气体(不考虑N2O4),然后充入0.125molO2并倒扣于水槽中,水刚好充满整个烧瓶,则NO和NO2体积比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
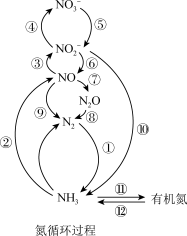
【推荐1】如图为氮的主要形态及氮的循环过程,主要包括同化吸收、氨化、硝化、反硝化、厌氧氨氧化和固氮。回答下列问题:
(1)图中属于氮的固定的是___________ (填数字序号)。
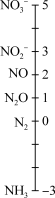
(2)反应②是工业上制硝酸的重要反应,写出该反应的化学方程式:___________ 。
(3)工业生产中,含NO、 废气可用澄清石灰水吸收,涉及反应为
废气可用澄清石灰水吸收,涉及反应为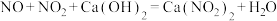 ;
;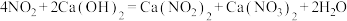 ,所得溶液经浓缩、结晶、过滤,得到
,所得溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是___________ (填化学式)。
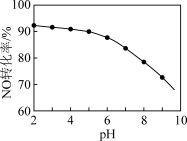
(4)NaClO溶液在酸性条件下可将NO转化为 ,其他条件相同,NO的转化率随NaClO溶液的pH(初始pH用稀硫酸调节)的变化如图所示。
,其他条件相同,NO的转化率随NaClO溶液的pH(初始pH用稀硫酸调节)的变化如图所示。
①在酸性条件下,NaClO溶液中存在HClO与NO生成 和
和 的反应,该反应的离子方程式为
的反应,该反应的离子方程式为___________ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是___________ 。
(5)可通过检测水中的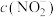 判断水质是否恶化,其原理是在酸性条件下
判断水质是否恶化,其原理是在酸性条件下 被
被 氧化为
氧化为 ,历程如下:
,历程如下:
I.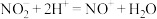
II.…
III.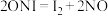
II的化学方程式为___________ 。
(6)二硫化亚铁( )与
)与 在反硝化细菌的作用下发生如下反应,请将离子方程式补充完整:
在反硝化细菌的作用下发生如下反应,请将离子方程式补充完整: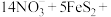
___________ 
___________
(1)图中属于氮的固定的是

(2)反应②是工业上制硝酸的重要反应,写出该反应的化学方程式:

(3)工业生产中,含NO、
 废气可用澄清石灰水吸收,涉及反应为
废气可用澄清石灰水吸收,涉及反应为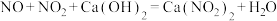 ;
;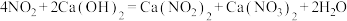 ,所得溶液经浓缩、结晶、过滤,得到
,所得溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是(4)NaClO溶液在酸性条件下可将NO转化为
 ,其他条件相同,NO的转化率随NaClO溶液的pH(初始pH用稀硫酸调节)的变化如图所示。
,其他条件相同,NO的转化率随NaClO溶液的pH(初始pH用稀硫酸调节)的变化如图所示。①在酸性条件下,NaClO溶液中存在HClO与NO生成
 和
和 的反应,该反应的离子方程式为
的反应,该反应的离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是

(5)可通过检测水中的
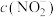 判断水质是否恶化,其原理是在酸性条件下
判断水质是否恶化,其原理是在酸性条件下 被
被 氧化为
氧化为 ,历程如下:
,历程如下:I.
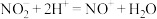
II.…
III.
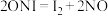
II的化学方程式为
(6)二硫化亚铁(
 )与
)与 在反硝化细菌的作用下发生如下反应,请将离子方程式补充完整:
在反硝化细菌的作用下发生如下反应,请将离子方程式补充完整: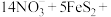

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
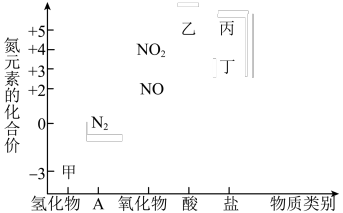
【推荐2】含氮化合物在农业、工业、国防等领域都有着广泛的应用。氮元素的价一类二维图如图,请回答下列问题:____________ ;丙为钠盐,其化学式为___________ 。
(2)甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为___________ 。
(3)甲的催化氧化是制备硝酸的重要反应,写出反应的化学方程式:___________ 。
(4)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:
NH3还原法:_________NH3+_________NO2 __________N2+_________H2O
__________N2+_________H2O
①配平NH3还原法的化学方程式:_________ 。
②碱液吸收法中,被氧化的物质是________ (填化学式)。
③同温同压下,将体积分别为V1、V2、V3的NO、NO2、O2混合于一个容积为V1+V2+V3的容器中后,倒立于水槽中,最终容器内充满水。则V2=__________ (用含V1、V3的代数式表示)。
(2)甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为
(3)甲的催化氧化是制备硝酸的重要反应,写出反应的化学方程式:
(4)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:

NH3还原法:_________NH3+_________NO2
 __________N2+_________H2O
__________N2+_________H2O①配平NH3还原法的化学方程式:
②碱液吸收法中,被氧化的物质是
③同温同压下,将体积分别为V1、V2、V3的NO、NO2、O2混合于一个容积为V1+V2+V3的容器中后,倒立于水槽中,最终容器内充满水。则V2=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】“价一类”二维图是元素化合物知识结构化的良好工具,如图是氮元素的“价一类”二维图。回答下列问题:

(1) 的电子式为
的电子式为_______ 。
(2)若物质 为
为 ,其气态呈
,其气态呈_______ 色,不能用排水法收集B气体的原因是_______ 。
(3) 是重要的化工原料,可以合成
是重要的化工原料,可以合成 ,写出工业上以
,写出工业上以 为原料制取
为原料制取 的第一步反应的化学方程式:
的第一步反应的化学方程式:_______ 。
(4)实验室中,检验 溶液中含有
溶液中含有 的实验操作和现象是
的实验操作和现象是_______ 。
(5)铜和足量的 的稀溶液反应,当生成
的稀溶液反应,当生成 (标准状况)
(标准状况) 时,转移的电子数目约为
时,转移的电子数目约为_______ ;反应中 表现的性质为
表现的性质为_______ (填字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(6)把盛有 由
由 和
和 组成的混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为
组成的混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为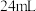 ,则原混合气中
,则原混合气中 的体积是
的体积是_______  。
。

(1)
 的电子式为
的电子式为(2)若物质
 为
为 ,其气态呈
,其气态呈(3)
 是重要的化工原料,可以合成
是重要的化工原料,可以合成 ,写出工业上以
,写出工业上以 为原料制取
为原料制取 的第一步反应的化学方程式:
的第一步反应的化学方程式:(4)实验室中,检验
 溶液中含有
溶液中含有 的实验操作和现象是
的实验操作和现象是(5)铜和足量的
 的稀溶液反应,当生成
的稀溶液反应,当生成 (标准状况)
(标准状况) 时,转移的电子数目约为
时,转移的电子数目约为 表现的性质为
表现的性质为A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(6)把盛有
 由
由 和
和 组成的混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为
组成的混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为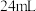 ,则原混合气中
,则原混合气中 的体积是
的体积是 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】 和
和 是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
(1)与酸反应的差异。甲组进行了如下4组实验。

其中实验________ 和_______ (填实验序号)可以鉴别 和
和 ,实验现象分别是
,实验现象分别是_______ 。
(2)稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。

①将分别装有 和
和 的试管同时放入装有某液体的烧杯中,对烧杯进行加热以便达到
的试管同时放入装有某液体的烧杯中,对烧杯进行加热以便达到 ,则烧杯中装的液体可以是
,则烧杯中装的液体可以是___________ (填字母)
A.水 B.酒精 C.植物油
②该实验用饱和碳酸钠溶液检验反应的产物,a、b试管中的实验现象分别为:___________ 、___________ 。
③试管b中发生反应的化学方程式为___________ 。
(3)与盐溶液反应的差异。丙组设计如下实验,探究 和
和 溶液与
溶液与 溶液反应的差异。(已知
溶液反应的差异。(已知 是表示浓度的一种单位)
是表示浓度的一种单位)
①若在室温下用 溶液鉴别同浓度的
溶液鉴别同浓度的 和
和 溶液,根据表格可知,选用的
溶液,根据表格可知,选用的 溶液的浓度最好是
溶液的浓度最好是___________ (填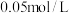 或
或 )。
)。
②请写出C组中 时,
时, 与
与 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
 和
和 是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:(1)与酸反应的差异。甲组进行了如下4组实验。

其中实验
 和
和 ,实验现象分别是
,实验现象分别是(2)稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。

①将分别装有
 和
和 的试管同时放入装有某液体的烧杯中,对烧杯进行加热以便达到
的试管同时放入装有某液体的烧杯中,对烧杯进行加热以便达到 ,则烧杯中装的液体可以是
,则烧杯中装的液体可以是A.水 B.酒精 C.植物油
②该实验用饱和碳酸钠溶液检验反应的产物,a、b试管中的实验现象分别为:
③试管b中发生反应的化学方程式为
(3)与盐溶液反应的差异。丙组设计如下实验,探究
 和
和 溶液与
溶液与 溶液反应的差异。(已知
溶液反应的差异。(已知 是表示浓度的一种单位)
是表示浓度的一种单位)| 实验组号 | 反应物 | 现象 | ||||
| 物质 | 浓度/ |  浓度/ 浓度/ | 是否有沉淀(室温) | 气泡情况 | ||
| 室温 | 60℃水浴 | |||||
| A |  | 0.05 | 0.05 | 有少量白色沉淀 | 无 | 无 |
| B |  | 0.05 | 0.05 | 有较多白色沉淀 | 无 | 无 |
| C |  | 0.5 | 0.5 | 有大量白色沉淀 | 无 | 有明显气泡 |
| D |  | 0.5 | 0.5 | 有大量白色沉淀 | 无 | 无 |
 溶液鉴别同浓度的
溶液鉴别同浓度的 和
和 溶液,根据表格可知,选用的
溶液,根据表格可知,选用的 溶液的浓度最好是
溶液的浓度最好是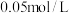 或
或 )。
)。②请写出C组中
 时,
时, 与
与 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
I.利用价类二维图像,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:
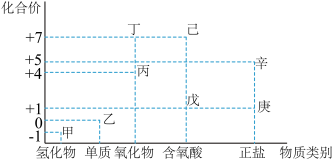
(1)丙的化学式为_______ ;戊的化学式为_______ ,具有_______ (任意写出一种戊具有的性质);
(2)根据氯元素的化合价判断,乙物质_______ 。
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)若庚是源白粉的有效成分。漂白粉也是常用消毒剂之一、漂白粉溶于水后,受空气中的 作用,产生有漂白、杀菌作用的次氯酸,其化学方程式为:
作用,产生有漂白、杀菌作用的次氯酸,其化学方程式为:_______ 。
II.某校化学课外小组为了鉴别 和
和 两种白色固体。用不同的方法做了以下实验,如图所示:
两种白色固体。用不同的方法做了以下实验,如图所示:

(4)方法I中逐滴加入 溶液
溶液_______ (填“能”或“不能”)鉴别 和
和 。
。
(5)方法II能鉴别 和
和 的现象是
的现象是_______ 。
(6)方法III、IV均能鉴别这两种物质,其中加热试管发生反应的化学方程式为____ ,与方法Ⅲ相比,方法IV的优点是____ (填字母)。
A.IV比III复杂
B.IV比III安全
C.IV比III操作简便
D.IV可以做到用一套装置同时进行两个实验,而III不行
(7)若用方法IV验证 和
和 的稳定性,则试管B中装入的固体是
的稳定性,则试管B中装入的固体是____ (填化学式)
I.利用价类二维图像,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:

(1)丙的化学式为
(2)根据氯元素的化合价判断,乙物质
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
(3)若庚是源白粉的有效成分。漂白粉也是常用消毒剂之一、漂白粉溶于水后,受空气中的
 作用,产生有漂白、杀菌作用的次氯酸,其化学方程式为:
作用,产生有漂白、杀菌作用的次氯酸,其化学方程式为:II.某校化学课外小组为了鉴别
 和
和 两种白色固体。用不同的方法做了以下实验,如图所示:
两种白色固体。用不同的方法做了以下实验,如图所示:
(4)方法I中逐滴加入
 溶液
溶液 和
和 。
。(5)方法II能鉴别
 和
和 的现象是
的现象是(6)方法III、IV均能鉴别这两种物质,其中加热试管发生反应的化学方程式为
A.IV比III复杂
B.IV比III安全
C.IV比III操作简便
D.IV可以做到用一套装置同时进行两个实验,而III不行
(7)若用方法IV验证
 和
和 的稳定性,则试管B中装入的固体是
的稳定性,则试管B中装入的固体是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请回答鉴定(认定)某白色固体样品(可能为NH4HCO3、NaHCO3、Na2CO3和NaCl中的一种)的下列问题。
(1)甲同学经分析后,认为以Ba(OH)2试液滴加到样品溶液中(必要时可加热),通过产生的现象即可完成实验。你认为该同学实验方案的设计________ (填写可行、不可行)。
(2)乙同学选用了试管、玻璃棒、酒精灯、试管夹;蒸馏水、pH试纸,通过合理、全面的实验步骤,给出了鉴定(认定)。
①为保证实验方案的顺利实施,乙同学在给固体样品加热时,正确的操作方法是__________________________________ 。(使用酒精灯和试管夹的方法不必叙述)
②乙在实验中可能要两次使用玻璃棒和pH试纸。第一次是将一小块试纸用蒸馏水润湿后粘在玻璃棒的一端,以便通过玻璃棒将试纸对准加热的试管附近;第二次(测试溶液的pH)的正确方法是_________________________ 。
③完成下表中空格部分的填写
(1)甲同学经分析后,认为以Ba(OH)2试液滴加到样品溶液中(必要时可加热),通过产生的现象即可完成实验。你认为该同学实验方案的设计
(2)乙同学选用了试管、玻璃棒、酒精灯、试管夹;蒸馏水、pH试纸,通过合理、全面的实验步骤,给出了鉴定(认定)。
①为保证实验方案的顺利实施,乙同学在给固体样品加热时,正确的操作方法是
②乙在实验中可能要两次使用玻璃棒和pH试纸。第一次是将一小块试纸用蒸馏水润湿后粘在玻璃棒的一端,以便通过玻璃棒将试纸对准加热的试管附近;第二次(测试溶液的pH)的正确方法是
③完成下表中空格部分的填写
固体试样 | 判断依据(要点) | 有关化学方程式(或离子方程式) |
碳酸氢铵 | NH4HCO3 NH3↑+CO2↑+H2O NH3↑+CO2↑+H2O | |
碳酸氢钠 | pH试纸显示有酸性气体产生 | 2NaHCO3 Na2CO3+CO2↑+H2O Na2CO3+CO2↑+H2OCO2+H2O  H2CO3 H2CO3 |
碳酸钠 | ||
氯化钠 | NaCl=Na++Cl- |
您最近一年使用:0次

 ,含
,含 、
、 氧化物等杂质)为主要原料制备红矾钠
氧化物等杂质)为主要原料制备红矾钠 ,首先将铬铁矿与纯碱在有氧条件下焙烧,该过程可将
,首先将铬铁矿与纯碱在有氧条件下焙烧,该过程可将 ,并将
,并将

