计算并回答下列问题:
(1)amol P和bmol Cl2恰好完全反应生成PCl3和PCl5的混合物,则混合物中PCl3和PCl5的物质的量之比为___________
(2)将标准状况下a L HCl溶解于m g的水中,得到盐酸溶液的物质的量浓度为b mol/L,则该盐酸溶液的密度为___________ g/cm3
(3)25℃时将Wg胆矾溶解在m g的水中,恰好得到饱和溶液,则该温度下,CuSO4的溶解度为___________ g
(4)将12mol/L的盐酸(密度为1.19g/ cm3)50mL稀释至6mol/L的盐酸(密度为1.10g/ cm3),需加水___________ mL
(5)某不纯的烧碱样品,含Na2CO3 3.8%、Na2O 5.8%、NaOH 90.4%。取M克样品,溶于40mL 2mol/L的盐酸中,并用2mol/L的NaOH溶液来中和剩余的盐酸至中性,把反应后的溶液蒸干后可得到固体质量是___________ g
(1)amol P和bmol Cl2恰好完全反应生成PCl3和PCl5的混合物,则混合物中PCl3和PCl5的物质的量之比为
(2)将标准状况下a L HCl溶解于m g的水中,得到盐酸溶液的物质的量浓度为b mol/L,则该盐酸溶液的密度为
(3)25℃时将Wg胆矾溶解在m g的水中,恰好得到饱和溶液,则该温度下,CuSO4的溶解度为
(4)将12mol/L的盐酸(密度为1.19g/ cm3)50mL稀释至6mol/L的盐酸(密度为1.10g/ cm3),需加水
(5)某不纯的烧碱样品,含Na2CO3 3.8%、Na2O 5.8%、NaOH 90.4%。取M克样品,溶于40mL 2mol/L的盐酸中,并用2mol/L的NaOH溶液来中和剩余的盐酸至中性,把反应后的溶液蒸干后可得到固体质量是
更新时间:2021-12-21 22:07:05
|
相似题推荐
计算题
|
较易
(0.85)
【推荐1】今有11.2g铁与500ml的盐酸恰好完全反应。求:
(1)在标准状况下,生成氢气的体积是多少升?
(2)反应前,盐酸的物质的量浓度?
(1)在标准状况下,生成氢气的体积是多少升?
(2)反应前,盐酸的物质的量浓度?
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)正常人的血液中葡萄糖(简称血糖,化学式为C6H12O6)的浓度在3.61-6.11 m mol / L之间,今测得某病人1mL血液中含葡萄糖0.60 mg,相当于_____________ mmol / L,他的血糖属正常、偏高还是偏低?________________ ;
(2)标准状况下11.2L,由CO和H2组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为___ ,如果此混合气体完全燃烧消耗氧气的物质的量为___ mol。
(2)标准状况下11.2L,由CO和H2组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】将4.6g钠投入一定量的水中,充分反应,所得溶液加水稀释到500mL。求:
(1)4.6g钠的物质的量;___________
(2)反应中生成的气体在标准状况下的体积;___________
(3)所得溶液中,溶质的物质的量浓度。___________
(1)4.6g钠的物质的量;
(2)反应中生成的气体在标准状况下的体积;
(3)所得溶液中,溶质的物质的量浓度。
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】(1)将40gNaOH溶于水,配成250mL溶液甲,甲的浓度为______ mol/L;将50mL甲加水稀释至100mL后,得溶液乙,乙的浓度为_____ mol/L。
(2)若18.6gNa2X中含有0.6mol钠离子,Na2X的摩尔质量是__ ,X的相对原子质量是___ 。
(2)若18.6gNa2X中含有0.6mol钠离子,Na2X的摩尔质量是
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】利用“化学计量在实验中的应用”的相关知识进行填空。
(1)49 g 的H2SO4的物质的量为______ mol。
(2)标准状况下,5.1g氨气的体积是__________ L。
(3)将53克Na2CO3 溶解在水中,配成500mL溶液,所得溶液中Na+物质的量浓度是_____ 。
(1)49 g 的H2SO4的物质的量为
(2)标准状况下,5.1g氨气的体积是
(3)将53克Na2CO3 溶解在水中,配成500mL溶液,所得溶液中Na+物质的量浓度是
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】按要求完成下列各题
(1)49gH2SO4中含有氧原子的物质的量为_______ ;
(2)标准状况下,0.2molNH3的体积是__________ ;
(3)在25gCuSO4·5H2O中:含有的Cu2+的数目是_________ ;含有的 的质量是
的质量是________ ;
(4)用14.2gNa2SO4配制成500mL溶液,其物质的量浓度为______ ,若从中取出10mL,含溶质质量为______ 。
(1)49gH2SO4中含有氧原子的物质的量为
(2)标准状况下,0.2molNH3的体积是
(3)在25gCuSO4·5H2O中:含有的Cu2+的数目是
 的质量是
的质量是(4)用14.2gNa2SO4配制成500mL溶液,其物质的量浓度为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐1】某小组设计如下实验研究实验室中的甲酸。已知:25℃时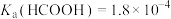
(1)配制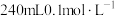 的HCOOH溶液,需
的HCOOH溶液,需 的HCOOH溶液的体积为
的HCOOH溶液的体积为_______ mL。
(2)为确定甲酸溶液的准确浓度,取20mL甲酸溶液于锥形瓶中,加入2滴_______ 溶液,用 的NaOH溶液滴定至终点,消耗NaOH溶液的体积为22.04mL,滴定实验中所使用的锥形瓶的容积最恰当的是
的NaOH溶液滴定至终点,消耗NaOH溶液的体积为22.04mL,滴定实验中所使用的锥形瓶的容积最恰当的是_______ (填字母)。
A.50mL B.100mL C.200mL D.250mL
(3)下列关于滴定操作的说法正确的_______
(4)小组同学用_______ 测出25℃时该甲酸溶液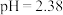 ,则水电离产生的
,则水电离产生的 数量级为
数量级为_______ 。
(5)25℃时甲酸与醋酸钠溶液反应: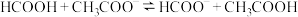 ,该反应的平衡常数为10,则该温度下醋酸的电离常数
,该反应的平衡常数为10,则该温度下醋酸的电离常数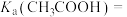
_______ 。
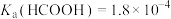
(1)配制
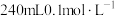 的HCOOH溶液,需
的HCOOH溶液,需 的HCOOH溶液的体积为
的HCOOH溶液的体积为(2)为确定甲酸溶液的准确浓度,取20mL甲酸溶液于锥形瓶中,加入2滴
 的NaOH溶液滴定至终点,消耗NaOH溶液的体积为22.04mL,滴定实验中所使用的锥形瓶的容积最恰当的是
的NaOH溶液滴定至终点,消耗NaOH溶液的体积为22.04mL,滴定实验中所使用的锥形瓶的容积最恰当的是A.50mL B.100mL C.200mL D.250mL
(3)下列关于滴定操作的说法正确的_______
| A.滴定前应检查滴定管是否漏水,进行洗涤、润洗 |
| B.将标准溶液装入滴定管时,应借助玻璃棒或漏斗等玻璃仪器转移 |
| C.进行滴定操作时,眼睛要始终注视着滴定管内液面的变化 |
| D.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 |
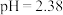 ,则水电离产生的
,则水电离产生的 数量级为
数量级为(5)25℃时甲酸与醋酸钠溶液反应:
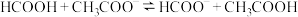 ,该反应的平衡常数为10,则该温度下醋酸的电离常数
,该反应的平衡常数为10,则该温度下醋酸的电离常数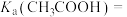
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】用14.2g无水硫酸钠配制成500mL溶液,其物质的量浓度为__________ mol•L-1。若从中取出50 mL,其物质的量浓度为__________ mol•L-1。若将这50 mL溶液用水稀释到100 mL,所得溶液中 的物质的量浓度为
的物质的量浓度为__________ mol•L-1, 的物质的量浓度为
的物质的量浓度为__________ mol•L-1。
 的物质的量浓度为
的物质的量浓度为 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐3】计算题(写计算过程)
Ⅰ.把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)Zn的物质的量______ ?(写出计算过程,下同)
(2)反应后ZnCl2的物质的量浓度______ ?
(3)生成H2的体积(标准状况)_______ ?
Ⅱ.实验室用密度为1.19g/cm3、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
(4)该浓盐酸中溶质的物质的量浓度为_______ ?
(5)用该浓盐酸配制250mL1.0mol L-1稀盐酸需要浓盐酸的体积是
L-1稀盐酸需要浓盐酸的体积是________ ?
Ⅰ.把13gZn放入500mL的盐酸中,Zn完全反应。(反应前后溶液体积变化忽略不计)计算:
(1)Zn的物质的量
(2)反应后ZnCl2的物质的量浓度
(3)生成H2的体积(标准状况)
Ⅱ.实验室用密度为1.19g/cm3、溶质质量分数为36.5%的浓盐酸配制稀盐酸,用于制备氢气。
(4)该浓盐酸中溶质的物质的量浓度为
(5)用该浓盐酸配制250mL1.0mol
 L-1稀盐酸需要浓盐酸的体积是
L-1稀盐酸需要浓盐酸的体积是
您最近一年使用:0次




