下列有关有效碰撞理论和活化能的认识错误的是
| A.对于气体参与的反应增大压强,活化分子百分数增加,故反应速率增大 |
| B.选用适当的催化剂,降低活化能,活化分子百分数增加,碰撞频率增加 |
| C.温度升高,分子动能增加,活化分子百分数增加,增加了碰撞频率 |
| D.溶液中Ag+和Cl-的反应活化能接近于零,反应几乎在瞬间完成 |
更新时间:2021-12-22 18:46:33
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在Cu(I)催化剂和水存在条件下, 还原为CO反应机理如图所示。图a为通过实验观察捕获中间体和产物推理出
还原为CO反应机理如图所示。图a为通过实验观察捕获中间体和产物推理出 还原为CO反应过程示意图;图b.表示
还原为CO反应过程示意图;图b.表示 转化为CO。反应过程经历中间体的能垒(活化分子含有的能参加化学反应的最低限度的能量,称为化学反应的能垒)变化。
转化为CO。反应过程经历中间体的能垒(活化分子含有的能参加化学反应的最低限度的能量,称为化学反应的能垒)变化。
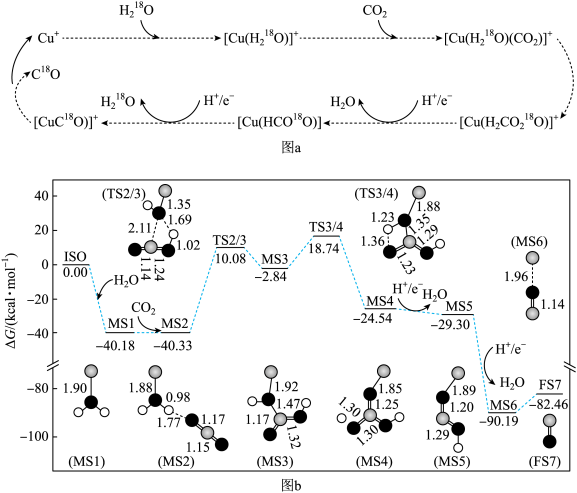
提示:MS代表反应物或中间产物;TS代表过渡态。FS代表终态产物。下列推断错误的是
 还原为CO反应机理如图所示。图a为通过实验观察捕获中间体和产物推理出
还原为CO反应机理如图所示。图a为通过实验观察捕获中间体和产物推理出 还原为CO反应过程示意图;图b.表示
还原为CO反应过程示意图;图b.表示 转化为CO。反应过程经历中间体的能垒(活化分子含有的能参加化学反应的最低限度的能量,称为化学反应的能垒)变化。
转化为CO。反应过程经历中间体的能垒(活化分子含有的能参加化学反应的最低限度的能量,称为化学反应的能垒)变化。
提示:MS代表反应物或中间产物;TS代表过渡态。FS代表终态产物。下列推断错误的是
| A.由图b知,总反应和各步反应的△H均小于0 |
B.在图a中,总反应是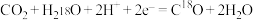 |
| C.在图b涉及的反应中,MS2→MS3是速控反应 |
D.由图a可知, 是总反应催化剂且化合价保持不变 是总反应催化剂且化合价保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】过渡金属元素离子催化乙烯氧化成乙醛的反应机理如图所示。下列说法正确的是
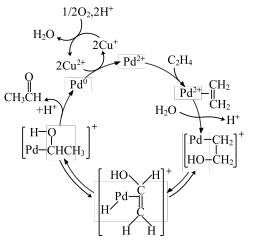

A. 和 和 能够降低反应的活化能 能够降低反应的活化能 |
| B.该反应历程中氢离子物质的量一直减小 |
| C.Pd的化合价在反应历程中未发生变化 |
D.该历程的总反应为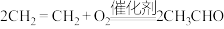 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】物质R能同时发生如下反应:①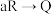 ;②
;②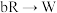 (a、b均为正整数)。恒容体系中R、Q、W的浓度c随时间t的变化曲线如图所示,下列说法错误的是
(a、b均为正整数)。恒容体系中R、Q、W的浓度c随时间t的变化曲线如图所示,下列说法错误的是

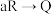 ;②
;②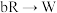 (a、b均为正整数)。恒容体系中R、Q、W的浓度c随时间t的变化曲线如图所示,下列说法错误的是
(a、b均为正整数)。恒容体系中R、Q、W的浓度c随时间t的变化曲线如图所示,下列说法错误的是
A. | B.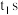 时, 时,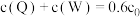 |
| C.活化能:①<② | D.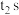 时,R的消耗速率大于W的生成速率 时,R的消耗速率大于W的生成速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上可采用CH3OH CO+2H2的方法来制取高纯度的
CO+2H2的方法来制取高纯度的  和
和 。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的及应历程,其中吸附在钯催化剂表面上的物种用*标注。下图为计算机模拟的各步反应的能量变化示意图,下列说法正确的是
。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的及应历程,其中吸附在钯催化剂表面上的物种用*标注。下图为计算机模拟的各步反应的能量变化示意图,下列说法正确的是
 CO+2H2的方法来制取高纯度的
CO+2H2的方法来制取高纯度的  和
和 。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的及应历程,其中吸附在钯催化剂表面上的物种用*标注。下图为计算机模拟的各步反应的能量变化示意图,下列说法正确的是
。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的及应历程,其中吸附在钯催化剂表面上的物种用*标注。下图为计算机模拟的各步反应的能量变化示意图,下列说法正确的是
A. 分子做配体时, 分子做配体时, 原子是配位原子 原子是配位原子 |
B.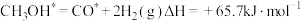 |
| C.使用催化剂可以增大反应进行的程度 |
D.该历程中决速步骤活化能 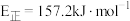 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关化学反应速率的说法正确的是
A.用铁片与稀硫酸反应制取氢气时,改用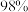 的浓硫酸可增大产生氢气的速率 的浓硫酸可增大产生氢气的速率 |
B. 的盐酸与锌片反应,加入适量的氯化钠溶液,化学反应速率不变 的盐酸与锌片反应,加入适量的氯化钠溶液,化学反应速率不变 |
C. 的催化氧化反应是一个放热反应,所以升高温度,化学反应速率减小 的催化氧化反应是一个放热反应,所以升高温度,化学反应速率减小 |
D.汽车尾气中的 与 与 可以缓慢反应生成 可以缓慢反应生成 和 和 ,增大压强,化学反应速率增大 ,增大压强,化学反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一密闭容器中充入1 mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发生反应H2(g)+I2(g)⇌2HI(g),下列说法正确的是
| A.保持容器容积不变,向其中加入1 mol H2,化学反应速率不变 |
| B.保持容器容积不变,向其中加入1 mol Ar,化学反应速率增大 |
| C.保持容器内气体压强不变,向其中加入1 mol Ar,化学反应速率不变 |
| D.保持容器内气体压强不变,向其中加入1 mol H2(g)和1 mol I2(g),化学反应速率不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】由下列实验操作和现象得出的结论错误的是
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下,分别用浓HNO3和稀HNO3与铁反应 | 稀HNO3与铁反应快 | 其它条件相同,反应物浓度越小,反应速率越快 |
| B | 往盛有FeCl3溶液的试管中滴加几滴淀粉-碘化钾溶液 | 溶液变蓝 | 氧化性:Fe2+>I2 |
| C | 常温下,向三支试管中分别加入1mL0.1mol/L、0.2mol/L、0.3mol/LNa2S2O3溶液,再同时分别加入2mL0.5mol/L稀硫酸 | 加入0.3mol/LNa2S2O3溶液的试管最先沉淀 | 其它条件相同,c(Na2S2O3)越大,反应生成S的速率越快 |
| D | 向盛有稀盐酸的试管中加入铁粉 | 刚开始时一段时间内产生气泡的速率加快 | 铁与稀盐酸反应放出热量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】为了研究外界条件对 分解反应速率的影响,某同学在相应条件下进行实验,实验记录如下表:
分解反应速率的影响,某同学在相应条件下进行实验,实验记录如下表:
下列说法中,不正确的是
 分解反应速率的影响,某同学在相应条件下进行实验,实验记录如下表:
分解反应速率的影响,某同学在相应条件下进行实验,实验记录如下表:| 实验序号 | 反应物 | 温度 | 催化剂 | 收集VmL气体所用时间 |
| ① | 5mL 4% 溶液 溶液 | 25℃ | 2滴  溶液 溶液 |  |
| ② | 5mL 4% 溶液 溶液 | 45℃ | 2滴  溶液 溶液 |  |
| ③ | 5mL 12% 溶液 溶液 | 45℃ | 2滴  溶液 溶液 |  |
| ④ | 5mL 4% 溶液 溶液 | T℃ | 无 |  |
| A.选择①和④实验研究催化剂对反应速率的影响,必须控制T=25 |
| B.通过实验①②,可研究温度对反应速率的影响 |
C.所用时间: |
| D.反应速率:③>② |
您最近一年使用:0次

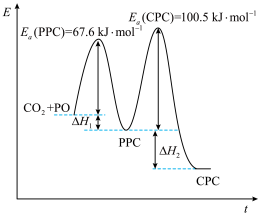
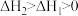
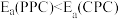 ,主反应的速率低于副反应速率
,主反应的速率低于副反应速率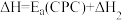
 、
、 、
、 、
、 、
、 、
、 等)制取硒的流程如下:
等)制取硒的流程如下:
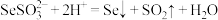
 2CO(g),能使反应速率加快的措施
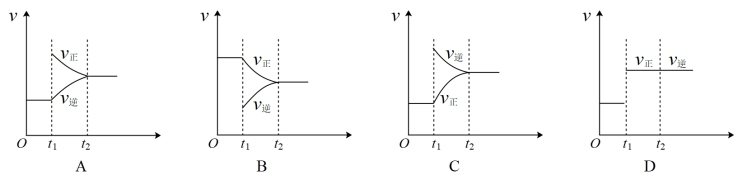
2CO(g),能使反应速率加快的措施 2SO3(g)(放热反应)已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是(O~t1:v正=v逆;t1时改变条件,t2时重新建立平衡)
2SO3(g)(放热反应)已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是(O~t1:v正=v逆;t1时改变条件,t2时重新建立平衡)