利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:
已知:
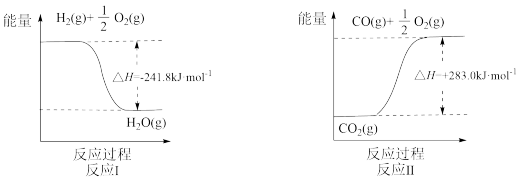
(1)反应Ⅱ是___________ 反应(填“吸热”或“放热”),其原因是___________ 。
(2)反应A的热化学方程式是___________ 。
反应A:

已知:

(1)反应Ⅱ是
(2)反应A的热化学方程式是
更新时间:2022/01/28 18:35:57
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现代社会的一切活动都离不开能源,为了更好的利用化学反应中的物质和能量变化,需要关注化学反应的快慢和程度。
Ⅰ.化学变化过程中均存在物质变化与能量变化,某化学兴趣小组进行如图1所示实验,以验证此结论。请回答下列问题。___________ 生成物成键释放的能量 填“大于”或“小于”
填“大于”或“小于” ;反应②中,反应物的总能量
;反应②中,反应物的总能量___________ 生成物的总能量 填“高于”或“低于”
填“高于”或“低于” 。
。
Ⅱ.某小组利用Na2S2O3溶液和稀硫酸的反应,通过比较反应完全所用时间长短验证不同因素对化学反应速率的影响。实验设计如表所示:
(2) 和稀硫酸反应的离子方程式为
和稀硫酸反应的离子方程式为___________ 。
(3)依据化学反应原理判断平均用时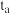
___________ 5(填“>”“=”或“<”)。
(4)通过对比实验a和c,验证稀 的浓度对反应速率的影响。该小组发现实验c存在不科学性,请提出对实验c的改进方案
的浓度对反应速率的影响。该小组发现实验c存在不科学性,请提出对实验c的改进方案___________ 。
Ⅲ.某同学用等质量的锌粉先后与盐酸及相同体积、未知浓度的盐酸反应,记录相关数据,并作出这两个反应过程中放出气体的体积随反应时间的变化曲线图(如图2所示)。___________  (填“>”“=”或“<”),若用
(填“>”“=”或“<”),若用 硫酸代替上述实验中的
硫酸代替上述实验中的 盐酸,二者的反应速率是否相同?理由是
盐酸,二者的反应速率是否相同?理由是___________ 。
(6)为控制反应速率,防止因反应过快而难以测量 体积,且不改变生成
体积,且不改变生成 的量,事先在盐酸中加入等体积的下列溶液以减慢反应速率。下列试剂中,不可行的是___________。
的量,事先在盐酸中加入等体积的下列溶液以减慢反应速率。下列试剂中,不可行的是___________。
Ⅰ.化学变化过程中均存在物质变化与能量变化,某化学兴趣小组进行如图1所示实验,以验证此结论。请回答下列问题。

 填“大于”或“小于”
填“大于”或“小于” ;反应②中,反应物的总能量
;反应②中,反应物的总能量 填“高于”或“低于”
填“高于”或“低于” 。
。Ⅱ.某小组利用Na2S2O3溶液和稀硫酸的反应,通过比较反应完全所用时间长短验证不同因素对化学反应速率的影响。实验设计如表所示:
| 实验编号 |  |  溶液 溶液 | 稀 溶液 溶液 | 反应完全所用时间 秒 秒 | ||
 |  | 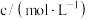 |  | s | ||
| a | 298 | 0.1 | 10 | 0 | 10 | 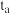 |
| b | 323 | 0.1 | 10 | 0.2 | 10 | 5 |
| c | 298 | 0.1 | 10 | 0.2 | 5 | 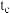 |
(2)
 和稀硫酸反应的离子方程式为
和稀硫酸反应的离子方程式为(3)依据化学反应原理判断平均用时
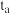
(4)通过对比实验a和c,验证稀
 的浓度对反应速率的影响。该小组发现实验c存在不科学性,请提出对实验c的改进方案
的浓度对反应速率的影响。该小组发现实验c存在不科学性,请提出对实验c的改进方案Ⅲ.某同学用等质量的锌粉先后与盐酸及相同体积、未知浓度的盐酸反应,记录相关数据,并作出这两个反应过程中放出气体的体积随反应时间的变化曲线图(如图2所示)。
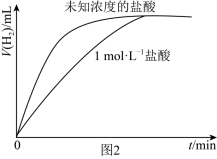
 (填“>”“=”或“<”),若用
(填“>”“=”或“<”),若用 硫酸代替上述实验中的
硫酸代替上述实验中的 盐酸,二者的反应速率是否相同?理由是
盐酸,二者的反应速率是否相同?理由是(6)为控制反应速率,防止因反应过快而难以测量
 体积,且不改变生成
体积,且不改变生成 的量,事先在盐酸中加入等体积的下列溶液以减慢反应速率。下列试剂中,不可行的是___________。
的量,事先在盐酸中加入等体积的下列溶液以减慢反应速率。下列试剂中,不可行的是___________。| A.蒸馏水 | B. 溶液 溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】化学反应过程中既有物质变化,也有能量变化。中和反应是化学中的一种重要反应,酸、碱在互相交换成分的过程中,也产生了能量的变化。
(1)中和反应是放热反应,下列反应也属于放热反应的是___________
(2)中和热的理论数值为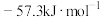 。
。
①请写出氢氧化钠和盐酸反应的热化学方程式:___________ 。
②若用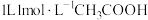 与等体积、等浓度的氢氧化钠溶液混合,放出的热量
与等体积、等浓度的氢氧化钠溶液混合,放出的热量___________ (填“大于”、“小于”或“等于”,后同) 。若用
。若用 稀
稀 与等体积、等浓度的
与等体积、等浓度的 溶液混合,放出的热量
溶液混合,放出的热量___________  。
。
(3)将 盐酸和
盐酸和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持
溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持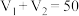 。下列叙述正确的是___________
。下列叙述正确的是___________
(1)中和反应是放热反应,下列反应也属于放热反应的是___________
| A.铝热反应 | B. 与 与 混合 混合 |
| C.碳酸氢钠分解 | D.冰融化为水 |
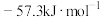 。
。①请写出氢氧化钠和盐酸反应的热化学方程式:
②若用
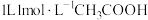 与等体积、等浓度的氢氧化钠溶液混合,放出的热量
与等体积、等浓度的氢氧化钠溶液混合,放出的热量 。若用
。若用 稀
稀 与等体积、等浓度的
与等体积、等浓度的 溶液混合,放出的热量
溶液混合,放出的热量 。
。(3)将
 盐酸和
盐酸和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持
溶液混合均匀后测量并记录溶液的温度,实验结果如图所示,实验中始终保持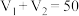 。下列叙述正确的是___________
。下列叙述正确的是___________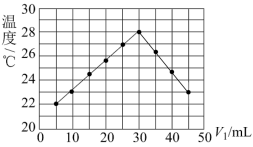
A.做该实验时环境温度低于 |
B.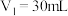 时,盐酸和氢氧化钠溶液恰好完全反应 时,盐酸和氢氧化钠溶液恰好完全反应 |
C. 溶液的浓度约为 溶液的浓度约为 |
| D.该实验表明有水生成的反应都是放热反应。 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题。
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察下图,图中所示反应是_______ (填“吸热”或“放热”)反应,该反应的
_______ (用 、
、 的代表示);下列4个反应中,不符合示意图描述的反应的是
的代表示);下列4个反应中,不符合示意图描述的反应的是_______ 。 反应
反应
C.盐酸与NaOH反应 D.Na与 反应生成
反应生成
(2)已知碳的燃烧热为-393.15kJ/mol,氢气的燃烧热为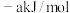 ,一氧化碳的燃烧热为
,一氧化碳的燃烧热为 ,请写出碳的燃烧热对应的热化学反应方程式
,请写出碳的燃烧热对应的热化学反应方程式_______ ,那么热化学反应

_______ kJ/mol(用a,b表示)。_______ ,如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等、不相等”),请以本实验测得数据为准,写出盐酸与NaOH反应中表示中和热的热化学反应方程_______ 。
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察下图,图中所示反应是

 、
、 的代表示);下列4个反应中,不符合示意图描述的反应的是
的代表示);下列4个反应中,不符合示意图描述的反应的是
 反应
反应C.盐酸与NaOH反应 D.Na与
 反应生成
反应生成
(2)已知碳的燃烧热为-393.15kJ/mol,氢气的燃烧热为
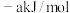 ,一氧化碳的燃烧热为
,一氧化碳的燃烧热为 ,请写出碳的燃烧热对应的热化学反应方程式
,请写出碳的燃烧热对应的热化学反应方程式


您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题
(1)下列各组物质:a.35Cl与37Cl B.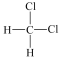 与
与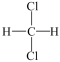 C.
C.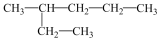 与
与 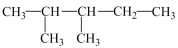 D.O2与O3 E.CH3-CH=CH2与CH3-CH2-CH=CH2
D.O2与O3 E.CH3-CH=CH2与CH3-CH2-CH=CH2
①属于同系物的是_______
②属于同素异形体的是_______
③属于同分异构体的是_______
(2)下列反应中,属于放热反应的是_______ ,属于吸热反应的是_______ 。(填序号)
①物质燃烧;②石灰石在高温下的分解反应;③酸碱中和反应;④二氧化碳通过炽热的炭;⑤食物因氧化而腐败;⑥Ba(OH)2·8H2O与NH4Cl反应;⑦氧化钙与水反应
(3)已知:Ⅰ.C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
Ⅱ.2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ·mol-1
Ⅲ.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2 599.2 kJ·mol-1
则由C(石墨,s)和H2(g)反应生成1 mol C2H2(g)的焓变ΔH=_______ 。
(4)某种甲烷燃料电池的工作原理如图所示,回答下列问题:
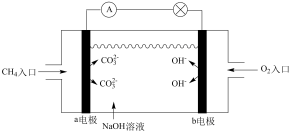
甲烷通入的一极为电源的_______ 极,该电极反应式:_______ ;当电路中累计有2mol电子通过时,消耗的氧气体积为(在标准状况下)_______ L
(1)下列各组物质:a.35Cl与37Cl B.
 与
与 C.
C. 与
与  D.O2与O3 E.CH3-CH=CH2与CH3-CH2-CH=CH2
D.O2与O3 E.CH3-CH=CH2与CH3-CH2-CH=CH2 ①属于同系物的是
②属于同素异形体的是
③属于同分异构体的是
(2)下列反应中,属于放热反应的是
①物质燃烧;②石灰石在高温下的分解反应;③酸碱中和反应;④二氧化碳通过炽热的炭;⑤食物因氧化而腐败;⑥Ba(OH)2·8H2O与NH4Cl反应;⑦氧化钙与水反应
(3)已知:Ⅰ.C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
Ⅱ.2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ·mol-1
Ⅲ.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2 599.2 kJ·mol-1
则由C(石墨,s)和H2(g)反应生成1 mol C2H2(g)的焓变ΔH=
(4)某种甲烷燃料电池的工作原理如图所示,回答下列问题:

甲烷通入的一极为电源的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ/mol,H—H键的键能是436.0 kJ/mol;由N2和H2合成1 mol NH3时可放出46.2 kJ的热量。则N—H键的键能是______ 。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol ①
3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) ΔH=-47.2 kJ/mol ②
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+640.5 kJ/mol ③
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式______ 。
(3)已知两个热化学方程式:
C(s)+O2(g)=CO2(g) △H= ― 393.5kJ/mol
2H2(g)+O2(g)=2H2O(g) △H= ― 483.6kJ/mol
现有炭粉和H2组成的悬浮气共0.2mol,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是______ 。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol ①
3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) ΔH=-47.2 kJ/mol ②
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+640.5 kJ/mol ③
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式
(3)已知两个热化学方程式:
C(s)+O2(g)=CO2(g) △H= ― 393.5kJ/mol
2H2(g)+O2(g)=2H2O(g) △H= ― 483.6kJ/mol
现有炭粉和H2组成的悬浮气共0.2mol,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。回答下列问题:
(1)已知298K时,白磷、红磷完全燃烧的热化学方程式如下:
P4(白磷,s)+5O2(g)=P4O10(s) △H1=-2983.2kJ•mol-1
P(红磷,s)+ O2(g)=
O2(g)= P4O10(s) △H2=-738.5kJ•mol-1
P4O10(s) △H2=-738.5kJ•mol-1
则该温度下,白磷转化为红磷的热化学方程式为___ 。
(2)已知298K时白磷不完全燃烧的热化学方程式为P4(白磷,s)+3O2(g)=P4O6(s) △H=-1638kJ•mol-1。在某密闭容器中加入62g白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为___ ,反应过程中放出的热量为___ kJ(保留2位小数)。
(1)已知298K时,白磷、红磷完全燃烧的热化学方程式如下:
P4(白磷,s)+5O2(g)=P4O10(s) △H1=-2983.2kJ•mol-1
P(红磷,s)+
 O2(g)=
O2(g)= P4O10(s) △H2=-738.5kJ•mol-1
P4O10(s) △H2=-738.5kJ•mol-1则该温度下,白磷转化为红磷的热化学方程式为
(2)已知298K时白磷不完全燃烧的热化学方程式为P4(白磷,s)+3O2(g)=P4O6(s) △H=-1638kJ•mol-1。在某密闭容器中加入62g白磷和50.4L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为
您最近一年使用:0次

 2
2

