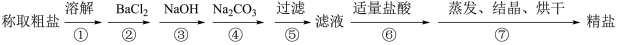草木灰中含有可溶性钾盐(主要成分是 、
、 、
、 )。骉学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤、取滤液;③蒸发滤液;④冷却结晶。
)。骉学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤、取滤液;③蒸发滤液;④冷却结晶。
(1)由草木灰提取钾盐并检验钾元素的存在,下列实验操作中正确的是___________ 。

(2)为检验草木灰中的其它离子,取少量晶体溶于水,并把溶液分成三份,完成以下实验报告(在横线上填写相关的内容):
(3)步骤III所得的结论,你认为是否正确?为什么?___________
(4)写出步骤II有关现象的化学方程式___________ 、___________ 。
 、
、 、
、 )。骉学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤、取滤液;③蒸发滤液;④冷却结晶。
)。骉学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤、取滤液;③蒸发滤液;④冷却结晶。(1)由草木灰提取钾盐并检验钾元素的存在,下列实验操作中正确的是

(2)为检验草木灰中的其它离子,取少量晶体溶于水,并把溶液分成三份,完成以下实验报告(在横线上填写相关的内容):
| 实验步骤 | 实验现象 | 实验结论 |
I. 取第一份溶液和适量稀盐酸加入试管中,把澄清的石灰水加入烧杯中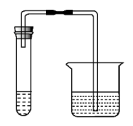 | 证明含有碳酸根离子 | |
| II.取第二份溶液,先后滴加 | 证明含有硫酸根离子 | |
III.取第三份溶液加入过量 溶液,过滤,除去 溶液,过滤,除去 和 和 ,再滴加 ,再滴加 溶液和稀硝酸 溶液和稀硝酸 | 有 | 证明含有氯离子 |
(4)写出步骤II有关现象的化学方程式
更新时间:2022-01-03 07:28:24
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某溶液中可能有下列阴离子中的一种或几种: 、
、 、
、 、
、 。我校化学学习兴趣小组为确定其成分,取abcd四支试管各加入1mL待测液,进行如下操作:
。我校化学学习兴趣小组为确定其成分,取abcd四支试管各加入1mL待测液,进行如下操作:
(1)向a试管中滴加少量稀盐酸溶液无明显现象,写出发生反应的离子方程式:___________ ;继续滴加稀盐酸有气泡产生,写出发生反应的离子方程式:___________ 。
(2)向b试管中滴加硝酸酸化的 溶液后,溶液变浑浊,写出发生反应的离子方程式:
溶液后,溶液变浑浊,写出发生反应的离子方程式:___________ 。
(3)向c试管中滴加盐酸酸化的 溶液后,无明显现象,说明待测液中无
溶液后,无明显现象,说明待测液中无___________ (填离子符号)。
(4)蘸取d试管中的待测液做焰色实验,透过蓝色钴玻璃观察到火焰呈紫色;通过上述4组实验,说明该溶液是___________ (填化学式)。
 、
、 、
、 、
、 。我校化学学习兴趣小组为确定其成分,取abcd四支试管各加入1mL待测液,进行如下操作:
。我校化学学习兴趣小组为确定其成分,取abcd四支试管各加入1mL待测液,进行如下操作:(1)向a试管中滴加少量稀盐酸溶液无明显现象,写出发生反应的离子方程式:
(2)向b试管中滴加硝酸酸化的
 溶液后,溶液变浑浊,写出发生反应的离子方程式:
溶液后,溶液变浑浊,写出发生反应的离子方程式:(3)向c试管中滴加盐酸酸化的
 溶液后,无明显现象,说明待测液中无
溶液后,无明显现象,说明待测液中无(4)蘸取d试管中的待测液做焰色实验,透过蓝色钴玻璃观察到火焰呈紫色;通过上述4组实验,说明该溶液是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4)反应的产物,以其产物为原料制备氯气:室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。分析实验并回答相应问题。
(1)M的化学式是_____ ,组成草酸的三种元素中,非金属性最强的是_____ (填元素符号)。
(2)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为_____ ,向滤液中加入盐酸时又产生无色无味气体,该反应的离子方程式为______ 。
(3)将过滤得到的滤渣洗涤干净,确认滤渣已洗涤干净的操作是_____ 。
(4)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为_____ 。
(5)写出高锰酸钾与草酸溶液发生反应的化学方程式,并用单线桥法表示反应中电子的转移情况:______ 。
(1)M的化学式是
(2)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为
(3)将过滤得到的滤渣洗涤干净,确认滤渣已洗涤干净的操作是
(4)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为
(5)写出高锰酸钾与草酸溶液发生反应的化学方程式,并用单线桥法表示反应中电子的转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】食盐是一种生活必需品,也是重要的工业原料,下图是以NaCl为主要原料的化工生产中物质转化关系图。已知D的水溶液商品名称叫“84”消毒液,C是反应中析出的沉淀。试回答有关问题。
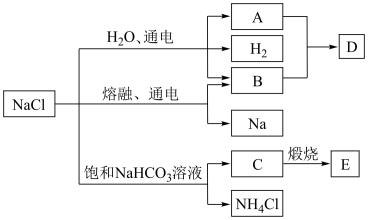
(1)写出A与B反应生成D的离子方程式:___________ 。
(2)C经加热煅烧可得重要化工原料E,写出C煅烧反应的化学方程式:___________ 。
(3)C和E都是白色固体,但二者物理化学性质有较大差别,可利用二者某种物理性质的差别区别这两种晶体,这种物理性质是___________ 。
(4)NaCl与饱和 溶液反应得到C的同时还得到
溶液反应得到C的同时还得到 ,请说出
,请说出 的一种用途:
的一种用途:___________ 。
(5)设计一个实验方案证明NaCl含有Na元素和Cl元素。请说明实验需要的试剂、实验方法、有关现象和你的结论___________ 。

(1)写出A与B反应生成D的离子方程式:
(2)C经加热煅烧可得重要化工原料E,写出C煅烧反应的化学方程式:
(3)C和E都是白色固体,但二者物理化学性质有较大差别,可利用二者某种物理性质的差别区别这两种晶体,这种物理性质是
(4)NaCl与饱和
 溶液反应得到C的同时还得到
溶液反应得到C的同时还得到 ,请说出
,请说出 的一种用途:
的一种用途:(5)设计一个实验方案证明NaCl含有Na元素和Cl元素。请说明实验需要的试剂、实验方法、有关现象和你的结论
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我国科学家屠呦呦因青蒿素研究获得诺贝尔奖,某实验小组拟提取青蒿素
【查阅资料】青蒿素为无色针状晶体,熔点156~157℃,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。实验室用乙醚提取青蒿素的工艺流程如图所示:

(1)在操作I前要对青蒿进行粉碎,其目的是_______ 。
(2)操作II的名称是___________ 。
(3)操作III进行的是重结晶,其操作步骤为加热溶解→____ →____ →过滤、洗涤、干燥。
【查阅资料】青蒿素为无色针状晶体,熔点156~157℃,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。实验室用乙醚提取青蒿素的工艺流程如图所示:

(1)在操作I前要对青蒿进行粉碎,其目的是
(2)操作II的名称是
(3)操作III进行的是重结晶,其操作步骤为加热溶解→
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】利用物质的溶解度对物质进行分离、提纯。图甲、图乙所示为一些物质的溶解度随温度变化的曲线.

(1)A点 溶液是
溶液是______ (填“饱和溶液”或“不饱和溶液”)。
(2)将B点 溶液变成饱和溶液的方法有
溶液变成饱和溶液的方法有________ 。
(3)常温下,由 稀溶液获取
稀溶液获取 固体的方法是
固体的方法是________ 。
(4)常温下由 稀溶液获取
稀溶液获取 固体的方法是
固体的方法是________ 。
(5) 固体中含少量
固体中含少量 ,提纯
,提纯 固体的方式是
固体的方式是________ 。
(6) 固体中含少量
固体中含少量 ,提纯
,提纯 固体的方式是
固体的方式是________ 。
(7)图乙所示为 的溶解度随温度的变化曲线.常温下由
的溶解度随温度的变化曲线.常温下由 稀溶液获取
稀溶液获取 固体的方法是什么?
固体的方法是什么?________ 。

(1)A点
 溶液是
溶液是(2)将B点
 溶液变成饱和溶液的方法有
溶液变成饱和溶液的方法有(3)常温下,由
 稀溶液获取
稀溶液获取 固体的方法是
固体的方法是(4)常温下由
 稀溶液获取
稀溶液获取 固体的方法是
固体的方法是(5)
 固体中含少量
固体中含少量 ,提纯
,提纯 固体的方式是
固体的方式是(6)
 固体中含少量
固体中含少量 ,提纯
,提纯 固体的方式是
固体的方式是(7)图乙所示为
 的溶解度随温度的变化曲线.常温下由
的溶解度随温度的变化曲线.常温下由 稀溶液获取
稀溶液获取 固体的方法是什么?
固体的方法是什么?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下列分离提纯中最适宜的方法是(填字母编号,每空只选一项):
A.洗气 B.升华 C.过滤 D.蒸发结晶 E.蒸馏 F.萃取 G.分液
①除去CO中混有的CO2___________ ;
②用75%的医用酒精制无水乙醇__________ ;
③提取碘水中的碘______________ ;
④从氯化钠和硝酸钾混合液中提取氯化钠_________ ;
⑤除去氯化钠溶液中的泥沙_________ ;
⑥分离植物油和水____________ ;
A.洗气 B.升华 C.过滤 D.蒸发结晶 E.蒸馏 F.萃取 G.分液
①除去CO中混有的CO2
②用75%的医用酒精制无水乙醇
③提取碘水中的碘
④从氯化钠和硝酸钾混合液中提取氯化钠
⑤除去氯化钠溶液中的泥沙
⑥分离植物油和水
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。请回答下列问题:
(1)海带中含有丰富的碘,将海带灼烧、浸泡、过滤,所得的滤液中含有丰富的碘离子。在实验室中进行过滤操作时,需要用到的玻璃仪器为___________ 。
(2) 的化学性质与卤素单质类似,
的化学性质与卤素单质类似, 也具有强氧化性,
也具有强氧化性, 可与氢硫酸(
可与氢硫酸( 的水溶液)反应生成淡黄色沉淀和两种强酸,试写出
的水溶液)反应生成淡黄色沉淀和两种强酸,试写出 和氢硫酸反应的化学方程式:
和氢硫酸反应的化学方程式:___________ 。 和
和 溶液反应生成
溶液反应生成 和
和 ,该反应
,该反应___________ 氧化还原反应(填“是”或“不是”)。
(3)加碘食盐中加入的是 。请回答下列问题:
。请回答下列问题:
①在 溶液中滴加少量
溶液中滴加少量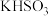 溶液,发生如下反应,请配平并写出该反应方程式
溶液,发生如下反应,请配平并写出该反应方程式___________ 。

②在 溶液中滴加过量
溶液中滴加过量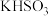 溶液,反应完全,推测反应后溶液中的还原产物为
溶液,反应完全,推测反应后溶液中的还原产物为___________ (填化学式)。(已知:还原性: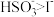 ;氧化性:
;氧化性: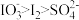 。)
。)
(1)海带中含有丰富的碘,将海带灼烧、浸泡、过滤,所得的滤液中含有丰富的碘离子。在实验室中进行过滤操作时,需要用到的玻璃仪器为
(2)
 的化学性质与卤素单质类似,
的化学性质与卤素单质类似, 也具有强氧化性,
也具有强氧化性, 可与氢硫酸(
可与氢硫酸( 的水溶液)反应生成淡黄色沉淀和两种强酸,试写出
的水溶液)反应生成淡黄色沉淀和两种强酸,试写出 和氢硫酸反应的化学方程式:
和氢硫酸反应的化学方程式: 和
和 溶液反应生成
溶液反应生成 和
和 ,该反应
,该反应(3)加碘食盐中加入的是
 。请回答下列问题:
。请回答下列问题:①在
 溶液中滴加少量
溶液中滴加少量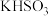 溶液,发生如下反应,请配平并写出该反应方程式
溶液,发生如下反应,请配平并写出该反应方程式
②在
 溶液中滴加过量
溶液中滴加过量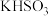 溶液,反应完全,推测反应后溶液中的还原产物为
溶液,反应完全,推测反应后溶液中的还原产物为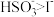 ;氧化性:
;氧化性: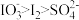 。)
。)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】可用于分离或提纯物质的方法有:a.过滤:b.结晶;c.蒸馏;d.加热;e.分液。请将相应分离提纯物质方法的字母填入空白处:
①除去澄清石灰水中悬浮的CaCO3颗粒:________ 。
②除去CaO中混有的CaCO3:________ 。
③分离酒精和水的混合物:________ 。
④分离水和CCl4的混合物:________ 。
⑤分离NaCl和KNO3的混合物:________ 。
①除去澄清石灰水中悬浮的CaCO3颗粒:
②除去CaO中混有的CaCO3:
③分离酒精和水的混合物:
④分离水和CCl4的混合物:
⑤分离NaCl和KNO3的混合物:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中两次检测结果如下表所示,请回答下列问题:
(1)两次检测结果中第 ___________ 次检测结果不正确。
(2)在检测时,为了检验溶液中是否存在SO 、CO
、CO 和Cl-。
和Cl-。
第一步:向溶液中滴加过量的___________ 溶液(填化学式),其目的是检验CO 并将其除去;发生反应的
并将其除去;发生反应的离子方程式 为___________ ;
第二步:加入过量的___________ 溶液(填化学式),其目的是检验并除去___________ 离子;发生反应的离子方程式 ___________ ;
第三步:过滤,再向滤液中加入___________ 溶液(填化学式),发生反应的离子方程式 ___________ 。
| 检测次数 | 溶液中检测出的粒子 |
| 第①次 | K+ Na+ CO SO SO Cl- Cl- |
| 第②次 | K+ Na+ Ba2+ Cl- SO |
(2)在检测时,为了检验溶液中是否存在SO
 、CO
、CO 和Cl-。
和Cl-。第一步:向溶液中滴加过量的
 并将其除去;发生反应的
并将其除去;发生反应的第二步:加入过量的
第三步:过滤,再向滤液中加入
您最近一年使用:0次
【推荐2】已知: +OH
+OH  NH3↑+H2O。有一瓶溶液只含Cl-、
NH3↑+H2O。有一瓶溶液只含Cl-、 、
、 、Na+、
、Na+、 、K+、Mg2+ 七种离子(忽略水溶液中极少量的H+、OH-)中的某几种。经实验:
、K+、Mg2+ 七种离子(忽略水溶液中极少量的H+、OH-)中的某几种。经实验:
①原溶液 白色沉淀。
白色沉淀。
②将①所得溶液 放出使湿润红色石蕊试纸变蓝的气体。
放出使湿润红色石蕊试纸变蓝的气体。
③原溶液中加BaCl2溶液不产生沉淀。
④原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
回答下列问题:
(1)试分析原溶液中一定含有的离子是_______ ,可能含有的离子是______ 。
(2)有同学认为实验④可以省略,你认为呢?_______ (填符号:A-可以,B -不可以)说明理由:_______ 。
(3)对可能存在的离子,可通过________ 方法进行鉴定。
 +OH
+OH  NH3↑+H2O。有一瓶溶液只含Cl-、
NH3↑+H2O。有一瓶溶液只含Cl-、 、
、 、Na+、
、Na+、 、K+、Mg2+ 七种离子(忽略水溶液中极少量的H+、OH-)中的某几种。经实验:
、K+、Mg2+ 七种离子(忽略水溶液中极少量的H+、OH-)中的某几种。经实验:①原溶液
 白色沉淀。
白色沉淀。②将①所得溶液
 放出使湿润红色石蕊试纸变蓝的气体。
放出使湿润红色石蕊试纸变蓝的气体。③原溶液中加BaCl2溶液不产生沉淀。
④原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
回答下列问题:
(1)试分析原溶液中一定含有的离子是
(2)有同学认为实验④可以省略,你认为呢?
(3)对可能存在的离子,可通过
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。右表是1 L“鲜花保鲜剂”的成分(其中阿司匹林不含K+ ,其存在也不会干扰成分中其他离子的检验),回答下列问题:
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是_____________ (填写名称)。
(2)“鲜花保鲜剂”中K+的物质的量浓度为________________ mol·L-1。(只要求写表达式,不用化简,不需计算)。
(3)下图所示的仪器中,在配制一定量浓度的“鲜花保鲜剂”溶液时肯定不需要的是________ (填字母),还缺少的玻璃仪器有_______________ (填仪器名称)。

(4)市面上,有一种营养液可用于无土栽培,该营养液中有KCl和K2SO4,其中K+的浓度为0.5mol/L,Cl-的浓度为0.1mol/L,则100mL该营养液中n(SO42-)=_______ mol。
(5)欲检验“鲜花保鲜剂”中的硫酸根离子,步骤是:取少量鲜花保鲜剂于试管中,滴加足量的盐酸后,再滴加___________ 溶液,看到______________ ,证明有硫酸根离子。
| 成分 | 质量/g | 摩尔质量/(g·mol-1) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是
(2)“鲜花保鲜剂”中K+的物质的量浓度为
(3)下图所示的仪器中,在配制一定量浓度的“鲜花保鲜剂”溶液时肯定不需要的是

(4)市面上,有一种营养液可用于无土栽培,该营养液中有KCl和K2SO4,其中K+的浓度为0.5mol/L,Cl-的浓度为0.1mol/L,则100mL该营养液中n(SO42-)=
(5)欲检验“鲜花保鲜剂”中的硫酸根离子,步骤是:取少量鲜花保鲜剂于试管中,滴加足量的盐酸后,再滴加
您最近一年使用:0次