回答下列问题:
(1)已知拆开 键、
键、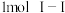 键、
键、 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、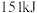 、
、 。则由氢气和碘反应生成1molHI(碘化氢)需要
。则由氢气和碘反应生成1molHI(碘化氢)需要_______ (填“放出”或“吸收”)_______  的热量。
的热量。
(2)发射卫星时可用肼( )为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:①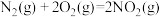
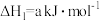
②

写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:_______ 。
(1)已知拆开
 键、
键、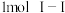 键、
键、 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、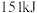 、
、 。则由氢气和碘反应生成1molHI(碘化氢)需要
。则由氢气和碘反应生成1molHI(碘化氢)需要 的热量。
的热量。(2)发射卫星时可用肼(
 )为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:①
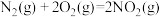
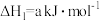
②


写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:
更新时间:2022-01-19 15:57:09
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】甲烷和水蒸气催化制氢主要有如下两个反应:
①CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206kJ/mol
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41kJ/mol
写出CH4与CO2生成H2和CO的热化学方程式:____ 。
①CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206kJ/mol
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41kJ/mol
写出CH4与CO2生成H2和CO的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请回答下列问题:
(Ⅰ)已知化学反应N2+3H2=2NH3的能量变化如图所示,

(1)1mol N 和3mol H 生成1mol NH3(g)是___________ 能量的过程(填“吸收”或“释放”)。
(2) N2(g)+
N2(g)+ H2(g)=NH3(g);△H=
H2(g)=NH3(g);△H=___________ ;
(3)N2(g)和H2(g)生成NH3(1)的热化学方程式为___________
(Ⅱ)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:___________
(Ⅰ)已知化学反应N2+3H2=2NH3的能量变化如图所示,

(1)1mol N 和3mol H 生成1mol NH3(g)是
(2)
 N2(g)+
N2(g)+ H2(g)=NH3(g);△H=
H2(g)=NH3(g);△H=(3)N2(g)和H2(g)生成NH3(1)的热化学方程式为
(Ⅱ)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)贮氢合金ThNi5可催化由CO、H2合成CH4的反应。温度为T时,该反应的热化学方程式为______
已知温度为T时:CH4(g)+2H2O(g)===CO2(g)+4H2(g) ΔH=+165kJ·mol-1
CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=-41kJ·mol-1
(2)用O2将HCl转化为Cl2,可提高效益,减少污染。

传统上该转化通过如图所示的催化循环实现。其中,反应①为:2HCl(g)+CuO(s) H2O(g)+CuCl2(s) ΔH1,反应②生成1molCl2(g)的反应热为ΔH2,则总反应的热化学方程式为
H2O(g)+CuCl2(s) ΔH1,反应②生成1molCl2(g)的反应热为ΔH2,则总反应的热化学方程式为_________________ (反应热用ΔH1和ΔH2表示)。
(3)已知:①Fe2O3(s)+3C(s)===2Fe(s)+3CO(g) ΔH=+494kJ·mol-1
②CO(g)+1/2O2(g)===CO2(g) ΔH=-283kJ·mol-1
③C(s)+1/2O2(g)===CO(g) ΔH=-110kJ·mol-1
则反应Fe2O3(s)+3C(s)+3/2O2(g)===2Fe(s)+3CO2(g)的ΔH=________ kJ·mol-1。理论上反应________ 放出的热量足以供给反应________ 所需要的热量(填上述方程式序号)。
已知温度为T时:CH4(g)+2H2O(g)===CO2(g)+4H2(g) ΔH=+165kJ·mol-1
CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=-41kJ·mol-1
(2)用O2将HCl转化为Cl2,可提高效益,减少污染。

传统上该转化通过如图所示的催化循环实现。其中,反应①为:2HCl(g)+CuO(s)
 H2O(g)+CuCl2(s) ΔH1,反应②生成1molCl2(g)的反应热为ΔH2,则总反应的热化学方程式为
H2O(g)+CuCl2(s) ΔH1,反应②生成1molCl2(g)的反应热为ΔH2,则总反应的热化学方程式为(3)已知:①Fe2O3(s)+3C(s)===2Fe(s)+3CO(g) ΔH=+494kJ·mol-1
②CO(g)+1/2O2(g)===CO2(g) ΔH=-283kJ·mol-1
③C(s)+1/2O2(g)===CO(g) ΔH=-110kJ·mol-1
则反应Fe2O3(s)+3C(s)+3/2O2(g)===2Fe(s)+3CO2(g)的ΔH=
您最近一年使用:0次
【推荐1】氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)===2H2O(1) ΔH=-572kJ·mol-1。请回答下列问题:
(1)生成物能量总和_____ (填“大于”“小于”或“等于”)反应物能量总和。
(2)若2 mol氢气燃烧生成水蒸气,则放出的热量______ (填“大于”“小于”或“等于”)572kJ。
(3)H2的标准燃烧热ΔH=_____ 。
(4)反应2H2+O2 2H2O的能量变化如图所示。
2H2O的能量变化如图所示。

已知拆开1molH2、1molO2和1 mol H—O中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)_____ (填“吸收”或“放出”)_____ kJ。
(1)生成物能量总和
(2)若2 mol氢气燃烧生成水蒸气,则放出的热量
(3)H2的标准燃烧热ΔH=
(4)反应2H2+O2
 2H2O的能量变化如图所示。
2H2O的能量变化如图所示。
已知拆开1molH2、1molO2和1 mol H—O中的化学键分别需要消耗436kJ、496kJ和463kJ的能量。则反应过程(Ⅱ)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】肼( )是一种重要的化工原料,在工农业生产和航天领域应用广泛。回答下列问题:
)是一种重要的化工原料,在工农业生产和航天领域应用广泛。回答下列问题:
(1)已知:
①g表示物质的状态为气态。
②298K时,1mol物质的相对能量如图所示:
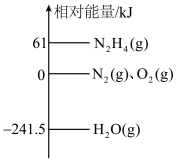
1mol (g)与足量
(g)与足量 (g)完全反应生成
(g)完全反应生成 (g)和
(g)和 (g)
(g)___________ (填吸收或释放)的能量为___________ kJ。
(2)298K时,1mol气态分子中的化学键断裂形成气态原子吸收的能量如下表所示:
a=___________  。
。
(3)根据 (g)与
(g)与 (g)的反应设计肼燃料电池,其工作原理如图所示。
(g)的反应设计肼燃料电池,其工作原理如图所示。
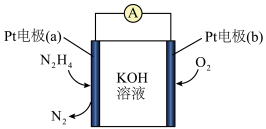
①下列说法正确的是___________ (填序号)。
A.电池工作时,将热能转化为电能 B.Pt电极a的电势低于Pt电极b
C.离子导体中, 向Pt电极b移动 D.电池工作时,KOH的物质的量不变
向Pt电极b移动 D.电池工作时,KOH的物质的量不变
②写出Pt电极a上的电极反应式___________ 。
 )是一种重要的化工原料,在工农业生产和航天领域应用广泛。回答下列问题:
)是一种重要的化工原料,在工农业生产和航天领域应用广泛。回答下列问题:(1)已知:
①g表示物质的状态为气态。
②298K时,1mol物质的相对能量如图所示:

1mol
 (g)与足量
(g)与足量 (g)完全反应生成
(g)完全反应生成 (g)和
(g)和 (g)
(g)(2)298K时,1mol气态分子中的化学键断裂形成气态原子吸收的能量如下表所示:
 (g) (g) |  (g) (g) |  (g) (g) |  (g) (g) |
1757 | a  | 946 | 926 |
 。
。(3)根据
 (g)与
(g)与 (g)的反应设计肼燃料电池,其工作原理如图所示。
(g)的反应设计肼燃料电池,其工作原理如图所示。
①下列说法正确的是
A.电池工作时,将热能转化为电能 B.Pt电极a的电势低于Pt电极b
C.离子导体中,
 向Pt电极b移动 D.电池工作时,KOH的物质的量不变
向Pt电极b移动 D.电池工作时,KOH的物质的量不变②写出Pt电极a上的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】人们常常利用化学反应中的能量变化为人类服务。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧生成水蒸气的能量变化如下图所示: 完全燃烧生成1 mol
完全燃烧生成1 mol 时,释放的能量是
时,释放的能量是______ kJ。
(2)下列化学反应在理论上可以设计成原电池的是______。
(3)下图是某兴趣小组设计的原电池示意图:_____________ 。
②将稀 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是______ (填“锌极”或“铜极”,下同),溶液中 移向
移向______ 。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧生成水蒸气的能量变化如下图所示:
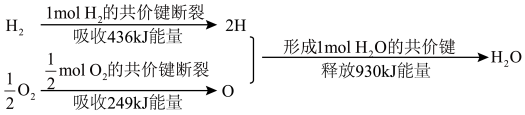
 完全燃烧生成1 mol
完全燃烧生成1 mol 时,释放的能量是
时,释放的能量是(2)下列化学反应在理论上可以设计成原电池的是______。
A.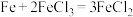 | B. |
C.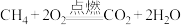 | D.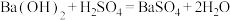 |
(3)下图是某兴趣小组设计的原电池示意图:
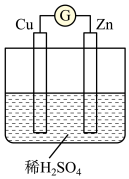
②将稀
 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是 移向
移向
您最近一年使用:0次



