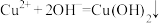对于下列实验,能正确描述其反应的离子方程式是
| A.向H2O2溶液中滴加少量HI溶液:2HI+H2O2=I2+2H2O |
| B.向CaCl2溶液中通入CO2:Ca2++H2O+CO2=CaCO3↓+2H+ |
C.用浓盐酸与二氧化锰反应制取氯气:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
D.同浓度同体积NH4HSO4溶液与NaOH溶液混合:NH +OH-=NH3·H2O +OH-=NH3·H2O |
更新时间:2022-01-20 11:01:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式正确的是
A.用醋酸和淀粉-KI溶液检验加碘盐中的 : : |
B.向 溶液中加入过量的 溶液中加入过量的 溶液: 溶液: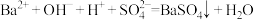 |
| C.向澄清石灰水中通入足量CO2:Ca2++2OH—+CO2=CaCO3↓+H2O |
D.明矾溶液与过量氨水混合:Al3++4NH3+4H2O=[Al(OH)4]—+4NH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式书写正确的是
| A.在氯化铝溶液中滴加过量的氨水:Al3++4OH-=[Al(OH)4]- |
B.酸性溶液中KIO3与KI反应生成I2:IO +5I-+6H+=3I2+3H2O +5I-+6H+=3I2+3H2O |
| C.标准状况下将112 mL氯气通入10 mL 1 mol·L-1的溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
D.向Mg(HCO3)2溶液中加入足量澄清石灰水:Mg2++2HCO +2Ca2++2OH-=Mg(OH)2↓+2CaCO3↓+2H2O +2Ca2++2OH-=Mg(OH)2↓+2CaCO3↓+2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列离子方程式错误的是
A.用新制 浊液检验淀粉的水解产物: 浊液检验淀粉的水解产物: |
B.在 浊液中滴加 浊液中滴加 溶液产生黄色沉淀: 溶液产生黄色沉淀: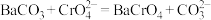 |
C.等体积等浓度的 溶液和 溶液和 溶液混合: 溶液混合: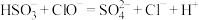 |
D.相同浓度的 溶液和 溶液和 溶液等体积混合: 溶液等体积混合: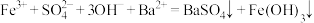 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列指定反应的离子方程式正确的是
A.铜与稀硝酸反应: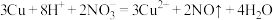 |
B.AgNO3溶液中加入过量氨水: |
C.向NaClO溶液中通入足量SO2气体: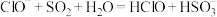 |
D.用惰性电极电解NaCl溶液: |
您最近一年使用:0次
【推荐3】高铁酸钾纯品为暗紫色有光泽粉末。在198  以下干燥空气中稳定。极易溶于水而形成浅紫红色溶液,静置后会分解放出氧气,并沉淀出水合三氧化二铁。溶液的碱性随分解而增大,在强碱性溶液中相当稳定,是极好的氧化剂。具有高效的消毒作用,比高锰酸钾具有更强的氧化性。高铁酸钾的分子式为K2FeO4,工业制备高铁酸钾的离子方程式为
以下干燥空气中稳定。极易溶于水而形成浅紫红色溶液,静置后会分解放出氧气,并沉淀出水合三氧化二铁。溶液的碱性随分解而增大,在强碱性溶液中相当稳定,是极好的氧化剂。具有高效的消毒作用,比高锰酸钾具有更强的氧化性。高铁酸钾的分子式为K2FeO4,工业制备高铁酸钾的离子方程式为 (未配平),下列有关说法不正确的是
(未配平),下列有关说法不正确的是
 以下干燥空气中稳定。极易溶于水而形成浅紫红色溶液,静置后会分解放出氧气,并沉淀出水合三氧化二铁。溶液的碱性随分解而增大,在强碱性溶液中相当稳定,是极好的氧化剂。具有高效的消毒作用,比高锰酸钾具有更强的氧化性。高铁酸钾的分子式为K2FeO4,工业制备高铁酸钾的离子方程式为
以下干燥空气中稳定。极易溶于水而形成浅紫红色溶液,静置后会分解放出氧气,并沉淀出水合三氧化二铁。溶液的碱性随分解而增大,在强碱性溶液中相当稳定,是极好的氧化剂。具有高效的消毒作用,比高锰酸钾具有更强的氧化性。高铁酸钾的分子式为K2FeO4,工业制备高铁酸钾的离子方程式为 (未配平),下列有关说法不正确的是
(未配平),下列有关说法不正确的是A.由上述反应可知,Fe(OH)3的氧化性强于 |
| B.高铁酸钾中铁显 + 6价 |
| C.上述反应氧化剂和还原剂的物质的量之比为3 : 2 |
| D.K2FeO4处理水时,不仅能消毒杀菌,而且生成Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】历史上曾利用“地康法”制氯气,其原理是以氯化铜作催化剂,利用氧气氧化氯化氢。如图为“地康法”制氯气的模拟装置.下列关有说法不正确的是


| A.关闭K2打开K1,若漏斗中的液面不持续下降,则装置1的气密性良好 |
| B.打开K3,将浓盐酸逐滴滴入浓硫酸中可制备反应所需要的氯化氢 |
| C.装置2中盛放的是浓硫酸,通过观察气泡逸出的快慢可判断气体的通入量 |
| D.后续需要净化氯气的装置中,除杂试剂依次为饱和食盐水、碱石灰 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列用如图装置(加热及夹持仪器已略去)进行的实验,不能达到相应实验目的的是


A.装置①中的a可用于吸收尾气中的 ,b可用于吸收气体时防倒吸 ,b可用于吸收气体时防倒吸 |
B.装置②可实现制取 实验中的“即关即止,即开即用”的作用 实验中的“即关即止,即开即用”的作用 |
C.利用装置③制取 ,并验证其还原性 ,并验证其还原性 |
D.利用装置④验证 和 和 的热稳定性,X中应放的物质是 的热稳定性,X中应放的物质是 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】第26届国际计量大会通过“修订国际单位制"决议,以阿伏加德罗常数定义物质的量的单位——摩尔,可大大提高稳定性和精确度。NA表示阿伏加德罗常数的值,下列说法正确的是
| A.12g金刚石中含有的共用电子对数为NA |
| B.一定条件下,含4molHCl的浓盐酸与足量MnO2充分反应,转移电子数为2NA |
| C.标准状况下,2.24LCl2与CH4反应完全,形成C-Cl键的数目为0.1NA |
| D.常温下,pH=10的CH3COONa溶液中,由水电离出的H+的数目为10-4NA |
您最近一年使用:0次

 +2H+=S↓+SO2↑+H2O
+2H+=S↓+SO2↑+H2O +
+ +H2O= Al(OH)3↓+
+H2O= Al(OH)3↓+
 溶液中滴加稀氨水:
溶液中滴加稀氨水: